1. 领域背景与文献
文献英文标题:Non-Genetically Modified Adoptive Cell Therapies for Solid Tumors: Current Landscape and Future Challenges;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:实体瘤肿瘤免疫治疗。
实体瘤是全球肿瘤相关死亡的主要原因,传统放化疗虽可在一定程度上控制肿瘤进展,但常伴随严重不良反应与耐药问题,患者长期生存率较低。领域共识:免疫治疗是当前实体瘤治疗的核心发展方向,其中嵌合抗原受体T细胞(CAR-T)等基因编辑过继细胞疗法在血液肿瘤中已取得突破性疗效,但在实体瘤中仍面临脱靶毒性、免疫抑制肿瘤微环境限制、抗原逃逸、T细胞耗竭等多重瓶颈,临床转化率较低。
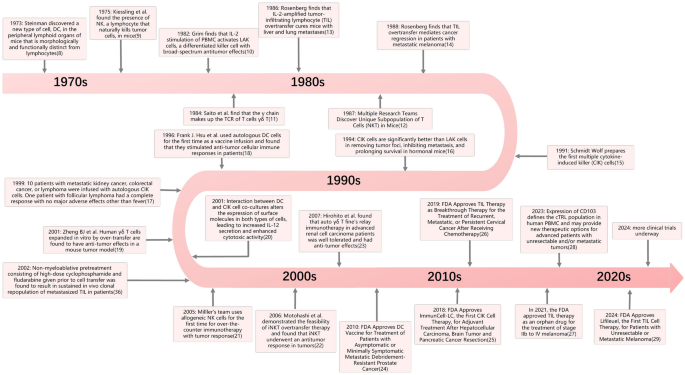
非基因修饰过继细胞疗法利用天然存在或体外活化的免疫细胞,规避了基因编辑带来的插入突变、自身免疫反应等风险,安全性更高,是实体瘤免疫治疗的重要分支。该领域的关键发展节点包括1968年明确T细胞的核心免疫功能,1973年发现树突状细胞,1980年代美国国立卫生研究院Rosenberg团队首次证实肿瘤浸润淋巴细胞(TIL)的抗肿瘤活性,1991年报道细胞因子诱导的杀伤细胞(CIK),2024年美国食品药品监督管理局(FDA)批准首个肿瘤浸润淋巴细胞疗法lifileucel用于晚期黑色素瘤治疗,标志着该类疗法正式进入临床应用阶段。
当前该领域的研究热点主要包括不同类型非基因修饰免疫细胞的临床转化、与免疫检查点抑制剂的联合方案优化、细胞规模化扩增工艺的标准化等,尚未解决的核心问题包括体外扩增效率不足、不同中心生产方案差异大导致临床结果异质性高、肿瘤微环境对输注细胞的抑制机制尚未完全阐明、缺乏预测疗效的特异性生物标志物等。本综述旨在系统梳理非基因修饰过继细胞疗法的作用机制、临床进展与现存局限,提出可落地的联合治疗优化方向,填补该领域从基础研究到临床转化的策略空白,为实体瘤免疫治疗提供新的范式参考。
2. 文献综述解析
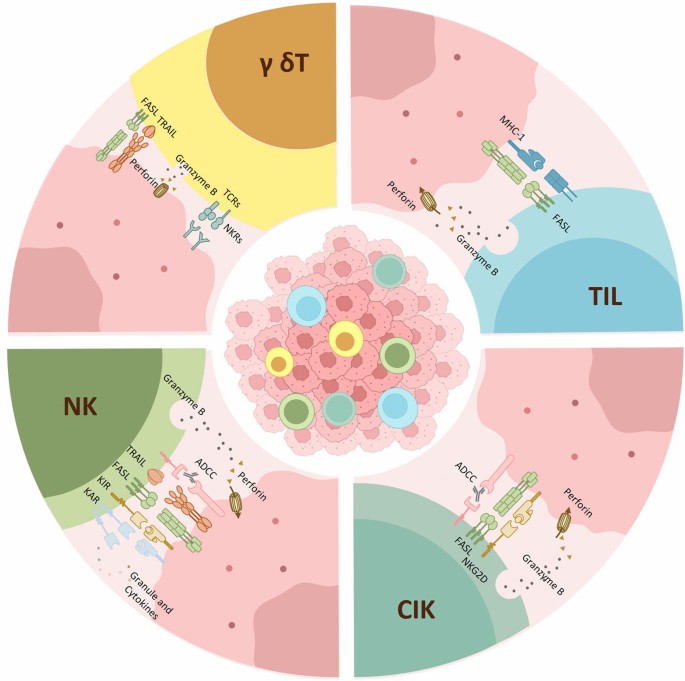
作者按细胞类型对非基因修饰过继细胞疗法的现有研究进行分类评述,涵盖肿瘤浸润淋巴细胞、细胞因子诱导的杀伤细胞/树突状细胞共培养(DC-CIK)、自然杀伤细胞(NK)、γδ T细胞四大类,从作用机制、临床证据、局限性三个维度进行结构化总结,系统对比了不同疗法的优劣势与适用场景。
现有研究的支持观点主要包括:非基因修饰细胞疗法无需进行基因操作,避免了基因编辑相关的遗传毒性、插入致瘤等风险,临床安全性更优;肿瘤浸润淋巴细胞具有天然的肿瘤抗原特异性,杀伤活性更精准,在黑色素瘤、非小细胞肺癌中已展现出明确的临床获益;细胞因子诱导的杀伤细胞兼具T细胞和自然杀伤细胞的特性,不受主要组织相容性复合体(MHC)限制,适用人群更广,在肝癌术后辅助治疗中已被纳入美国国家综合癌症网络(NCCN)指南推荐;自然杀伤细胞和γδ T细胞可识别抗原丢失的肿瘤变异株,降低肿瘤逃逸风险,且异体来源产品无移植物抗宿主病(GvHD)风险,具备“现货型”产品的开发潜力。
现有研究的技术优势包括:肿瘤浸润淋巴细胞可直接识别患者肿瘤的新生抗原,对异质性较高的实体瘤杀伤活性更强;细胞因子诱导的杀伤细胞体外扩增工艺成熟,生产成本较低,适合基层推广;自然杀伤细胞无需抗原预致敏,可快速启动抗肿瘤免疫反应,适合联合单克隆抗体治疗以增强抗体依赖的细胞介导的细胞毒性(ADCC)效应;γδ T细胞是多种实体瘤的阳性预后指标,兼具固有免疫和适应性免疫的特性,抗肿瘤谱更广。
现有研究的局限性主要包括:多数临床研究为小样本单中心试验,缺乏大样本III期循证医学证据;不同中心的细胞扩增工艺、质控标准差异较大,导致临床结果的异质性较高,难以进行跨研究比较;单独应用非基因修饰细胞疗法的客观缓解率普遍低于30%,在免疫“冷肿瘤”中的疗效尤为有限;缺乏预测疗效的特异性生物标志物,无法实现精准的患者分层,部分患者无法从中获益。
本综述的创新价值在于,首次系统整合了四类非基因修饰过继细胞疗法的临床前与临床数据,明确了当前领域的三大核心挑战,即体外扩增效率低、生产方案缺乏标准化、肿瘤微环境对输注细胞的活性抑制,提出了基于生物标志物患者分层、细胞因子优化、联合免疫检查点抑制剂/代谢调节剂的可落地解决方案,填补了该领域系统性策略梳理的空白,为后续的临床转化研究提供了明确的方向。
3. 研究思路总结与详细解析
本综述的核心研究目标是系统梳理非基因修饰过继细胞疗法在实体瘤中的应用现状与瓶颈,提出可落地的优化策略以推动其临床转化,核心科学问题是如何通过方案优化解决非基因修饰细胞疗法的疗效局限性,技术路线遵循“发展历程梳理→分细胞类型机制与临床证据总结→核心挑战提炼→优化策略提出”的逻辑框架,所有结论均基于已发表的同行评议研究数据。
3.1 肿瘤浸润淋巴细胞疗法进展解析
本部分的核心实验目的是明确肿瘤浸润淋巴细胞疗法的作用机制、临床证据与优化方向。采用的研究方法为系统梳理已发表的临床试验数据,肿瘤浸润淋巴细胞的常规制备流程为从患者手术切除的肿瘤组织中分离淋巴细胞,在含白细胞介素-2(IL-2)的培养基中体外扩增,患者经非清髓性淋巴细胞清除预处理后回输细胞,部分研究联合免疫检查点抑制剂使用。
对应的研究结果显示,首个获批的肿瘤浸润淋巴细胞产品lifileucel在经免疫检查点抑制剂和靶向治疗进展的晚期黑色素瘤患者中客观缓解率为31.4%(n=153),41.7%的缓解持续时间≥18个月;在经治的转移性非小细胞肺癌患者中客观缓解率为21.4%(n=28);与帕博利珠单抗联合用于初治转移性非小细胞肺癌时客观缓解率可达47.1%,尤其是表皮生长因子受体(EGFR)野生型、程序性死亡配体1(PD-L1)阴性患者的获益更显著。研究证实,输注的肿瘤浸润淋巴细胞中CD8+T细胞比例、肿瘤组织中基线CD8+肿瘤浸润淋巴细胞浸润水平与临床疗效正相关,基线CD8+肿瘤浸润淋巴细胞比例≥10%的患者客观缓解率为45%,显著高于比例低于10%的患者的12%(P<0.01),且输注产品中干细胞样转录因子7阳性(TCF7+)CD8+T细胞亚型的体内持久性更优,与长期获益相关。
本部分涉及的实验产品文献未明确提及,领域常规使用重组人白细胞介素-2、抗CD3单克隆抗体用于肿瘤浸润淋巴细胞的体外扩增,非清髓性预处理常用环磷酰胺、氟达拉滨。
3.2 细胞因子诱导的杀伤细胞与树突状细胞共培养疗法进展解析
本部分的核心实验目的是明确细胞因子诱导的杀伤细胞与树突状细胞共培养疗法的抗肿瘤机制、临床应用证据与适用场景。采用的研究方法为系统回顾已发表的随机对照试验数据,细胞因子诱导的杀伤细胞的常规制备流程为从患者外周血单个核细胞中分离淋巴细胞,依次加入干扰素-γ(IFN-γ)、抗CD3单克隆抗体、重组人白细胞介素-2体外扩增,与负载肿瘤抗原的树突状细胞共培养可增强细胞因子诱导的杀伤细胞的杀伤活性,回输前无需清髓性预处理。
对应的研究结果显示,细胞因子诱导的杀伤细胞联合化疗用于晚期鳞状非小细胞肺癌可延长无进展生存期4.7个月、总生存期10.7个月,且未增加不良反应发生率;肝癌术后辅助治疗的III期试验显示,细胞因子诱导的杀伤细胞治疗可延长中位无复发生存期至44.0个月,对照组为30.0个月(P=0.01),5年总生存率提升21%(66% vs 45%,P=0.008)。树突状细胞共培养的细胞因子诱导的杀伤细胞联合化疗可显著提升实体瘤患者的总生存期、无病生存期与客观缓解率,但由于抗原负载方案不统一、研究人群异质性大,其疗效相较于细胞因子诱导的杀伤细胞单药未展现出统计学差异。
本部分涉及的实验产品文献未明确提及,领域常规使用重组人干扰素-γ、抗CD3单克隆抗体、重组人白细胞介素-2用于细胞因子诱导的杀伤细胞的体外扩增。
3.3 自然杀伤细胞疗法进展解析
本部分的核心实验目的是明确自然杀伤细胞疗法的抗肿瘤机制、来源差异与临床转化潜力。采用的研究方法为系统对比不同来源自然杀伤细胞的临床前与临床数据,自然杀伤细胞可来源于自体/异体外周血、脐带血、NK-92细胞系、诱导多能干细胞(iPSC),体外经多种细胞因子刺激扩增后回输,可联合单克隆抗体增强抗体依赖的细胞介导的细胞毒性作用。
对应的研究结果显示,异体自然杀伤细胞通过杀伤免疫球蛋白样受体(KIR)配体错配避免自体主要组织相容性复合体I类分子的抑制信号,临床安全性良好,无移植物抗宿主病风险;在表皮生长因子受体突变阳性的晚期肺腺癌中,自体自然杀伤细胞联合阿法替尼可显著提升缓解率;与抗人表皮生长因子受体2(HER2)单克隆抗体联合时可通过抗体依赖的细胞介导的细胞毒性增强对HER2阳性乳腺癌等实体瘤的杀伤活性,但单独应用的客观缓解率较低,受肿瘤微环境中免疫抑制因子的影响较大。
本部分涉及的实验产品文献未明确提及,领域常规使用白细胞介素-2、白细胞介素-15、白细胞介素-12等细胞因子用于自然杀伤细胞的体外扩增与活化。
3.4 γδ T细胞疗法进展解析
本部分的核心实验目的是明确γδ T细胞疗法的抗肿瘤机制、临床应用现状与优化方向。采用的研究方法为系统梳理γδ T细胞的临床研究证据,γδ T细胞的常规制备流程为从患者外周血中分离γδ T细胞,经唑来膦酸、白细胞介素-2等刺激体外扩增后回输,可通过磷酸抗原特异性识别、自然杀伤受体介导识别等方式杀伤肿瘤细胞,不受主要组织相容性复合体限制。
对应的研究结果显示,γδ T细胞是25种癌症中最强的阳性预后指标,临床研究显示其在晚期肾细胞癌、转移性实体瘤中安全性良好,异体γδ T细胞治疗可延长晚期肺癌、肝癌患者的生存时间,但目前临床研究多为I/II期,单独应用的客观缓解率约为18%,缺乏大样本III期证据。
本部分涉及的实验产品文献未明确提及,领域常规使用唑来膦酸、白细胞介素-2用于γδ T细胞的体外扩增。
3.5 核心挑战与优化策略解析
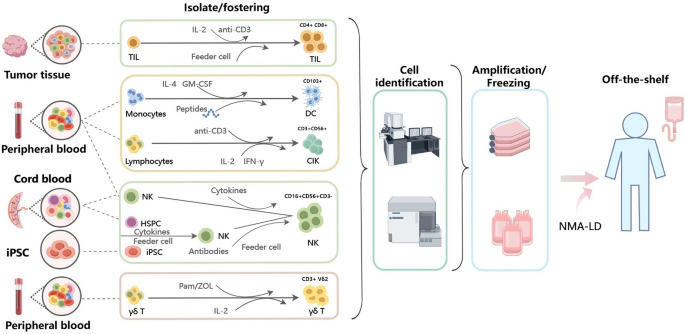
本部分的核心实验目的是提炼非基因修饰过继细胞疗法的共性挑战,提出可落地的优化方向。采用的研究方法为整合已发表的临床前与临床研究数据,从细胞生产、临床方案、患者分层三个维度分析瓶颈,提出对应的解决策略。
对应的研究结果显示,当前领域的三大核心挑战为:体外扩增效率低、生产方案缺乏标准化、肿瘤微环境抑制导致细胞体内活性不足。优化策略主要包括三个方向:第一是联合治疗,与免疫检查点抑制剂、代谢调节剂、局部治疗(放疗、经动脉化疗栓塞)联用,重塑肿瘤微环境,提升细胞浸润与活性;第二是扩增方案标准化,建立统一的细胞质量评价体系,引入代谢功能评分、类器官杀伤模型评估细胞活性,缩短生产周期,如新型肿瘤浸润淋巴细胞Gen-2扩增方案可将生产时间缩短至22天,且细胞的抗肿瘤活性更优;第三是生物标志物指导的患者分层,基于基线肿瘤浸润淋巴细胞浸润水平、程序性死亡配体1表达、T细胞受体(TCR)克隆性等指标筛选获益人群,提升治疗精准度。
本部分涉及的实验产品文献未明确提及,领域常规使用单细胞测序、空间多组学技术用于肿瘤微环境分析,患者来源类器官用于细胞杀伤活性的预评估。
4. 生物标志物研究及发现成果
本综述梳理的非基因修饰过继细胞疗法相关生物标志物主要涵盖疗效预测类与细胞产品质量类两大类型,筛选验证逻辑遵循“临床相关性分析→功能验证→临床队列验证”的路径,目前已有部分标志物展现出潜在的临床应用价值,但仍缺乏大样本队列的统一验证。
疗效预测类生物标志物的来源主要为患者基线肿瘤组织与外周血样本,验证方法包括免疫组化(IHC)、流式细胞术、T细胞受体测序等。已报道的具有潜在预测价值的标志物包括:第一是肿瘤组织基线CD8+肿瘤浸润淋巴细胞浸润水平,基线CD8+肿瘤浸润淋巴细胞比例≥10%的黑色素瘤患者接受肿瘤浸润淋巴细胞治疗的客观缓解率为45%,显著高于比例低于10%的患者的12%(P<0.01),是目前证据最充分的预测标志物;第二是程序性死亡配体1表达,程序性死亡配体1阳性的乳腺癌患者接受细胞因子诱导的杀伤细胞治疗的获益更显著;第三是输注细胞的表型,肿瘤浸润淋巴细胞产品中干细胞样转录因子7阳性CD8+T细胞比例与体内持久性正相关,细胞因子诱导的杀伤细胞产品中CD3+CD56+细胞比例≥30%时临床获益更显著;第四是T细胞受体克隆性,输注的肿瘤浸润淋巴细胞产品中T细胞受体多样性过高提示非肿瘤反应性克隆占比高,与较差的预后相关。
细胞产品质量类生物标志物主要用于生产过程中的质控,包括细胞活率、效应细胞比例、细胞因子分泌水平等,目前已有79%的临床试验设定了明确的细胞质量阈值,如要求细胞因子诱导的杀伤细胞产品中CD3+CD56+细胞比例≥30%,以保障产品的一致性。
本综述在生物标志物领域的核心成果为,首次提出应建立“基线组织标志物+输注细胞质量标志物+动态循环标志物”的多维度预测体系,其中动态监测外周血T细胞受体克隆演变可实时评估输注细胞的体内持久性,为疗效预测提供新的方向。目前现有生物标志物的敏感性、特异性数据尚未有大样本队列的统一验证,cut-off值也尚未标准化,仍需后续研究进一步明确。
推测:未来可通过空间多组学技术挖掘更多与非基因修饰细胞疗法疗效相关的微环境标志物,结合输注细胞的多组学特征,构建精准的疗效预测模型,进一步提升该类疗法的临床获益率,需大样本前瞻性队列验证。
