1. 领域背景与文献
文献英文标题:Stereotactic ablative radiotherapy-driven immunosuppression is associated with poorer progression-free survival in cancer patients;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:肿瘤放射免疫学。
肿瘤治疗领域在近50年间发展迅速,手术、化疗、放疗仍是主流治疗方案,同时免疫治疗单药或联合其他治疗手段的应用占比逐年提升。领域共识认为,放疗具有免疫原性,可诱导抗原特异性T细胞活化,识别照射野之外的远端肿瘤病灶(即远隔效应),这一范式推动了放疗联合免疫治疗的相关研究。1995年学界提出寡转移概念,指出肿瘤局限转移的状态可通过局部治疗实现根治,为立体定向消融放疗(stereotactic ablative radiotherapy,SABR)的临床应用提供了理论基础。2010年前后立体定向消融放疗进入临床常规应用,其高精度的剂量递送模式可在降低周围正常组织损伤的同时,给予肿瘤病灶更高的消融剂量,且疗程短于常规放疗。2019年发布的SABR-COMET II期临床试验结果显示,立体定向消融放疗可将寡转移患者的无进展生存期从标准治疗的6个月延长至12个月,总生存期延长13个月,证实了其临床价值。
当前领域仍存在多个未解决的核心问题:一是立体定向消融放疗对全身免疫系统的动态调控机制尚不明确,现有研究多聚焦其免疫激活效应,对潜在的免疫抑制作用关注不足;二是患者接受立体定向消融放疗后的预后异质性较大,缺乏可早期预测疗效的动态生物标志物;三是放疗剂量、靶区体积等参数与免疫变化、预后的关联尚未明确,无法指导临床方案优化。本研究针对上述空白,通过纵向采集患者立体定向消融放疗前后的外周血样本,系统分析免疫细胞亚群、细胞因子、抗原特异性T细胞功能的动态变化,明确免疫扰动与患者预后的关联,为优化立体定向消融放疗的临床应用提供依据。
2. 文献综述解析
本研究的文献综述部分按照研究主题分为立体定向消融放疗的临床疗效、放疗的免疫调控效应两个分类维度,系统梳理了领域内的现有进展与局限性。
现有临床研究证实,立体定向消融放疗对寡转移病灶的局部控制率高,可显著延长患者的无进展生存期与总生存期,是寡转移患者的标准治疗方案之一;基础与转化研究显示,放疗可通过诱导免疫原性细胞死亡,释放肿瘤相关抗原,激活先天与适应性免疫应答,为放疗联合免疫治疗提供了理论支撑;回顾性临床研究发现,基线中性粒细胞淋巴细胞比(neutrophil-to-lymphocyte ratio,NLR)可作为多种实体瘤患者放疗后的预后标志物,具有检测便捷、成本低廉的优势。
现有研究仍存在明显局限性:多聚焦立体定向消融放疗的临床疗效与局部肿瘤微环境的变化,缺乏对治疗前后全身免疫动态变化的纵向分析;多数研究仅关注放疗的免疫激活效应,忽略了放疗诱导的淋巴细胞减少等免疫抑制作用及其对预后的影响;现有预后标志物多为基线静态指标,对治疗过程中动态变化的免疫特征关注不足,预测效能有限。
本研究的创新价值显著,首次通过多时间点纵向采样,系统分析了立体定向消融放疗对全身免疫细胞亚群、炎症因子、抗原特异性T细胞功能的影响,明确了立体定向消融放疗诱导的淋巴细胞减少及中性粒细胞淋巴细胞比升高与不良预后的因果关联,弥补了现有研究对立体定向消融放疗免疫抑制效应认知的不足,首次提出治疗期间中性粒细胞淋巴细胞比的动态变化可作为预后预测标志物,为后续优化放疗方案、联合免疫干预策略提供了高质量的临床证据。
3. 研究思路总结与详细解析
本研究的核心目标是明确立体定向消融放疗对肿瘤患者全身免疫系统的调控作用,鉴定可预测患者无进展生存期的免疫特征;核心科学问题为立体定向消融放疗诱导的免疫变化如何影响患者预后;整体技术路线为“患者队列招募→多时间点外周血采集→多维度免疫指标检测→免疫特征与临床预后的关联分析→结论验证”的闭环逻辑。
3.1 患者队列构建与样本采集
实验目的:构建符合研究纳入标准的立体定向消融放疗治疗队列,获取治疗前后多个时间点的外周血样本,为后续免疫分析提供材料。
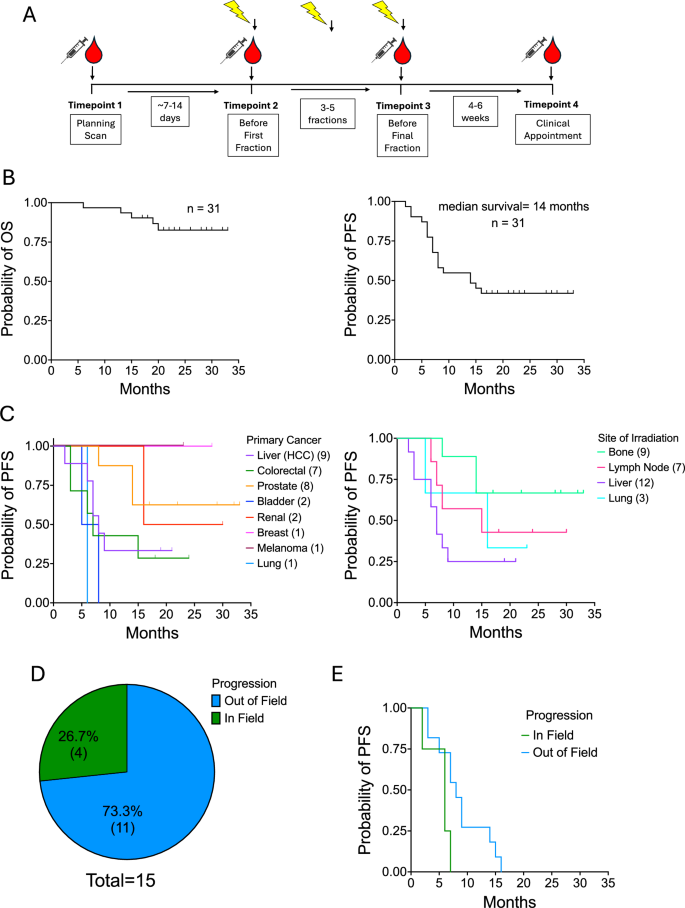
方法细节:研究经伦理委员会批准,纳入31例经多学科团队评估符合立体定向消融放疗指征的原发或寡转移肿瘤患者,排除年龄小于18岁、合并严重免疫缺陷、使用抗排斥药物或大剂量糖皮质激素的患者。分别在4个时间点采集30-50ml肝素抗凝全血:治疗前规划扫描时(TP1)、首次分割放疗前(TP2)、末次分割放疗前(TP3)、治疗后4-6周(TP4),其中TP1与TP2的检测结果合并为治疗前基线均值,与TP3(治疗中)、TP4(治疗后)的结果进行对比。
结果解读:研究队列共包含8种原发肿瘤类型,中位随访时间为23个月,随访期间5例患者死亡,17例患者出现疾病进展,其中多数进展发生在照射野之外,接受肝脏病灶立体定向消融放疗的患者无进展生存期最短。
实验所用关键产品:BD的肝素采血管(货号368480)、STEMCELL Technologies的淋巴细胞分离液(货号07851)、BioLegend的红细胞裂解液(货号420301)、Sigma-Aldrich的碘化丙啶染色试剂(货号P4864)、Agilent的Novocyte自动采样器。
3.2 外周血免疫细胞亚群动态分析
实验目的:分析立体定向消融放疗治疗前后外周血免疫细胞亚群的动态变化规律,明确放疗对全身免疫细胞组成的影响。
方法细节:采用临床全血细胞计数检测各时间点淋巴细胞、单核细胞、中性粒细胞的绝对计数;采用流式细胞术检测淋巴细胞亚群(CD4+T细胞、CD8+T细胞、B细胞、自然杀伤细胞)的比例与绝对计数,以及T细胞表面程序性死亡受体1的表达水平、调节性T细胞的比例。
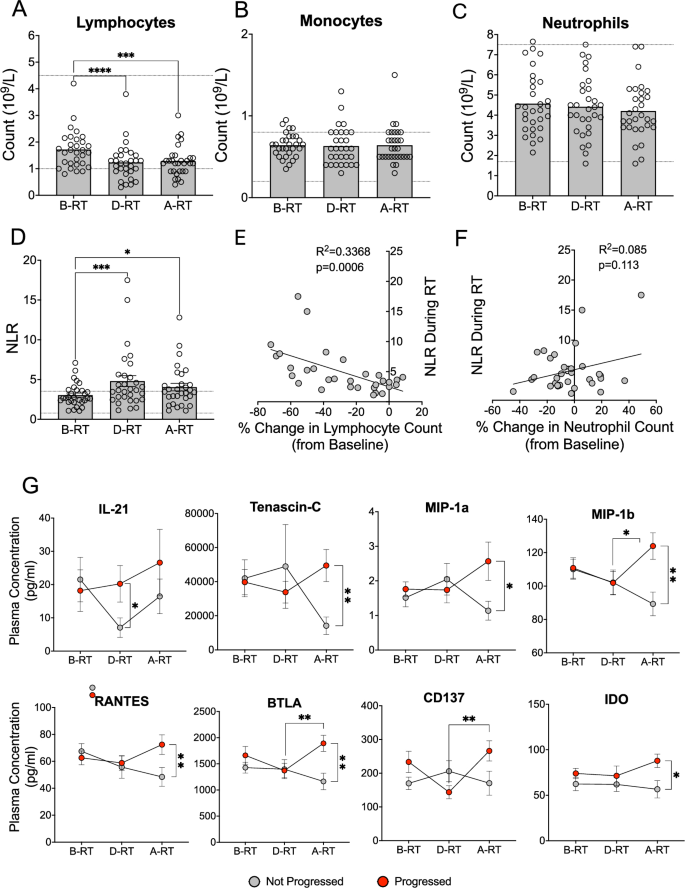
结果解读:全血细胞计数结果显示,立体定向消融放疗治疗后患者淋巴细胞计数较基线显著降低(n=30,P<0.0001),且降低趋势持续至治疗后4-6周(n=30,P=0.0002),部分患者淋巴细胞计数降至淋巴细胞减少症阈值(<1×10^9细胞/升)以下;CD4+T细胞、CD8+T细胞、B细胞、自然杀伤细胞的计数均出现显著降低,而单核细胞、中性粒细胞计数无明显变化。剩余T细胞中CD4+T细胞比例轻微升高,CD8+T细胞比例轻微降低,程序性死亡受体1的表达无显著变化。淋巴细胞计数的显著降低导致中性粒细胞淋巴细胞比较基线显著升高(n=30,P=0.0001),且升高持续至治疗后4-6周(n=30,P=0.0135);相关性分析显示,中性粒细胞淋巴细胞比的升高与淋巴细胞计数的变化呈显著负相关(n=30,P=0.0006),与中性粒细胞计数无显著相关性,提示中性粒细胞淋巴细胞比的升高完全由淋巴细胞减少驱动。
实验所用关键产品:BioLegend的人TBNK 6色鸡尾酒抗体(货号391503)、Invitrogen的活死细胞染色试剂(货号L34957)、Thermo Fisher的固定/破膜试剂盒(货号00-5523-00)、Agilent的Novocyte 3000流式细胞仪。
3.3 抗原特异性T细胞功能检测
实验目的:评估立体定向消融放疗对病毒抗原和肿瘤相关抗原特异性T细胞功能的影响,明确放疗对效应与记忆T细胞功能的调控差异。
方法细节:采用酶联免疫斑点试验(ELISpot)检测外周血单个核细胞对病毒肽池(巨细胞病毒、EB病毒、流感病毒组成的CEF肽池,及在此基础上增加破伤风毒素、腺病毒的CEFTA肽池)、肿瘤相关抗原肽池(滋养层糖蛋白5T4、热休克蛋白家族成员DNAJB7、癌胚抗原相关细胞黏附分子3、锌指蛋白ZSWIM1)的干扰素-γ分泌水平;采用离体酶联免疫斑点试验(直接孵育抗原)检测效应T细胞功能,采用抗原预刺激培养10-14天后的培养酶联免疫斑点试验检测记忆T细胞功能。
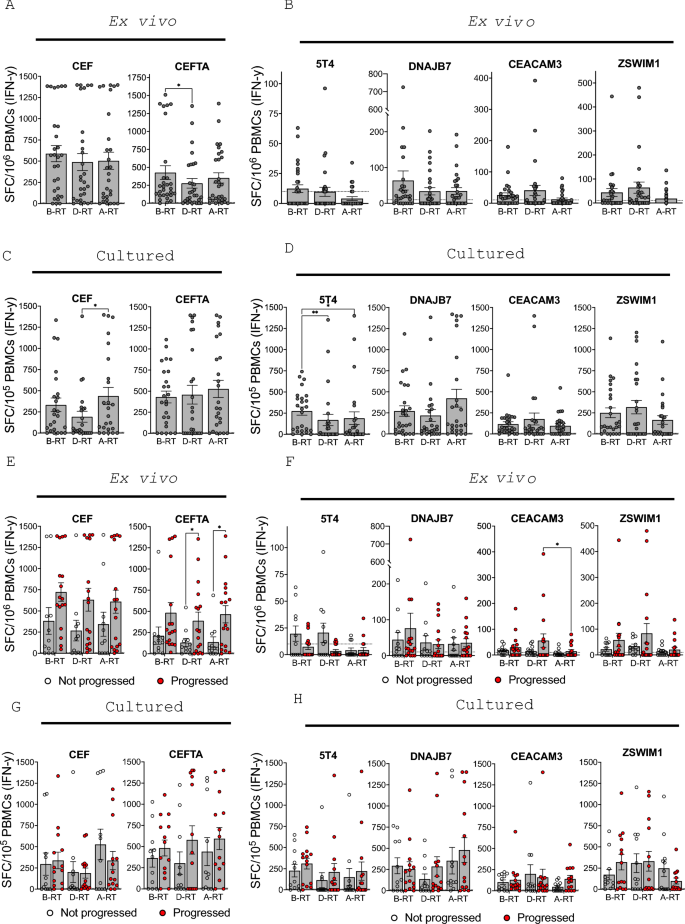
结果解读:离体酶联免疫斑点试验结果显示,立体定向消融放疗后CD4+T细胞对CEFTA肽池的应答较基线显著降低(n=28,P=0.0213),对5T4的应答也出现降低,提示效应T细胞功能整体受到抑制;而培养酶联免疫斑点试验结果显示,记忆T细胞对病毒抗原的应答在治疗后显著升高,对多数肿瘤相关抗原的应答无显著变化,仅5T4特异性记忆应答降低,提示立体定向消融放疗主要影响效应T细胞功能,对记忆T细胞的影响较小。进展患者与非进展患者的T细胞应答无显著差异,仅进展患者治疗后对癌胚抗原相关细胞黏附分子3的离体应答显著降低。
实验所用关键产品:Mabtech的干扰素-γ酶联免疫斑点试剂盒(货号3420-2A)、Millipore的96孔聚偏二氟乙烯滤膜板(货号MAIPS4510)、Mabtech的CEF肽池(货号3616-1)、CEFTA肽池(货号3617-1)、GLBiochem的肿瘤相关抗原重叠肽池。
3.4 免疫特征与临床预后的关联分析
实验目的:鉴定立体定向消融放疗诱导的免疫变化、放疗参数与患者无进展生存期的关联,筛选可预测预后的免疫标志物。
方法细节:采用Spearman秩相关分析免疫指标、放疗参数(生物有效剂量、计划靶体积)与患者预后的相关性;采用Kaplan-Meier曲线分析不同免疫特征、放疗参数患者的无进展生存期差异,采用对数秩检验比较组间差异。
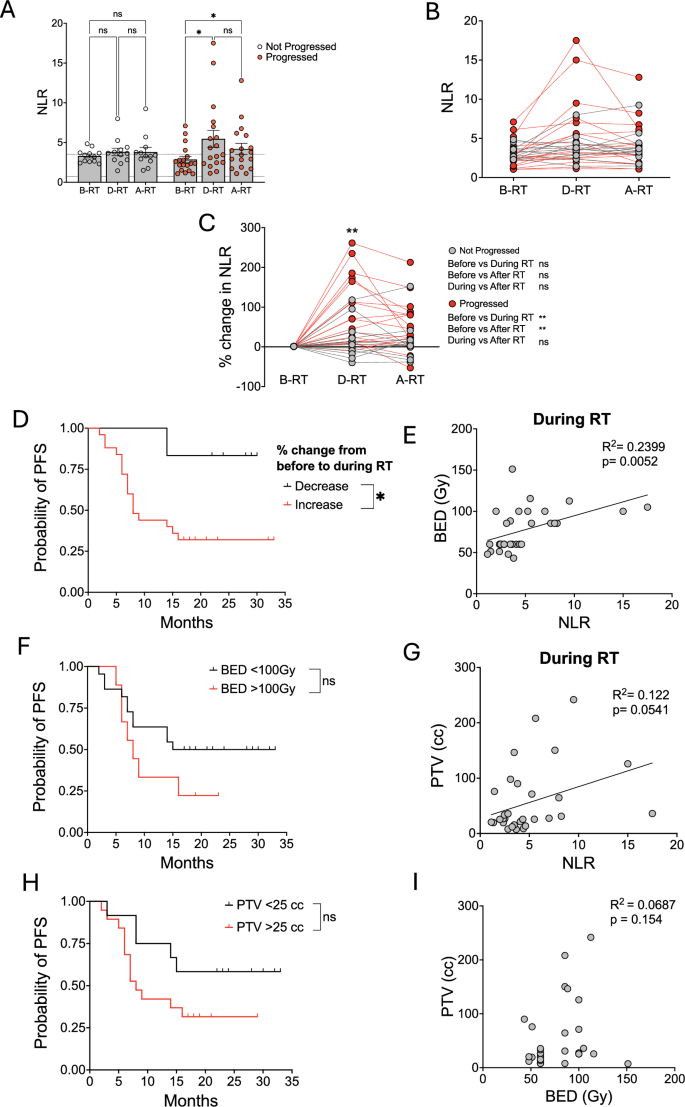
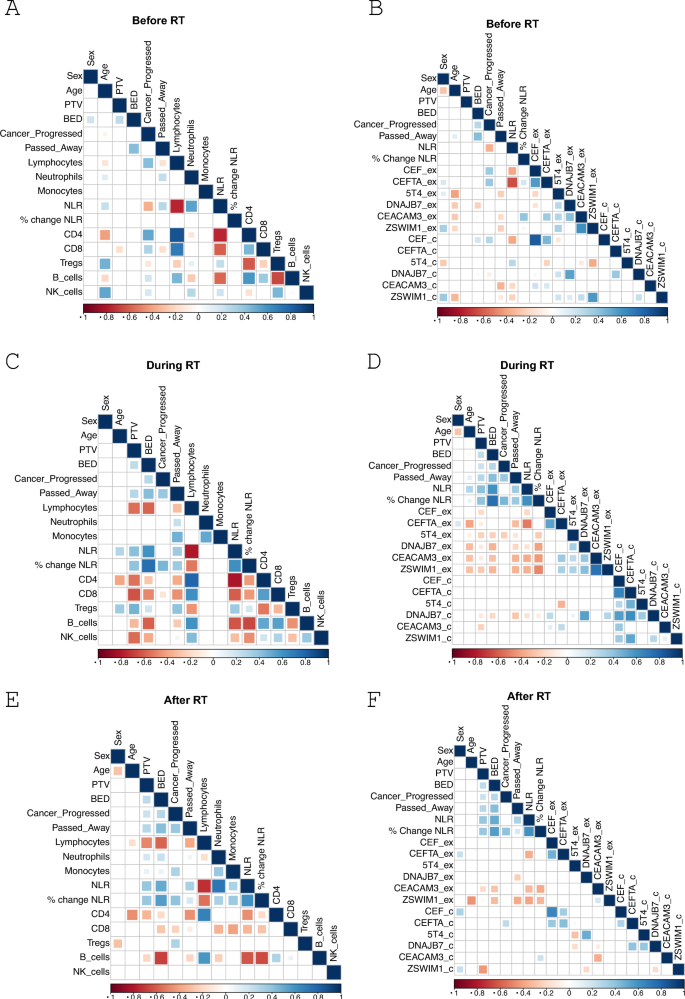
结果解读:基线中性粒细胞淋巴细胞比在进展患者与非进展患者中无显著差异,而治疗期间中性粒细胞淋巴细胞比升高的患者无进展生存期显著短于降低的患者(n=30,P=0.0328)。更高的生物有效剂量(≥100Gy)和更大的计划靶体积(≥25cc)均与治疗期间中性粒细胞淋巴细胞比升高相关(生物有效剂量与中性粒细胞淋巴细胞比的相关性n=30,P=0.0052),且存在更差的无进展生存期趋势,其中计划靶体积≥25cc的患者中位无进展生存期为8个月,而<25cc的患者中位无进展生存期未达到。多因素相关性分析显示,中性粒细胞淋巴细胞比升高、生物有效剂量和计划靶体积增大均与淋巴细胞减少、效应T细胞功能降低、调节性T细胞比例升高相关,共同驱动患者不良预后。
实验所用关键产品:文献未提及统计分析以外的实验产品,领域常规使用GraphPad Prism、R软件进行统计分析与可视化。
4. Biomarker研究及发现成果
本研究鉴定的核心生物标志物为立体定向消融放疗治疗期间中性粒细胞淋巴细胞比的动态变化,属于血液学炎症类生物标志物,可直接反映放疗诱导的免疫抑制程度,预测患者无进展生存期。
该生物标志物的筛选与验证遵循“全血细胞计数动态检测→中性粒细胞淋巴细胞比变化与免疫细胞亚群的关联验证→中性粒细胞淋巴细胞比变化与预后的关联验证→放疗参数与中性粒细胞淋巴细胞比的关联分析”的完整逻辑链条。其检测样本为患者外周全血,验证方法为临床常规全血细胞计数后直接计算中性粒细胞与淋巴细胞的比值,无需额外复杂检测。统计学分析显示,治疗期间中性粒细胞淋巴细胞比升高的患者无进展生存期显著更差(n=30,P=0.0328);其升高与更高的生物有效剂量呈正相关(n=30,P=0.0052),与淋巴细胞计数的降低呈显著负相关(n=30,P=0.0006),排除了中性粒细胞升高的干扰,特异性较高。文献未明确提供该生物标志物的敏感性、特异性及受试者工作特征曲线下面积数据,其预测效能需在更大样本量的单病种队列中进一步验证。
该生物标志物的功能关联为可直接反映立体定向消融放疗诱导的淋巴细胞减少及全身免疫抑制程度,治疗后中性粒细胞淋巴细胞比升高提示患者无进展生存期更差,该关联在接受肝脏病灶立体定向消融放疗的患者中更为显著。其创新性在于首次明确立体定向消融放疗治疗期间中性粒细胞淋巴细胞比的动态变化而非基线值是预后预测标志物,证实其升高完全由淋巴细胞减少驱动,而非炎症诱导的中性粒细胞升高,为临床快速评估患者预后提供了便捷的检测指标。
推测:后续可通过优化放疗计划减少循环淋巴细胞的照射剂量,或联合白细胞介素-7等淋巴细胞生长因子、低剂量免疫激动剂缓解放疗诱导的免疫抑制,进一步改善接受立体定向消融放疗患者的预后。
