1. 领域背景与文献
文献英文标题:In vivo generation of functional CD19 CAR-T cells via fusogenic nanovesicles ameliorates experimental rheumatoid arthritis;发表期刊:Journal of Nanobiotechnology;影响因子:10.2(2024年);研究领域:自身免疫病免疫治疗(类风湿关节炎方向)。
类风湿关节炎是临床常见的慢性自身免疫病,领域共识:其核心发病机制为异常活化的B细胞通过分泌自身抗体、呈递抗原、释放促炎细胞因子,驱动关节滑膜持续炎症、软骨与骨结构破坏,最终导致患者残疾与沉重的社会经济负担。现有常规治疗方案包括非甾体抗炎药、糖皮质激素、改善病情抗风湿药,仅能缓解部分患者症状,约30%的患者无法实现持久缓解,长期治疗还存在免疫抑制相关的全身毒性风险。嵌合抗原受体(CAR)T细胞疗法近年在B细胞恶性肿瘤中实现突破性应用,也展现出自身免疫病治疗潜力,其中分化簇19(CD19)靶向的CAR-T细胞可精准耗竭致病B细胞,在难治性自身免疫病中已观察到显著的临床应答。但传统CAR-T疗法依赖体外细胞制备与病毒载体介导的基因修饰,存在制备周期长、成本高、可扩展性差的核心缺陷,新兴的体内CAR-T生成策略如慢病毒递送、脂质纳米粒mRNA递送,仍受限于插入突变风险、递送效率不足、系统复杂度高等问题,领域尚未形成安全、高效、可规模化的体内CAR-T制备技术用于自身免疫病治疗。本研究针对上述研究空白,开发靶向T细胞的融合纳米囊泡系统FuNVCAR,实现无需基因修饰的体内CAR-T细胞生成,为类风湿关节炎及其他B细胞驱动的自身免疫病提供新的治疗范式。
2. 文献综述解析
本研究文献综述部分按治疗技术迭代的分类维度展开评述,首先明确B细胞异常活化在类风湿关节炎发生发展中的核心作用,从致病机制层面论证B细胞作为治疗靶点的科学性与必要性。
作者梳理现有类风湿关节炎治疗方案的研究进展:现有研究支持常规免疫抑制与免疫调节药物可缓解部分患者的症状、减缓疾病进展,该类方案的技术优势为临床应用成熟、给药方式便捷,但局限性十分突出,约30%患者治疗应答不佳,长期使用会增加感染、脏器损伤等全身毒性风险,且无法针对致病机制实现持久的病因学干预。随后作者总结CAR-T疗法的发展现状,现有研究支持CD19靶向CAR-T可有效耗竭B细胞,在难治性自身免疫病中已观察到显著的临床与血清学应答,其技术优势为靶向性强,可实现致病免疫细胞的精准清除,但传统CAR-T的局限性同样明显,体外制备、病毒载体修饰的工艺复杂、成本高昂,可扩展性差,难以满足自身免疫病患者的大规模临床需求,新兴的体内CAR-T策略中,慢病毒递送存在插入突变的安全风险,脂质纳米粒mRNA递送存在翻译效率不稳定、体内靶向性不足的问题。
通过对比现有研究的未解决问题,本研究的创新价值得到凸显:研究首次开发基于膜融合的蛋白递送纳米囊泡系统,无需基因修饰即可在体内靶向生成功能性CAR-T细胞,既规避了病毒载体和基因编辑的安全风险,又大幅降低了制备成本、提升了可扩展性,弥补了现有CAR-T技术在自身免疫病应用场景中的核心缺陷。
3. 研究思路总结与详细解析
本研究的核心目标是开发可体内靶向生成CD19 CAR-T细胞的融合纳米囊泡系统,验证其对类风湿关节炎的治疗效果与安全性,核心科学问题是如何实现T细胞的精准靶向、高效递送CAR蛋白并保留CAR-T细胞的功能活性,技术路线遵循“系统构建→体外表征→功能验证→体内疗效评价→安全性评估”的闭环逻辑。

3.1 FuNVCAR纳米囊泡的构建与表征
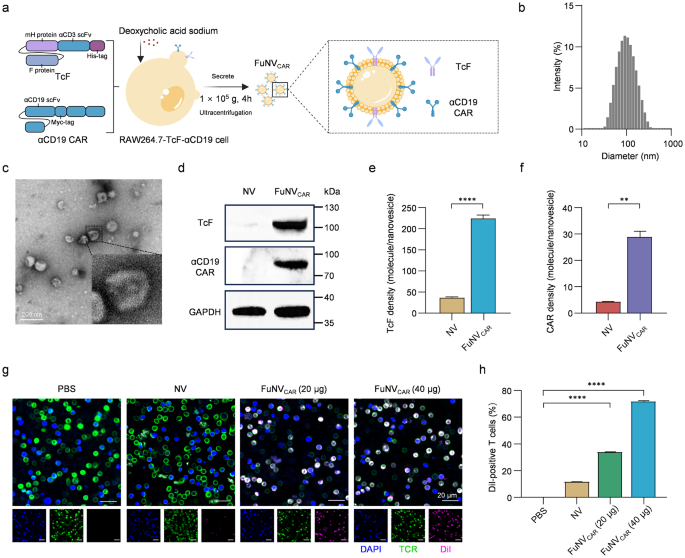
实验目的为构建靶向T细胞的融合纳米囊泡系统,验证其结构组成与递送功能的基础特性。方法细节:通过基因工程在RAW264.7细胞中共同表达CD3靶向的麻疹病毒融合蛋白(TcF)和带Myc标签的二代抗CD19 CAR,采用去污剂辅助膜囊泡化结合超速离心的方法制备FuNVCAR,对照纳米囊泡(NV)采用野生型RAW264.7细胞同法制备;采用动态光散射、透射电子显微镜、纳米颗粒跟踪分析、蛋白免疫印迹、酶联免疫吸附实验(ELISA)对囊泡的粒径、形貌、蛋白载量进行表征。结果解读:动态光散射结果显示FuNVCAR平均水合粒径为98.15±22.34nm,透射电镜图显示为均一的椭圆形囊泡,具有完整的双层膜结构;蛋白免疫印迹和ELISA结果证实每个囊泡平均装载222.88±7.32个TcF分子和28.16±3.12个CAR分子,无目标蛋白的NV对照组未检测到对应信号。实验所用关键产品:赛默飞世尔的BCA蛋白定量试剂盒、Myc标签ELISA检测试剂盒(美恩,上海)、His标签ELISA检测试剂盒(金斯瑞,美国)。
3.2 FuNVCAR的T细胞融合特异性与体外CAR-T生成效率验证
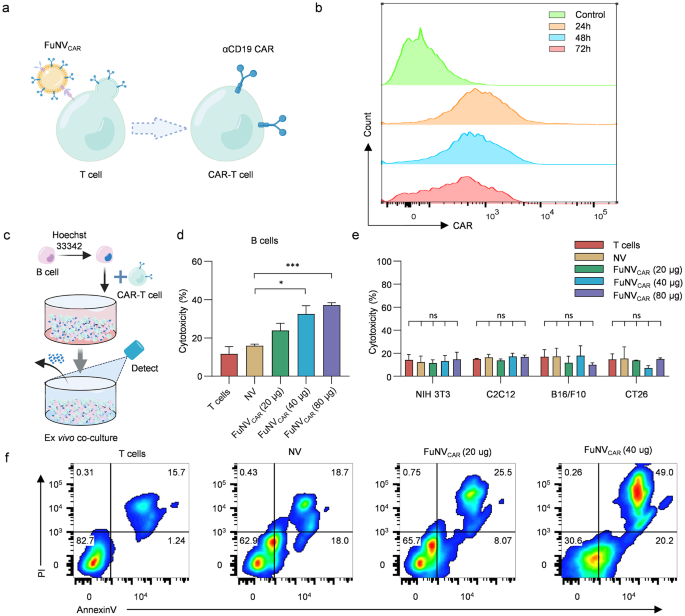
实验目的为验证FuNVCAR对T细胞的融合特异性,以及体外生成CD19 CAR-T细胞的效率与功能。方法细节:采用DiI标记FuNVCAR和对照NV,与原代小鼠T细胞或总脾细胞共孵育10h,通过共聚焦显微镜和流式细胞术检测融合效率与细胞类型选择性;将不同剂量FuNVCAR与T细胞共孵育后,在24、48、72h通过流式细胞术检测T细胞表面CAR的表达水平;采用Hoechst标记的CD19+B细胞和CD19-对照细胞系与CAR-T细胞共培养48h,检测细胞毒性,同时采用Annexin V/PI染色检测靶细胞凋亡水平。结果解读:共聚焦结果显示FuNVCAR可特异性与T细胞受体(TCR)阳性T细胞膜融合,流式结果显示融合效率呈剂量依赖性,40μg剂量下T细胞融合阳性率可达72.2%(n=5,P<0.0001),几乎不与B细胞、髓系细胞融合;CAR表达检测显示40μg剂量下24h CAR阳性T细胞比例可达44.7%(n=5,P<0.0001),72h仍可维持23.8%的阳性率;细胞毒性实验显示CAR-T细胞可剂量依赖性杀伤CD19+B细胞,40μg剂量下24h B细胞凋亡率可达49.0%(n=5,P<0.0001),对CD19-细胞无明显杀伤作用。实验所用关键产品:美天旎的小鼠Pan T细胞分离试剂盒、Biolegend的流式抗体、Elabscience的Annexin V/PI凋亡检测试剂盒。
3.3 体内CAR-T生成与B细胞耗竭效果验证
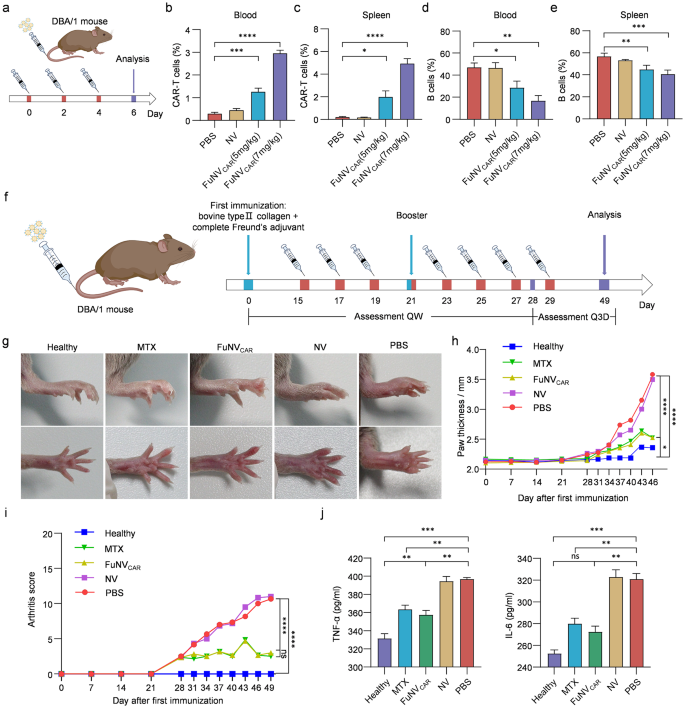
实验目的为验证FuNVCAR在体内生成CAR-T细胞、耗竭B细胞的能力。方法细节:采用DBA/1小鼠,分别静脉注射PBS、NV、5mg/kg和7mg/kg FuNVCAR,在第0、2、4天给药,第6天采集外周血和脾脏,通过流式细胞术检测CAR-T细胞比例和CD19+B细胞比例。结果解读:7mg/kg剂量下,外周血中CAR-T细胞占总T细胞的2.74%(n=5,P<0.001),B细胞比例较对照组降低28.1%(n=5,P<0.001);脾脏中CAR-T细胞占比达4.78%(n=5,P<0.0001),B细胞比例降低12.4%(n=5,P<0.01),呈现明确的剂量依赖性效应。
3.4 胶原诱导关节炎(CIA)模型的治疗效果评价
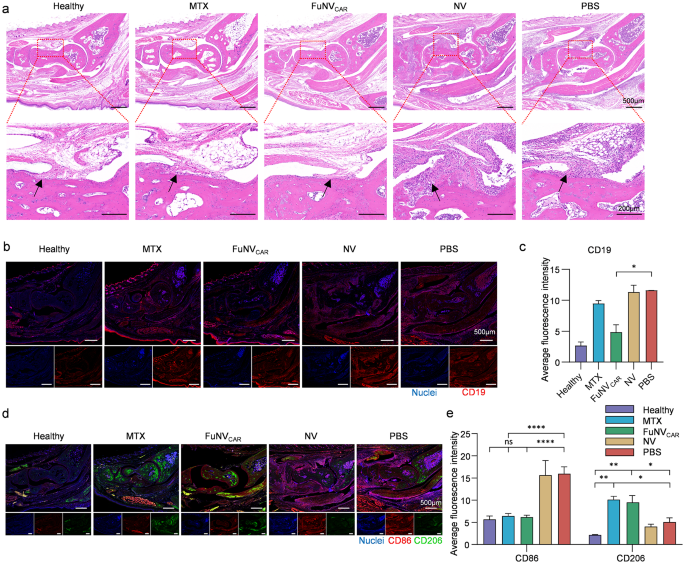
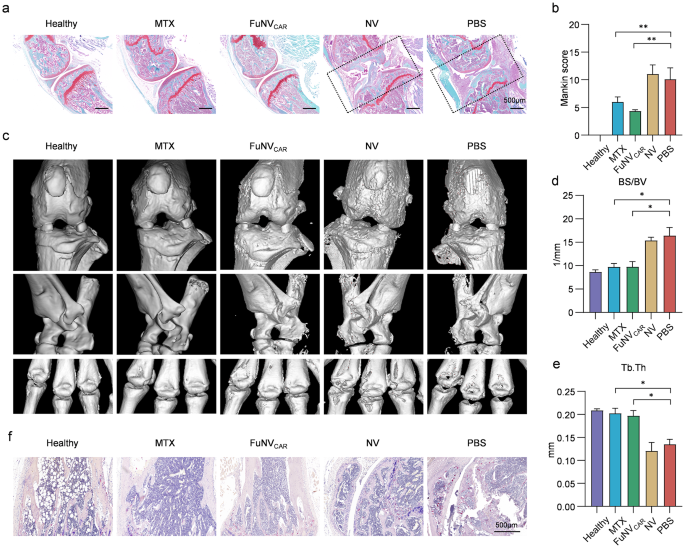
实验目的为验证FuNVCAR对类风湿关节炎模型的治疗效果。方法细节:采用DBA/1J小鼠构建CIA模型,分为健康组、甲氨蝶呤(MTX)组、7mg/kg FuNVCAR组、NV组、PBS组,每组8只,造模后第15天开始给药,FuNVCAR每2天给药1次共8次,MTX每周2次共4次;动态监测踝关节厚度、关节炎临床评分,给药结束后采集血清检测炎症因子水平,取关节组织进行苏木精-伊红(H&E)染色、免疫荧光染色、番红O/固绿染色、显微计算机断层扫描(micro-CT)检测,评估关节病理损伤、免疫细胞浸润、软骨和骨破坏情况。结果解读:FuNVCAR治疗可显著降低小鼠踝关节厚度和关节炎临床评分,疗效与MTX相当;血清肿瘤坏死因子-α(TNF-α)、白介素-6(IL-6)水平较PBS组显著降低(n=5,P<0.001);关节组织H&E染色显示炎症细胞浸润、滑膜增生显著减轻,CD19+B细胞浸润较对照组降低约70%(n=8,P<0.0001);番红O染色显示软骨蛋白多糖保留更完整,Mankin评分较PBS组降低62%(n=8,P<0.01);micro-CT结果显示骨表面/骨体积比(BS/BV)降低28%(n=8,P<0.01),骨小梁厚度(Tb.Th)增加22%(n=8,P<0.05),骨侵蚀显著减轻。实验所用关键产品:Chondrex的牛II型胶原、完全弗氏佐剂、抗II型胶原IgG ELISA试剂盒。
3.5 体内安全性与药代动力学评估
实验目的为评估FuNVCAR的体内安全性、免疫原性与药代动力学特征。方法细节:给药结束后采集小鼠心、肝、脾、肺、肾组织进行H&E染色,评估器官毒性;采用ELISA检测血清抗FuNVCAR IgG水平,评估免疫原性;在给药后不同时间点采集血清,检测FuNVCAR和MTX的血药浓度。结果解读:各主要器官未见明显病理损伤,较PBS组反而减轻了RA相关的脾红髓充血和肝炎症浸润;血清抗FuNVCAR IgG水平与对照组无显著差异(n=5,P>0.05),无明显免疫原性;药代动力学结果显示FuNVCAR体内清除较快,给药后第5天接近检测下限,无长期蓄积风险。文献未提及具体实验产品,领域常规使用病理染色相关试剂、ELISA试剂盒开展该类检测。
4. Biomarker研究及发现成果
本研究涉及的核心Biomarker包括CD19+B细胞、II型胶原特异性IgG、炎症因子TNF-α和IL-6,以及关节结构损伤相关标志物,用于评估治疗效果与疾病进展,筛选与验证逻辑为“血清学标志物检测→组织浸润标志物检测→结构损伤标志物验证”的完整链条。
本研究的Biomarker来源包括小鼠外周血血清、关节组织、脾脏组织,验证方法包括流式细胞术、ELISA、免疫荧光染色、组织病理染色、micro-CT成像。其中CD19+B细胞作为核心疗效标志物,在7mg/kg FuNVCAR治疗后,外周血B细胞耗竭率达28.1%(n=5,P<0.001),关节组织CD19+B细胞荧光强度降低72%(n=8,P<0.0001),与疾病活动度呈显著正相关;II型胶原特异性IgG作为RA核心致病自身抗体,治疗后水平较PBS组降低45%(n=5,P<0.001),降幅优于MTX组;炎症因子TNF-α和IL-6治疗后分别降低58%和52%(n=5,P<0.001),可反映全身炎症控制效果;关节结构标志物Mankin评分、BS/BV、Tb.Th的检测结果显示FuNVCAR可显著抑制软骨和骨破坏,与临床评分结果一致。
核心成果方面,本研究证实CD19+B细胞的体内靶向耗竭可有效缓解RA的炎症和结构损伤,FuNVCAR介导的CAR-T生成可作为调控B细胞水平的新型策略,所有检测指标均具有统计学显著性,为后续临床转化提供了明确的疗效评价Biomarker组合。推测:该融合纳米囊泡平台可通过更换CAR的靶点结构,拓展应用于其他B细胞驱动的自身免疫病以及B细胞恶性肿瘤的治疗,需进一步开展大动物实验验证其安全性与有效性。