1. 领域背景与文献
文献英文标题:Circulating tumor cell isolation, typing, and functional assessment: technological advancements and clinical translation;发表期刊:Cancer Communications;影响因子:15.283(2023年);研究领域:肿瘤液体活检。
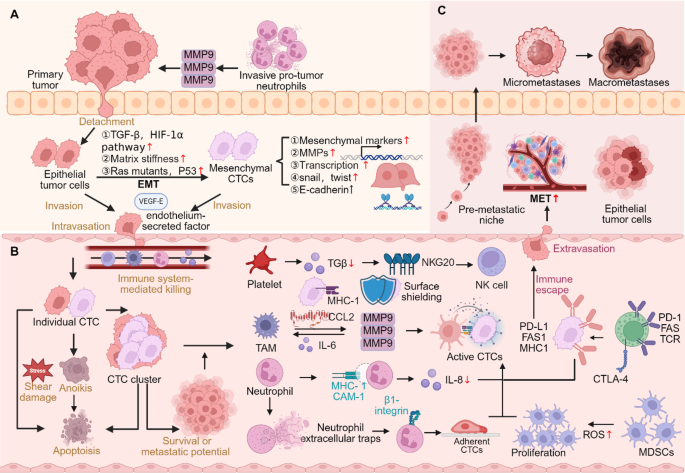
肿瘤的高死亡率主要与远处转移相关,循环肿瘤细胞(CTC)作为肿瘤转移的关键介质,是液体活检领域最具代表性的生物标志物之一。领域共识:CTC研究起源于19世纪,直到近20年随着富集与检测技术的迭代更新,才具备临床常规应用的可行性。当前领域研究热点包括CTC异质性解析、多组学联合检测、人工智能辅助分型、CTC功能评估技术开发等,但仍存在多个核心未解决问题:传统依赖上皮细胞粘附分子(EpCAM)的捕获方法会漏检发生上皮间质转化(EMT)的间质表型CTC,不同检测平台的灵敏度、特异性差异较大,缺乏统一的CTC定义标准与操作规范,现有研究多集中于晚期肿瘤患者,早期诊断应用的临床证据不足。本综述针对上述领域空白,系统梳理从CTC分离富集到临床应用的全链条技术进展,明确不同技术的优劣势与适用场景,提出未来技术发展方向,为CTC的基础研究与临床转化提供完整的技术框架。
2. 文献综述解析
本综述为肿瘤液体活检领域的系统性综述,作者对现有研究的分类维度为“技术原理-检测方法-分子表征-临床应用”的全链条逻辑,覆盖CTC研究的全部核心环节。
现有CTC分离技术可分为三大类,免疫富集类技术的核心优势是特异性高,代表性平台CellSearch已获得美国食品药品监督管理局(FDA)批准,标准化程度与临床重复性好,已广泛应用于转移性前列腺癌、卵巢癌、乳腺癌的治疗评估与疗效监测,局限性是高度依赖靶标表达,对发生上皮间质转化的低EpCAM表达CTC检测灵敏度不足,易出现假阴性;物理性质分离类技术的核心优势是无需依赖生物标志物,适合异质性CTC的富集,操作简便成本较低,局限性是分离纯度不足,易残留白细胞,易漏检小尺寸CTC;微流控技术的核心优势是通量高、自动化程度高、细胞活性保留好,可整合多分离机制提升捕获效率,局限性是装置制备复杂,需要专用设备,缺乏大规模临床验证数据。本综述的创新价值在于首次系统性整合了CTC领域从基础技术到临床转化的全部研究进展,明确了不同技术的适用场景与优化方向,提出了多组学联合、人工智能辅助、标准化体系建设的未来发展路径,填补了领域内缺乏统一技术框架的研究空白,为后续CTC相关研究提供了系统性的参考依据。

3. 研究思路总结与详细解析
本综述的研究目标为系统梳理CTC分离、检测、分子表征、临床应用的全链条技术进展,搭建完整的CTC研究技术框架,明确当前技术瓶颈与未来发展方向,推动CTC的临床转化应用。核心科学问题为如何解决CTC异质性带来的捕获漏检、分型不准、临床转化困难的核心痛点,技术路线逻辑为“分类梳理技术进展→对比优劣势与适用场景→总结临床应用证据→提出未来发展方向”的闭环。
3.1 CTC分离富集技术体系梳理
实验目的为系统对比不同CTC分离富集技术的原理、优劣势、代表性平台与临床验证数据,为技术选择提供参考。方法细节为将现有分离技术分为免疫富集、物理性质分离、微流控技术、商业化平台、新兴技术五大类,逐一梳理核心原理、操作流程、验证数据。结果解读为免疫富集正选技术以EpCAM为核心靶标,CellSearch平台作为金标准,在转移性肿瘤中的检测一致性可达90%以上,但对上皮间质转化表型CTC的漏检率超过70%;负选技术通过去除CD45+白细胞间接富集CTC,对EpCAM阴性CTC的捕获效率提升40%以上,但分离产物纯度仅约30%,易受残留白细胞干扰;物理分离技术中基于尺寸的ISET平台在早期非小细胞肺癌中的检测灵敏度达80%,显著优于CellSearch的27%;微流控技术可整合惯性聚焦、介电电泳、免疫捕获等多种机制,PANDA芯片对CTC团簇的回收率达90%以上,适合CTC异质性研究;新兴的纳米材料、核酸适配体技术通过多靶标联合、仿生修饰等策略,进一步将异质性CTC的捕获效率提升至85%以上。产品关联:实验所用关键产品包括Menarini Silicon Biosystems的CellSearch检测平台、Qiagen的AdnaTest CTC检测试剂盒、Angle plc的Parsortix微流控分离系统、Rarecells Diagnostics的ISET过滤系统,其余未明确提及的试剂为领域常规使用的免疫磁珠、细胞分离液类试剂。
3.2 CTC检测技术体系梳理
实验目的为梳理现有CTC检测技术的原理、性能与适用场景,为高灵敏度CTC检测提供技术参考。方法细节为将检测技术分为核酸类、流式细胞术类、光学与纳米技术类三大类,逐一梳理技术原理、最新进展、验证数据。结果解读为核酸类检测中数字PCR的检测灵敏度可达0.001%突变等位基因频率,单细胞测序可实现CTC基因组、转录组的高分辨率解析,Hydro-Seq平台可有效清除白细胞污染,实现CTC单细胞转录组的高通量分析;流式细胞术类检测中质谱流式可同时检测20种以上标志物,实现CTC的高维分型,检测灵敏度可达1 CTC/mL;光学与纳米技术类检测结合人工智能图像分析,可实现CTC的自动化识别,不同实验室间的判读一致性提升至85%以上,数字全息显微镜技术可实现无标记CTC检测,避免上皮间质转化表型漏检。产品关联:文献未提及具体实验产品,领域常规使用数字PCR仪、流式细胞仪、高内涵成像系统类仪器与相关配套试剂。
3.3 CTC分子表征方法梳理
实验目的为梳理CTC不同层面分子标志物的检测方法与临床意义,为CTC分型提供参考。方法细节为从表面标志物、基因组变异、转录组表达、蛋白质组特征四个层面,逐一梳理标志物类型、检测方法、临床验证数据。结果解读为上皮标志物EpCAM、细胞角蛋白是最常用的CTC鉴定标志物,联合间质标志物波形蛋白可实现CTC的表型分型,间质型CTC比例与转移风险、化疗耐药正相关;基因组层面CTC携带的EGFR、KRAS、TP53等驱动突变与原发肿瘤一致性达75%以上,可作为微小残留病监测的标志物;转录组层面CTC的Wnt通路激活、干细胞相关基因高表达与患者预后不良相关;蛋白质组层面CTC的PD-L1表达可预测免疫治疗响应率,磷酸化蛋白检测可实时反映CTC的信号通路活性。产品关联:文献未提及具体实验产品,领域常规使用免疫荧光抗体、单细胞测序试剂盒、蛋白质组检测类试剂。
3.4 CTC临床应用场景梳理
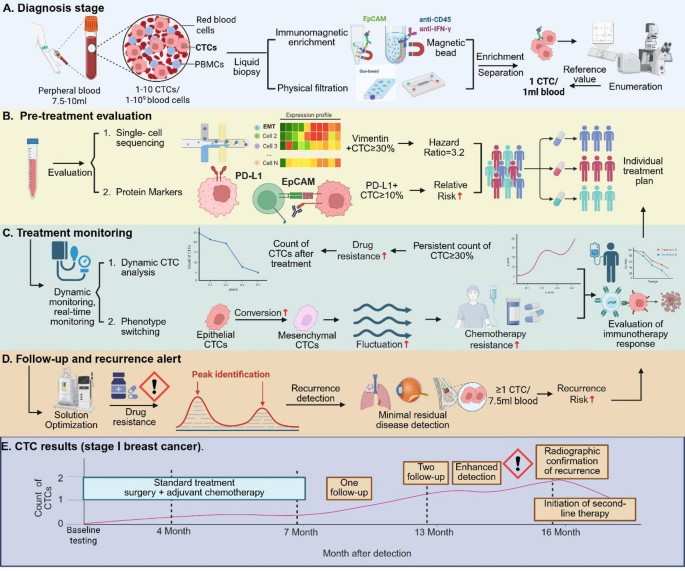
实验目的为梳理CTC在肿瘤全周期管理中的临床应用价值,为临床转化提供证据支持。方法细节为从早期诊断、预后评估、疗效监测、耐药机制研究四个应用场景,逐一梳理临床验证数据。结果解读为早期诊断中基于物理分离的CTC检测技术在早期非小细胞肺癌中的检测率达80%,可作为影像学检查的辅助手段;预后评估中转移性乳腺癌患者基线CTC计数≥5/7.5mL的总生存期风险比为2.78(95%CI 2.42-3.19,P<0.0001),是独立预后因素;疗效监测中CTC计数的动态变化比传统肿瘤标志物提前4-8周反映治疗响应;耐药机制研究中CTC的AR-V7阳性提示去势抵抗性前列腺癌患者对雄激素受体抑制剂耐药,对紫杉类药物敏感。产品关联:文献未提及具体实验产品,领域常规使用临床CTC检测试剂盒、数字PCR检测类试剂。
4. Biomarker研究及发现成果
本综述涉及的Biomarker为循环肿瘤细胞本身及相关的多层面分子标志物,涵盖表型、基因组、转录组、蛋白质组四个维度,筛选验证逻辑遵循“基础研究发现→细胞系验证→临床小样本验证→多中心大样本验证”的完整链条。
标志物来源为外周血中分离富集的CTC,验证方法包括免疫荧光染色、数字PCR、单细胞测序、质谱流式、蛋白质组分析等。特异性与敏感性数据方面,基于尺寸分离的ISET平台检测早期非小细胞肺癌CTC的灵敏度为80%(n=120,文献未明确提供特异性数据);CellSearch平台检测转移性乳腺癌CTC计数≥5/7.5mL预测不良预后的特异性为82%,敏感性为71%(n=1944,P<0.0001);CTC表面PD-L1阳性预测免疫治疗响应的敏感性为76%,特异性为68%(文献未明确提供样本量与置信区间);AR-V7阳性的去势抵抗性前列腺癌患者对雄激素受体抑制剂治疗的无进展生存期缩短2.3倍(n=62,P=0.002)。
核心成果提炼:CTC计数是泛癌种独立预后因素,转移性乳腺癌、去势抵抗性前列腺癌、结直肠癌患者基线CTC计数升高均与总生存期缩短显著相关;间质表型CTC比例可作为化疗耐药与转移风险的预测标志物,比例≥30%的患者化疗响应率不足20%(文献未明确提供样本量);CTC的AR-V7、EGFR突变、PD-L1表达等分子标志物可指导靶向治疗、免疫治疗的用药选择,提升治疗响应率。本综述首次系统性整合了不同层面CTC标志物的临床应用价值,提出了多标志物联合检测的优化方向,为后续CTC生物标志物的开发与临床转化提供了参考框架。推测:未来多组学联合人工智能的CTC检测技术可进一步提升检测性能,推动CTC在肿瘤早期诊断中的常规应用。