1. 领域背景与文献
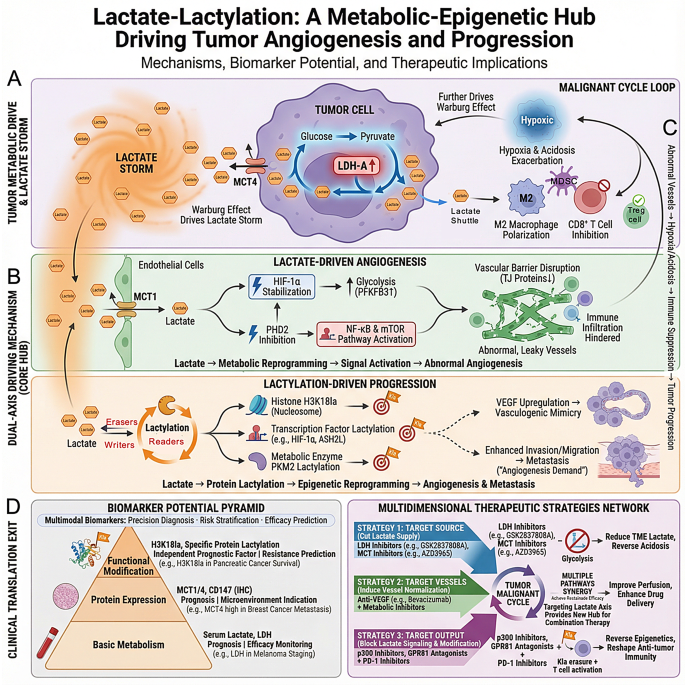
文献英文标题:Targeting lactate metabolism and lactylation for tumor vascular normalization and cancer immunotherapy;发表期刊:Molecular Cancer;影响因子:37.3(2023版);研究领域:肿瘤代谢调控与肿瘤血管靶向治疗。
领域共识:实体瘤生长超过1~2mm³后必须依赖新生血管获取营养和氧气,血管生成是肿瘤发生、发展、转移的核心生物学过程。血管内皮生长因子(VEGF)通路是目前抗血管生成治疗的核心靶点,但临床应用中普遍存在疗效短暂、易耐药、加重肿瘤免疫抑制等未解决的问题,严重限制了患者的生存获益。20世纪20年代瓦博格效应的发现揭示了肿瘤代谢重编程的核心特征,即肿瘤细胞即使在有氧条件下也优先通过糖酵解代谢葡萄糖,生成大量乳酸,过去乳酸被认为是无功能的代谢废物,2019年赖氨酸乳酸化修饰的首次发现,搭建了代谢微环境与表观遗传调控之间的桥梁,成为近年肿瘤领域的研究热点。
当前领域尚未明确的核心问题包括:乳酸对肿瘤血管生成的双向调控机制及阈值条件不清晰,乳酸化修饰的调控网络、组织特异性和功能异质性尚未阐明,缺乏靶向乳酸通路的高特异性药物和精准生物标志物,无法有效指导临床转化应用。本综述系统梳理了乳酸代谢及乳酸化修饰在肿瘤血管生成、免疫抑制、治疗抵抗中的多维度调控作用,提出了多通路联合治疗策略,为克服抗血管生成治疗耐药、提升实体瘤治疗效果提供了新的研究框架。
2. 文献综述解析
本综述的核心评述逻辑为“从生理机制到病理功能,从基础发现到临床转化”,按照乳酸稳态调控、乳酸对血管的直接调控、乳酸通过免疫微环境的间接调控、乳酸化的表观遗传调控、生物标志物潜力、靶向治疗策略、现存挑战的时间线和逻辑层次展开,覆盖了领域内近30年的核心研究成果。
现有研究的关键支持结论包括:一是肿瘤微环境中乳酸通过单羧酸转运体1/4(MCT1/4)形成四种穿梭模式,介导肿瘤细胞、基质细胞、免疫细胞之间的代谢互作和信号交流;二是乳酸可通过抑制脯氨酰羟化酶2(PHD2)稳定缺氧诱导因子-1α(HIF-1α),直接诱导内皮细胞糖代谢重编程,促进血管生成;三是乳酸可重塑肿瘤免疫微环境,诱导免疫抑制表型,间接驱动异常血管生成;四是赖氨酸乳酸化修饰可通过调控基因表达和蛋白功能,参与肿瘤血管生成、转移和治疗抵抗的全过程。现有技术的核心优势为:修饰蛋白质组学技术可实现乳酸化位点的高通量鉴定,多种靶向乳酸代谢通路的小分子抑制剂已进入临床前或临床研究阶段,为机制验证和转化应用提供了支撑。
现有研究的局限性包括:一是乳酸对血管生成的双向调控的浓度阈值、pH依赖机制尚未明确,不同研究的结论存在差异;二是乳酸化的写入器、擦除器、阅读器的底物特异性、组织异质性研究不足,调控网络尚未完全阐明;三是多数体外研究采用超生理浓度的乳酸处理模型,结论的生理相关性有待验证;四是缺乏特异性靶向乳酸化的小分子药物,临床转化的证据链尚不完善。
本综述的创新价值在于,首次系统整合了乳酸代谢、乳酸化修饰在肿瘤血管生成、免疫抑制、治疗抵抗中的交叉调控网络,提出了“代谢干预-免疫重塑-血管正常化”的三联治疗策略,明确了乳酸及相关分子作为诊断、预后、疗效预测生物标志物的应用潜力,为后续基础研究和临床转化提供了清晰的指导框架,填补了领域内缺乏系统性整合综述的空白。
3. 研究思路总结与详细解析
本综述的核心研究目标为系统阐明乳酸代谢及乳酸化修饰调控肿瘤血管生成的分子机制,挖掘潜在的生物标志物和治疗靶点,为克服抗血管生成治疗耐药提供新的解决方案。核心科学问题包括乳酸稳态调控的分子网络、乳酸调控血管生成的双向机制、乳酸化修饰的病理功能、靶向乳酸通路的转化策略四个方面,技术路线遵循“机制梳理→功能验证→标志物挖掘→治疗策略构建”的闭环逻辑。
3.1 肿瘤微环境乳酸稳态调控机制解析
实验目的:明确肿瘤微环境中乳酸生成、转运、穿梭的核心调控机制。
方法细节:梳理1926年瓦博格效应发现以来的核心研究成果,整合细胞代谢实验、同位素示踪实验、动物肿瘤模型、临床样本相关性分析的多维度证据。
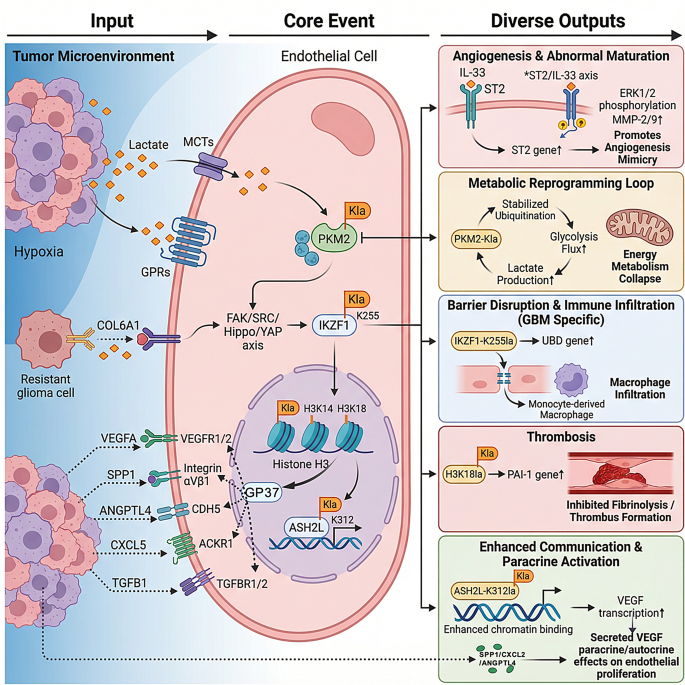
结果解读:肿瘤细胞通过瓦博格效应大量生成乳酸,由MCT4转运到胞外,氧化型细胞包括肿瘤相关内皮细胞、氧化表型肿瘤细胞通过MCT1摄取乳酸作为三羧酸循环的代谢底物,形成四种核心乳酸穿梭模式:一是肿瘤细胞间的代谢共生,缺氧区肿瘤细胞分泌乳酸,常氧区肿瘤细胞摄取利用;二是肿瘤与癌相关成纤维细胞之间的反向瓦博格效应,成纤维细胞分泌乳酸供肿瘤细胞利用;三是乳酸与内皮细胞的穿梭,乳酸通过调控HIF-1α通路促进血管生成;四是乳酸与免疫细胞的穿梭,乳酸塑造免疫抑制微环境。同时明确了D-乳酸的独特来源,包括肠道菌群代谢、细胞内甲基乙二醛通路,以及其独特功能,如诱导肿瘤细胞铁死亡、促进巨噬细胞向M1型极化。对应机制如图1所示:
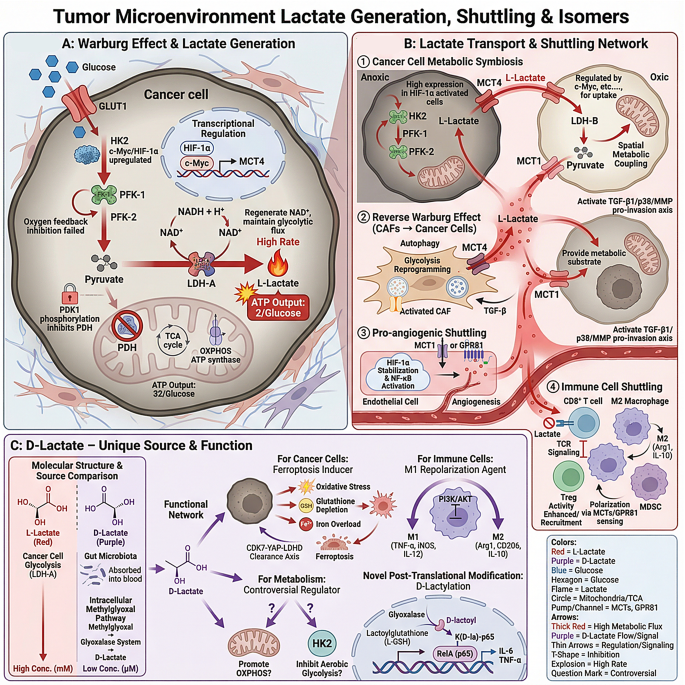
产品关联:文献未提及具体实验产品,领域常规使用糖酵解通量检测试剂盒、乳酸浓度检测试剂盒、MCT1/4特异性抗体等试剂。
3.2 乳酸对肿瘤血管生成的直接与间接调控作用解析
实验目的:阐明乳酸调控肿瘤血管生成的多维度机制,明确其双向调控的阈值条件。
方法细节:整合内皮细胞功能实验包括增殖、迁移、成管实验、免疫细胞极化检测、动物肿瘤模型、临床样本验证的相关研究证据。
结果解读:直接调控方面,乳酸可通过抑制PHD2稳定HIF-1α,诱导内皮细胞从氧化磷酸化向糖酵解的代谢重编程,形成“乳酸-HIF-1α-糖酵解”的正反馈环路,促进内皮细胞增殖、迁移和新生血管生成,同时乳酸可诱导内皮间质转化,下调紧密连接蛋白表达,破坏血管屏障完整性,促进肿瘤转移。乳酸对血管生成存在双向调控作用,中等乳酸浓度<30mM、pH>6.8时为促血管生成窗口,高乳酸浓度>20mM、pH<6.8时为抑制窗口,内皮细胞的碳酸酐酶II介导的pH缓冲是维持促血管功能的关键,相关调控网络如图2所示:

间接调控方面,乳酸可通过激活G蛋白偶联受体相关通路,促进肿瘤相关巨噬细胞向M2型极化、激活髓源性抑制细胞、增强调节性T细胞的免疫抑制功能、抑制CD8+T细胞和自然杀伤细胞的杀伤功能,形成免疫抑制微环境,免疫抑制细胞分泌大量VEGF、基质金属蛋白酶9(MMP9)等促血管生成因子,进一步驱动血管异常生成,形成“乳酸-免疫抑制-血管生成”的正反馈环路,相关机制如图3所示:

双向调控的阈值模型如图4所示:
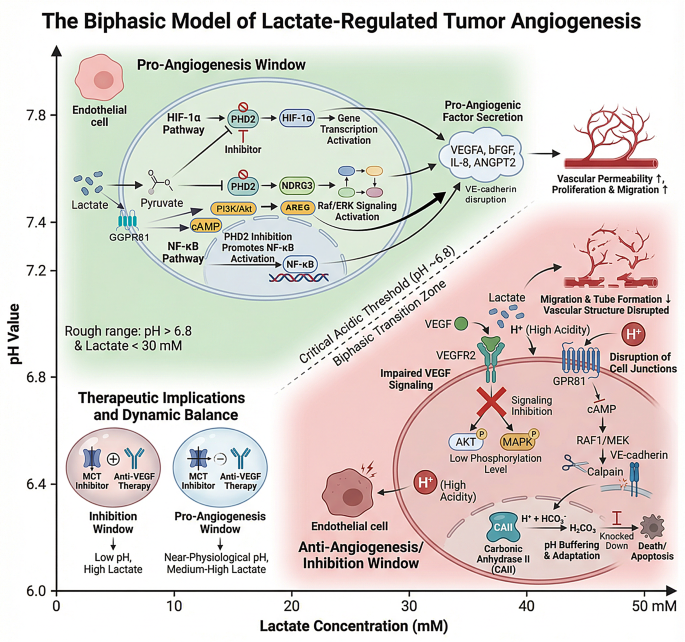
产品关联:文献未提及具体实验产品,领域常规使用内皮细胞成管实验试剂盒、免疫细胞极化检测试剂、流式细胞术检测试剂盒等。
3.3 乳酸化修饰的调控网络及病理功能解析
实验目的:明确赖氨酸乳酸化修饰的调控体系及在肿瘤血管生成、免疫抑制、治疗抵抗中的病理功能。
方法细节:整合修饰蛋白质组学检测、基因编辑技术、功能验证实验、临床样本相关性分析的研究证据。
结果解读:乳酸化修饰是动态可逆的表观遗传调控机制,由三类分子调控:写入器包括p300/CBP、AARS1/2、KAT家族,负责催化乳酸基团结合到赖氨酸残基;擦除器包括HDAC1~3、Sirtuin1~3,负责移除乳酸化修饰;阅读器包括DPF2等,负责识别乳酸化修饰并介导下游功能。乳酸化可发生在组蛋白和非组蛋白上,组蛋白乳酸化可通过调控下游基因转录,促进血管生成、肿瘤转移、免疫抑制;非组蛋白乳酸化可通过调控蛋白功能,促进DNA损伤修复、介导治疗抵抗。肿瘤相关内皮细胞中的乳酸化修饰可作为内皮功能状态的标志物,提示血管生成活性、代谢紊乱程度、屏障功能异常。乳酸化的调控体系如图5所示:

乳酸化调控肿瘤血管生成的具体机制如图6所示:
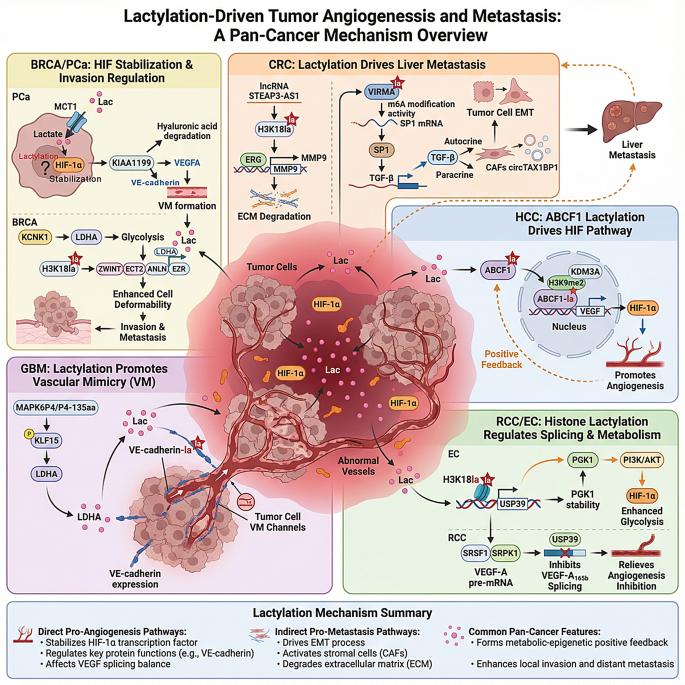
乳酸化介导内皮细胞功能转化的机制如图7所示:
产品关联:文献未提及具体实验产品,领域常规使用赖氨酸乳酸化泛抗体、位点特异性乳酸化抗体、修饰蛋白质组学检测服务等。
3.4 靶向乳酸通路的治疗策略解析
实验目的:梳理靶向乳酸代谢及乳酸化的治疗策略,构建联合治疗方案。
方法细节:整合临床前药物研究、临床试验结果的相关证据,分析不同联用方案的协同机制。
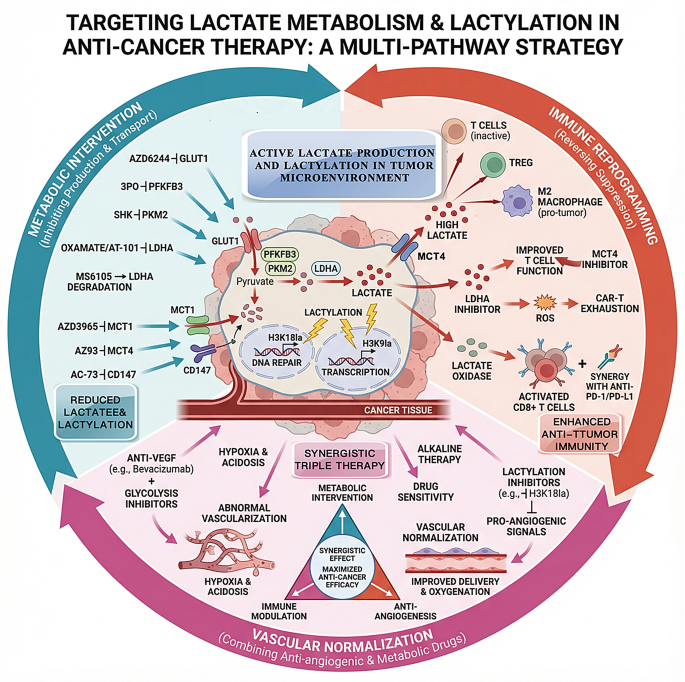
结果解读:靶向策略分为三类:一是靶向乳酸代谢酶,抑制葡萄糖转运体1(GLUT1)、PFKFB3、PKM2、乳酸脱氢酶A(LDHA)可减少乳酸生成,相关抑制剂如AT-101、FX-11已进入临床研究阶段;二是靶向乳酸转运体,抑制MCT1/4如AZD3965、AZ93或其伴侣蛋白CD147可阻断乳酸穿梭,已在多种肿瘤模型中显示抗肿瘤疗效;三是靶向乳酸化修饰,抑制写入器酶、激活擦除器酶、靶向特异性乳酸化位点可阻断乳酸化的病理作用,相关小分子如C646、王浆酸已在临床前模型中验证疗效。联合策略方面,靶向乳酸通路可与免疫检查点抑制剂、抗血管生成药物联用,通过重塑免疫微环境、促进血管正常化,增强治疗效果,克服耐药,多维治疗策略的框架如图9所示:
产品关联:文献未提及具体实验产品,领域常规使用上述通路的小分子抑制剂、抗体类药物等。
4. Biomarker 研究及发现成果
本综述涉及的生物标志物包括代谢类、蛋白类、修饰类三种类型,筛选验证逻辑为“分子功能相关性验证→大样本临床队列验证→预后/疗效预测价值评估”,覆盖诊断、预后、疗效预测全流程应用场景。
研究过程详述:一是循环乳酸及代谢组panel,血清乳酸水平、乳酸/丙酮酸比值、包含乳酸、丙酮酸、柠檬酸、葡萄糖的4代谢物panel可用于肿瘤辅助诊断,其中4代谢物panel在胰腺癌中的诊断曲线下面积(AUC)为0.956(文献未明确提供样本量),治疗前血清乳酸升高与多种实体瘤总生存期缩短显著相关;二是乳酸脱氢酶LDH,血清LDH是已被纳入临床分期的预后标志物,黑色素瘤中高LDH患者总生存期风险比(HR)为1.97(95%置信区间1.62~2.40,P<0.001),动态监测LDH变化可预测治疗反应,治疗后LDH降至正常的晚期患者总生存期可从1.7个月延长至22.6个月;三是乳酸转运体MCT1/4,MCT4高表达与胰腺癌、乳腺癌、肝癌等多种实体瘤总生存期缩短显著相关,MCT1高表达是头颈部鳞癌放化疗后无进展生存期(HR=3.1,P<0.001)和总生存期(HR=3.8,P<0.001)的独立危险因素;四是乳酸化修饰,组蛋白H3K18乳酸化(H3K18la)是目前研究最充分的修饰标志物,胰腺导管腺癌中高H3K18la是总生存期(HR=2.297,P<0.001)和无病生存期的独立危险因素,非组蛋白乳酸化如ABCF1-K430la、ASH2L-K312la也可作为预后标志物,与肿瘤微血管密度、转移风险显著相关。相关生物标志物的转化应用框架如图8所示:
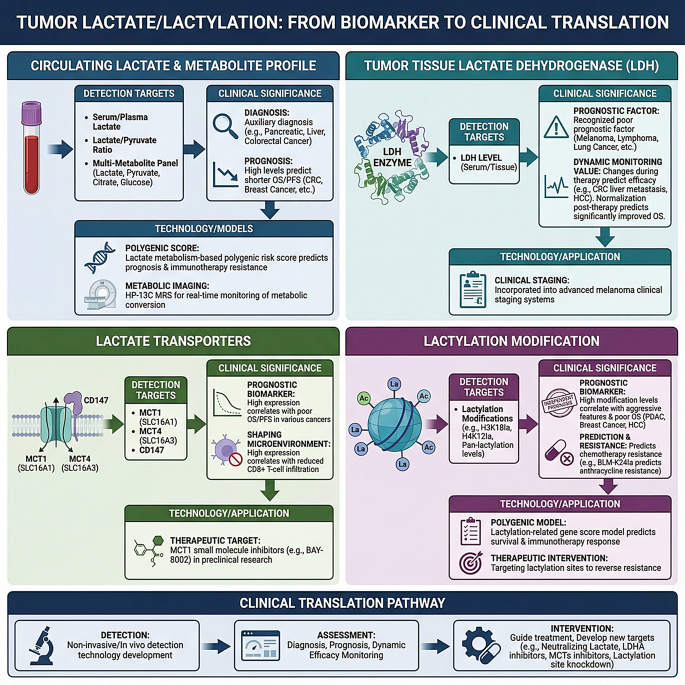
核心成果提炼:上述生物标志物可分别用于肿瘤辅助诊断、预后分层、疗效预测,其中乳酸化修饰作为功能型标志物,可同时提示肿瘤代谢状态、免疫抑制程度和血管生成活性,为精准分层治疗提供依据;部分标志物如H3K18la还可作为治疗响应预测标志物,指导靶向乳酸通路药物的使用。推测:未来基于乳酸、LDH、MCT1/4、乳酸化修饰的多标志物联合检测panel,可实现实体瘤患者的精准分层,最大化靶向乳酸通路治疗的临床获益。