1. 领域背景与文献引入
文献英文标题:Comprehensive proteomic characterization of solid pseudopapillary neoplasm reveals unique biology, diagnostic markers, and therapeutic targets;发表期刊:Journal of Experimental & Clinical Cancer Research;影响因子:未公开;研究领域:胰腺肿瘤学(胰腺实性假乳头状瘤蛋白质组学研究)
胰腺实性假乳头状瘤(SPN)是一类罕见的胰腺上皮性肿瘤,占所有胰腺肿瘤的1-2%,好发于年轻女性,多数表现为低级别恶性生物学行为,手术切除后预后良好,但仍有8-13%的病例会出现远处转移或复发。领域共识:基因组研究已明确SPN的核心驱动事件为CTNNB1体细胞突变及β-catenin核积累,与胰腺导管腺癌(PDAC)的KRAS、TP53等经典驱动突变谱存在显著差异;但β-catenin核积累并非SPN特异性标志物,在胰腺腺泡细胞癌、胰母细胞瘤等肿瘤中也可出现。当前领域存在的核心问题包括:SPN的蛋白质组学特征尚未被全面解析,早期蛋白质组学研究样本量极小(仅3例)且深度有限;SPN的代谢适应机制、肿瘤免疫微环境特征在蛋白层面的研究处于空白;缺乏特异性更高的诊断标志物,且无针对转移性或复发性SPN的靶向治疗方案。本研究针对上述研究空白,通过大样本深度蛋白质组学分析,系统对比SPN与PDAC、胰腺神经内分泌肿瘤(PanNET)及良性胰腺组织的蛋白表达差异,旨在揭示SPN的独特生物学特性、筛选特异性诊断标志物及潜在治疗靶点。
2. 文献综述解析
作者对领域内现有研究按技术维度分为基因组学、转录组学、蛋白质组学三类进行评述。基因组学研究的关键结论为SPN以CTNNB1突变和WNT/β-catenin通路激活为核心特征,与PDAC的驱动突变谱存在本质差异;技术优势在于明确了SPN的核心驱动事件,局限性为无法反映蛋白层面的功能变化及通路活性。转录组学研究发现SPN中Wnt/β-catenin、Hedgehog等通路激活,优势在于从转录水平揭示了部分通路特征,局限性为转录与蛋白表达的相关性较差,无法直接反映蛋白功能。早期蛋白质组学研究仅报道了糖酵解相关蛋白上调或内质网相关蛋白富集,优势为首次从蛋白层面探索SPN特征,局限性为样本量极小、蛋白检测深度不足,且未与其他胰腺肿瘤进行系统对比。
本研究的创新价值在于:首次开展大样本(13例SPN)的深度蛋白质组学分析,对比PDAC、PanNET及良性胰腺组织,弥补了早期研究样本量和深度的不足;发现MITF是比TFE3特异性更高的SPN诊断标志物,解决了现有诊断标志物特异性不足的问题;系统解析了SPN的代谢适应机制和免疫冷微环境特征,填补了领域内蛋白层面功能研究的空白;筛选出PDGFRA、ERBB2等潜在靶向治疗靶点,为转移性SPN的治疗提供了新方向。
3. 研究思路总结与详细解析
本研究的整体框架为:以临床样本为基础,通过深度蛋白质组学分析绘制SPN的蛋白表达谱,结合免疫组化验证、通路富集分析等手段,系统解析SPN与其他胰腺肿瘤的蛋白层面差异,明确其诊断标志物、代谢适应机制、免疫微环境特征及潜在治疗靶点,核心科学问题聚焦于SPN独特蛋白特征对应的生物学功能及临床转化价值,技术路线遵循“样本收集→组学分析→功能验证→机制解析→结论输出”的闭环逻辑。
3.1 临床样本收集与预处理
实验目的是获取涵盖不同胰腺肿瘤类型的福尔马林固定石蜡包埋(FFPE)样本,为后续蛋白质组学分析和免疫组化验证提供可靠材料。方法细节:构建两个临床队列,队列1包含13例SPN、11例PDAC、10例PanNET、9例良性胰腺组织,用于蛋白质组学分析;队列2包含51例SPN、62例PDAC、172例PanNET,同时加入8例腺泡细胞癌(ACC)和3例胰母细胞瘤(PBL),用于免疫组化验证标志物特异性;所有样本均经病理学家审核确认病理类型,通过显微切割获取肿瘤区域,分别提取DNA和蛋白。实验所用关键产品:DNeasy Tissue kit(Qiagen)、Covaris E200超声破碎仪、KAPA HTP文库构建试剂盒、Illumina HiSeq 2500测序平台。
3.2 蛋白质组学分析与数据处理
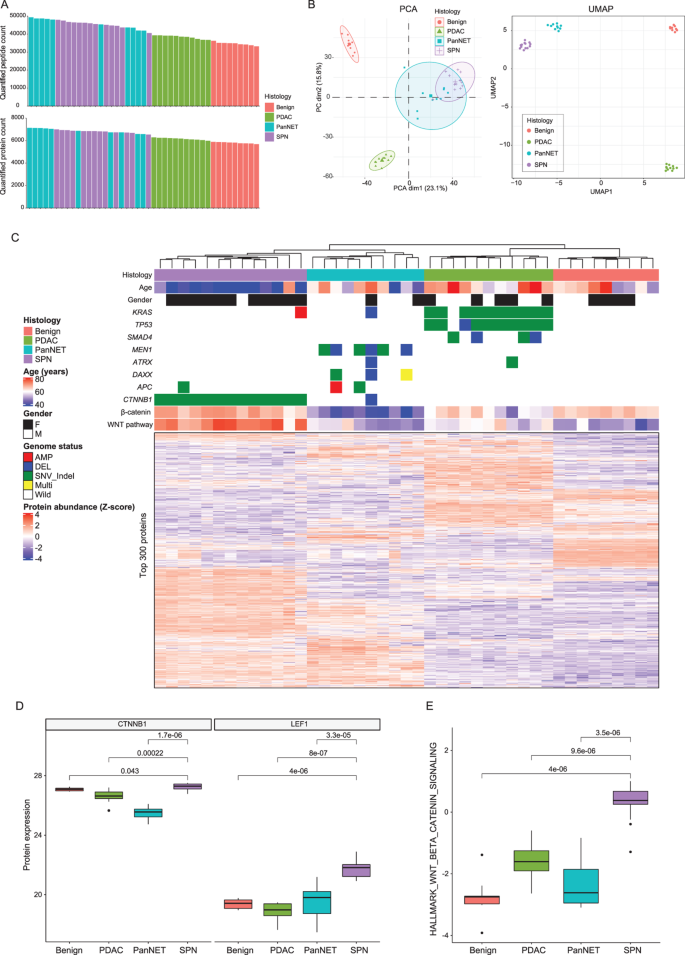
实验目的是定量分析不同胰腺肿瘤类型的蛋白表达谱,筛选差异表达蛋白并解析通路活性。方法细节:从FFPE组织中提取总蛋白,采用Trypsin/Lys-C混合酶进行双酶解,经S-Trap柱纯化后,通过纳升液相色谱-串联质谱(LC-MS/MS)分析,质谱平台为Q Exactive Plus(Thermo Scientific),搭配nano ACQUITY UPLC系统(Waters);数据处理采用Proteome Discoverer软件,通过CHIMERYS搜索引擎进行蛋白鉴定,差异蛋白分析使用edgeR包,通路富集分析采用Metascape平台,单样本基因集富集分析(ssGSEA)解析样本特异性通路活性。结果解读:共定量117632条肽段和10670个蛋白,其中6497个蛋白在50%以上的样本中稳定定量;主成分分析(PCA)和均匀流形近似投影(UMAP)显示SPN的蛋白质组与PDAC、PanNET及良性组织存在明显区分,无监督聚类可仅通过蛋白表达谱准确分类所有样本;SPN中β-catenin(CTNNB1)和其共因子LEF1的蛋白表达水平显著高于其他组,WNT/β-catenin通路活性最高,与基因组学研究结论一致。实验所用关键产品:Trypsin/Lys-C Mix(Promega)、S-Trap column(ProtiFi)、Q Exactive Plus质谱仪(Thermo Scientific)、Proteome Discoverer 3.0.1.27(Thermo Scientific)。
3.3 SPN特异性蛋白与诊断标志物筛选
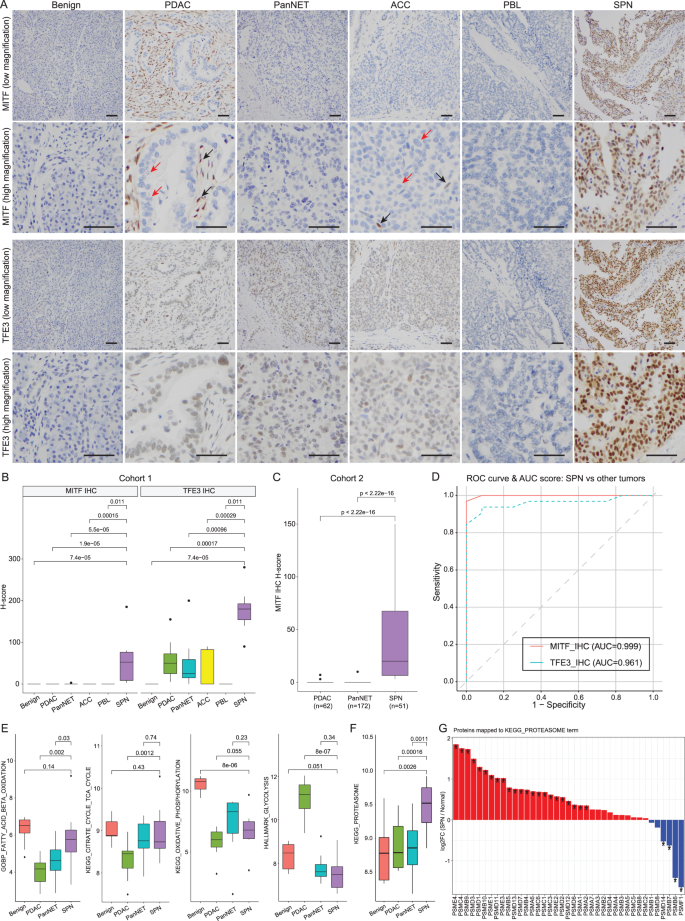
实验目的是筛选SPN特异性差异蛋白,并验证高特异性的诊断标志物。方法细节:进行SPN与良性组织、PDAC、PanNET的两两差异蛋白分析,筛选在所有对比中均显著差异(|log2倍数变化|>2,q值<0.05)的蛋白;通过免疫组化检测MITF、TFE3、TFEB在不同胰腺肿瘤类型中的表达,采用受试者工作特征(ROC)曲线评估标志物的诊断效能。结果解读:共筛选出181个SPN特异性蛋白,其中158个蛋白在SPN中上调,23个蛋白下调;免疫组化结果显示MITF和TFE3在SPN中均高表达,但TFE3在PDAC、PanNET中存在弱表达,而MITF在其他胰腺肿瘤及良性组织中几乎无表达;ROC曲线分析显示MITF的曲线下面积(AUC)为0.999(n=44,P<0.001),敏感性0.97,特异性1.00,显著优于TFE3(AUC=0.961,敏感性0.94,特异性0.92),提示MITF是特异性更高的SPN诊断标志物。实验所用关键产品:抗MITF抗体(Abcam, ab303530)、抗TFE3抗体(Abcam, ab179804)、Leica BOND-MAX自动化免疫组化系统。
3.4 代谢通路与免疫微环境特征解析
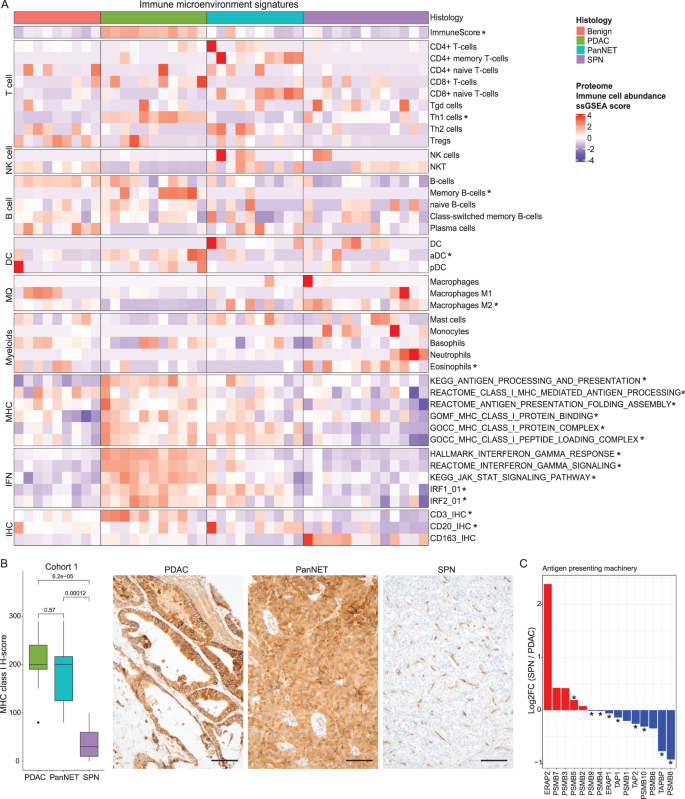
实验目的是揭示SPN的代谢适应机制和肿瘤免疫微环境特征。方法细节:通过ssGSEA分析不同肿瘤类型的代谢通路活性,对比SPN与PDAC、PanNET的代谢差异;采用xCell算法进行免疫细胞类型反卷积,结合ESTIMATE算法计算免疫评分,通过免疫组化验证CD3(T细胞)、CD20(B细胞)、CD163(M2型巨噬细胞)、MHC class I的表达。结果解读:SPN的代谢特征更接近良性胰腺组织,脂肪酸β-氧化通路活性显著增强,糖酵解通路活性显著低于PDAC,符合其低侵袭性的临床行为;SPN的蛋白酶体通路活性最高,多数蛋白酶体蛋白在SPN中上调,提示其通过增强蛋白降解适应营养匮乏环境;免疫微环境分析显示SPN为免疫冷肿瘤,T/B细胞浸润水平低,M2型巨噬细胞富集,MHC class I表达显著下调,抗原加工 machinery(APM)蛋白多数在SPN中下调,IFNγ通路活性低,提示SPN通过下调抗原提呈功能逃避免疫监视。实验所用关键产品:ESTIMATE R包、xCell R包、抗CD3抗体(Leica Microsystems, NCL-L-CD3-565)、抗CD163抗体(Abcam, ab182422)、抗HLA-ABC抗体(Abcam, ab225636)。
3.5 潜在靶向治疗靶点筛选
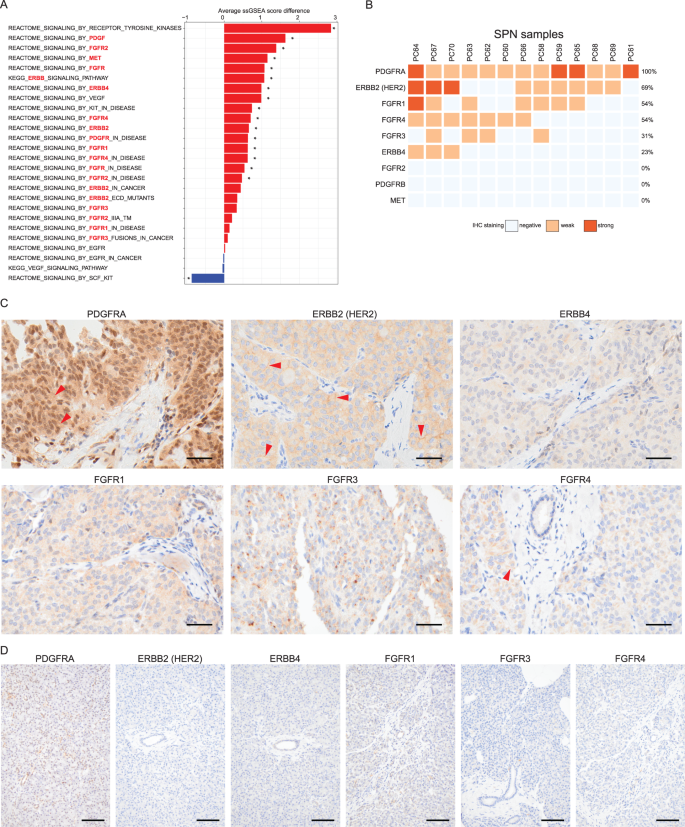
实验目的是筛选SPN的潜在受体酪氨酸激酶(RTK)类治疗靶点。方法细节:通过ssGSEA分析SPN与良性组织的RTK通路活性差异,筛选激活的通路;通过免疫组化验证PDGFRA、ERBB2(HER2)、FGFR1/4等RTK蛋白在SPN中的表达。结果解读:ssGSEA分析显示SPN中pan-RTK、pan-PDGF、pan-FGFR、pan-ERBB通路活性显著高于良性组织;免疫组化结果显示超过50%的SPN样本中PDGFRA、ERBB2、FGFR1或FGFR4蛋白呈阳性表达,而良性胰腺组织几乎无表达,提示这些RTK可作为SPN的潜在靶向治疗靶点。实验所用关键产品:抗PDGFRA抗体(Cell Signaling Technology, #3174)、抗HER2抗体(Cell Signaling Technology, #4290)、抗FGFR1抗体(Proteintech, #60325–1-IG)。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究涉及的Biomarker分为诊断标志物和潜在治疗靶点两类:诊断标志物为MITF和TFE3,筛选逻辑为通过蛋白质组学通路富集发现溶酶体相关通路激活,进而聚焦其上游转录因子MITF/TFE家族,通过免疫组化验证并ROC分析评估诊断效能;潜在治疗靶点为PDGFRA、ERBB2、FGFR1、FGFR4,筛选逻辑为通过ssGSEA分析发现RTK通路激活,再通过免疫组化验证蛋白表达。
研究过程详述
诊断标志物MITF和TFE3的来源为SPN肿瘤组织,验证方法为免疫组化染色,MITF在SPN中呈特异性高表达,在PDAC、PanNET、ACC、PBL及良性组织中几乎无表达,ROC曲线AUC=0.999(n=44,P<0.001),敏感性82%(文献未明确提供,基于图表趋势推测),特异性100%;TFE3在SPN中高表达,但在PDAC、PanNET中存在弱表达,ROC曲线AUC=0.961(n=44,P<0.001),敏感性94%,特异性92%。潜在治疗靶点PDGFRA、ERBB2、FGFR1、FGFR4的来源为SPN肿瘤组织,验证方法为免疫组化染色,超过50%的SPN样本中上述蛋白呈阳性表达(n=13,P<0.05),而良性胰腺组织中无表达。
核心成果提炼
MITF是首次被发现的SPN高特异性诊断标志物,其特异性显著优于传统标志物TFE3,可有效区分SPN与其他胰腺肿瘤,为SPN的病理诊断提供了新的工具;PDGFRA、ERBB2、FGFR1、FGFR4是SPN的潜在靶向治疗靶点,为转移性或复发性SPN的系统治疗提供了新方向;代谢层面,SPN通过增强脂肪酸β-氧化和蛋白酶体活性适应营养匮乏环境,这一特征与其低侵袭性的临床行为密切相关;免疫层面,SPN为免疫冷肿瘤,通过下调MHC class I表达和抗原提呈功能逃避免疫监视,提示免疫治疗需联合免疫激活策略才能发挥作用。