1. 领域背景与文献引入
文献英文标题:Measurable residual disease monitoring in acute myeloid leukemia: current landscape and emerging technologies;发表期刊:未明确提供;影响因子:未公开;研究领域:急性髓系白血病微小残留病检测
急性髓系白血病(AML)是一类具有高度异质性的血液系统恶性肿瘤,尽管近几十年来治疗取得显著进展,包括十余种化疗药物获批、异基因造血干细胞移植(HSCT)的常规应用,但仍有30%~50%获得完全缓解(CR,骨髓原始细胞<5%、外周血计数正常、无髓外病变)的患者最终复发,核心原因是常规形态学检测无法识别的残留白血病干细胞(LSC)持续存在。微小残留病(MRD)检测作为AML预后评估和治疗决策的关键工具,已成为领域研究热点。当前临床常用的MRD检测方法包括多参数流式细胞术(MFC)、定量PCR(qPCR)、下一代测序(NGS),这些方法虽具有明确的预后价值,但存在技术复杂度高、标志物特异性不足、可及性有限等局限:MFC依赖新鲜高质量样本,实验室间重复性差;qPCR仅适用于约50%携带特定基因突变或融合的患者;NGS成本高昂且需专业数据分析能力。此外,部分患者缺乏有效MRD检测标志物,现有方法的检测灵敏度和覆盖范围仍需提升。针对上述领域空白,本文系统综述了AML中MRD检测的现有技术与新兴方法,重点探讨DNA甲基化分析和表面增强拉曼散射(SERS)技术的临床潜力,为MRD检测的优化与创新提供参考。
2. 文献综述解析
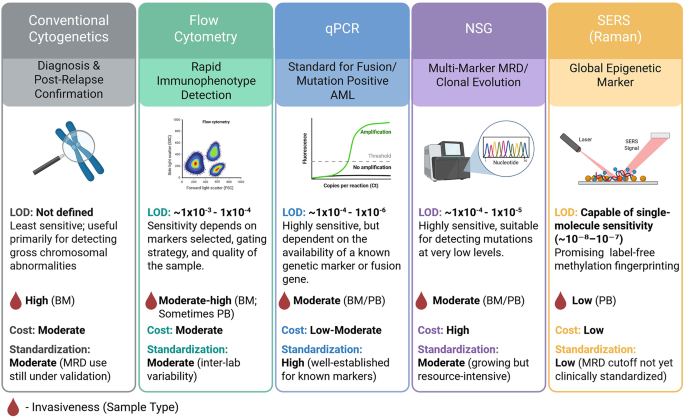
本文按检测技术类型对AML MRD检测方法进行分类综述,涵盖细胞遗传学、免疫表型分析(MFC)、分子生物学方法(PCR、NGS)及新兴的DNA甲基化、SERS技术,系统对比各类方法的优势、局限及临床应用证据,重点聚焦新兴技术的验证需求与转化潜力。
作者首先梳理了细胞遗传学方法的临床应用,该方法通过G显带或荧光原位杂交(FISH)检测染色体异常,部分研究显示其在HSCT前MRD评估中可预测患者复发率、无进展生存期(PFS)和总生存期(OS),但检测限(LoD)不明确,不同研究结果存在矛盾,临床价值仍需进一步验证。接着综述了MFC方法,其作为当前应用最广泛的MRD检测技术,分为白血病相关免疫表型(LAIP)和异常分化(DfN)两种策略,可覆盖90%以上AML病例,检测限为10^-3~10^-4,能区分活细胞与死细胞,但存在需新鲜样本、实验室间标准化不足、结果解读需专业经验等局限,且约35%的检测会出现“不确定”结果,对应中等复发风险人群。对于分子生物学方法,qPCR灵敏度可达10^-4~10^-6,但仅适用于携带特定基因融合(如RUNX1::RUNX1T1、CBFB::MYH11)或突变(如NPM1)的患者,覆盖约50%AML病例;NGS灵敏度为10^-4~10^-5,无需预先知晓突变状态,可实现个性化检测,但成本高、数据分析难度大。最后,作者重点介绍了新兴的DNA甲基化和SERS技术,DNA甲基化利用AML细胞的表观遗传异常,通过检测CpG位点甲基化水平反映疾病负荷;SERS通过检测生物流体或DNA的分子光谱特征实现非侵入性检测,检测限可达10^-6,但目前仍处于概念验证阶段,需大样本临床研究验证。
与现有综述相比,本文的核心创新价值在于不仅系统总结了常规MRD检测方法的临床证据,更聚焦DNA甲基化和SERS这两类新兴技术,填补了对其临床应用潜力、验证需求及与传统方法对比分析的空白,为AML MRD检测技术的未来发展方向提供了全面的参考框架,尤其为缺乏有效分子标志物的患者提供了潜在的检测新途径。
3. 研究思路总结与详细解析
本文采用综述研究框架,以AML MRD检测的临床需求为切入点,先阐述MRD在AML治疗中的重要性,再按技术类型分章节解析各类MRD检测方法的原理、临床数据、优势与局限,最后重点探讨新兴技术的研究进展与转化前景,整体逻辑清晰,覆盖了从常规到新兴技术的全维度分析。
3.1 细胞遗传学MRD检测方法解析
实验目的:明确细胞遗传学方法在AML MRD检测中的临床价值与局限性。
方法细节:通过G显带或荧光原位杂交(FISH)技术检测患者骨髓或外周血中的染色体异常,包括平衡结构异常(如易位、倒位)和非平衡结构异常(如缺失、重复、单体),并对比其与MFC、qPCR、NGS等方法的检测限。
结果解读:部分临床研究显示,HSCT前采用细胞遗传学方法检测MRD阳性的患者复发率显著升高,PFS和OS显著降低,与MFC检测结果的预后价值相当;但细胞遗传学的检测限未明确界定,且不同研究结果存在矛盾,其临床应用仍需进一步验证。
产品关联:文献未提及具体实验产品,领域常规使用染色体核型分析试剂盒、FISH探针试剂盒等。
3.2 多参数流式细胞术MRD检测方法解析
实验目的:系统分析MFC在AML MRD检测中的应用策略、临床预后价值与技术局限。
方法细节:采用LAIP和DfN两种策略,LAIP监测诊断时确定的白血病特异性免疫表型,DfN通过对比正常细胞识别异常免疫表型;当前指南推荐整合两种策略,使用CD34、CD117、CD45等核心标志物面板,针对单核细胞亚型可补充CD64、CD11b等标志物。
结果解读:MFC可覆盖90%以上AML病例,检测限为10^-3~10^-4,儿童AML研究显示,诱导治疗后第28-35天(TP1)和第二次诱导治疗结束时(TP2)的MRD阳性均与不良预后相关,其中TP2 MRD是更强的独立预测因子;约35%的检测会出现“不确定”结果(原始细胞占比0.01%~0.1%),该人群复发率(21%)介于MRD阴性(8%)与明确阳性(33%)之间,提示需密切监测;HSCT前MRD阳性患者复发风险更高,且“低MRD”(0.1%~0.5%)与“高MRD”(>0.5%)的复发风险无显著差异。
产品关联:文献未提及具体实验产品,领域常规使用流式细胞仪、白血病免疫表型检测抗体面板等。
3.3 分子生物学MRD检测方法解析
实验目的:对比PCR与NGS在AML MRD检测中的应用范围、灵敏度与临床价值。
方法细节:qPCR主要检测特定基因融合(如RUNX1::RUNX1T1)和突变(如NPM1);NGS采用基因面板检测,需排除生殖系突变和年龄相关克隆造血(CHIP)相关突变(如DNMT3A、TET2、ASXL1),仅跟踪与白血病克隆明确相关的突变(如NPM1、FLT3-ITD),缓解后可采用患者特异性最小面板进行纵向监测。
结果解读:qPCR灵敏度可达10^-4~10^-6,但仅适用于约50%AML患者;NGS灵敏度为10^-4~10^-5,可检测约80%MFC阳性的MRD病例,HSCT前NGS检测到FLT3-ITD或NPM1突变的患者复发率升高、预后不良;NGS可识别常规方法未检测到的突变,为治疗决策提供更全面的依据,但成本高、数据分析难度大。
产品关联:文献未提及具体实验产品,领域常规使用qPCR扩增试剂盒、NGS测序文库制备试剂盒、基因测序平台等。
3.4 新兴DNA甲基化MRD检测技术解析
实验目的:探讨DNA甲基化作为AML MRD检测标志物的潜力与挑战。
方法细节:利用AML细胞的表观遗传异常,通过焦磷酸测序、亚硫酸氢盐扩增测序(BA-seq)等技术检测特定基因(如PDE4C)或CpG位点的甲基化水平,构建评分模型(如d-score、n-score、AML-score)区分恶性与正常样本。
结果解读:PDE4C基因的甲基化评分在AML诊断和复发时显著升高,完全缓解时恢复正常,且与MDS患者的总生存期相关;基于四个CpG位点的AML-score在诊断时准确性高,但区分MRD阳性与阴性样本的能力有限,主要受健康对照甲基化变异的影响,提示需提升检测灵敏度或与其他方法整合。
产品关联:文献未提及具体实验产品,领域常规使用甲基化DNA提取试剂盒、焦磷酸测序试剂盒、亚硫酸氢盐转化试剂盒等。
3.5 新兴SERS技术在MRD检测中的应用解析
实验目的:评估SERS技术在AML MRD检测中的可行性与临床潜力。
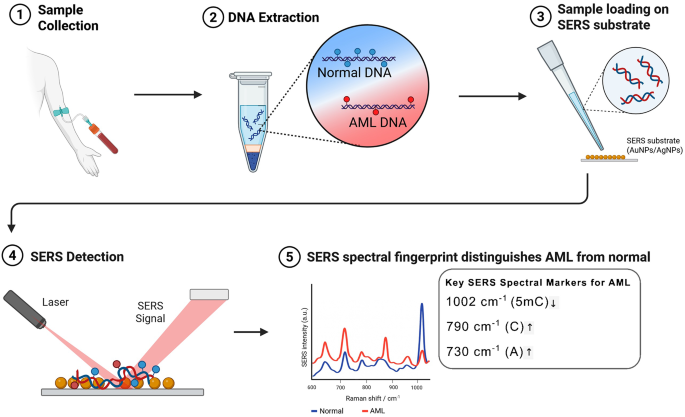
方法细节:采用银或金纳米颗粒增强拉曼信号,直接分析血清、血浆等生物流体的分子光谱特征,或提取DNA后检测甲基化相关的光谱差异,结合深度学习算法进行样本分类。
结果解读:概念验证研究显示,SERS可区分AML患者与健康对照,准确率达95.4%~100%,还可区分AML与急性淋巴细胞白血病(ALL),并能识别与复发相关的光谱特征;检测限可达10^-6,且具有非侵入性、快速、无需标记的优势,但目前研究多为回顾性小样本,缺乏外部验证,且无法精确定位甲基化位点或基因突变,需与现有方法整合提升可靠性。
产品关联:文献未提及具体实验产品,领域常规使用SERS基底(如金/银纳米颗粒)、拉曼光谱仪等。
4. Biomarker研究及发现成果解析
本文涉及的MRD Biomarker涵盖染色体异常、免疫表型标志物、基因突变/融合、DNA甲基化位点、SERS分子光谱特征五大类,各类标志物的筛选与验证逻辑、临床价值存在差异,新兴标志物为缺乏有效检测手段的患者提供了潜在方向。
Biomarker定位与筛选验证逻辑:染色体异常标志物通过细胞遗传学技术筛选,验证其在HSCT前MRD评估中的预后价值;免疫表型标志物通过MFC的LAIP和DfN策略筛选,基于大规模临床研究验证其预后意义;基因突变/融合标志物通过qPCR或NGS筛选,针对携带特定突变的患者进行纵向监测;DNA甲基化标志物基于AML的表观遗传异常,通过焦磷酸测序、BA-seq等技术筛选特定基因或CpG位点,验证其与疾病负荷的相关性;SERS分子光谱特征通过分析生物流体或DNA的拉曼光谱筛选,结合深度学习算法验证其分类准确性。
研究过程详述:染色体异常标志物来源于患者骨髓或外周血样本,通过G显带或FISH检测,部分研究显示其可预测HSCT后复发风险,但检测限未明确;免疫表型标志物来源于骨髓样本,MFC检测核心标志物面板的表达异常,儿童AML研究显示TP2 MRD阳性(≥0.1%)患者PFS和OS显著降低(文献未明确样本量与P值);基因突变/融合标志物来源于骨髓样本,qPCR检测NPM1突变等的灵敏度可达10^-6,NGS检测到的非CHIP突变(VAF≥0.1%~1%)具有临床意义;DNA甲基化标志物来源于骨髓或外周血样本,PDE4C基因的d-score和n-score在AML诊断时显著升高(文献未明确具体数值与统计学结果);SERS分子光谱特征来源于血清或DNA样本,检测限可达10^-6,区分AML与健康对照的准确率达95.4%(n=67,43例AML、24例健康对照)、100%(n=50,20例AML、30例健康对照)。
核心成果提炼:染色体异常标志物可作为MFC的补充方法,部分场景下具有预后价值;免疫表型标志物覆盖范围广,是当前临床最常用的MRD检测指标,可有效分层复发风险;基因突变/融合标志物灵敏度高,为携带特定突变的患者提供精准监测手段;DNA甲基化标志物可反映疾病负荷,为缺乏分子标志物的患者提供潜在检测途径,但目前区分MRD的能力有限;SERS标志物具有非侵入性、快速、高灵敏度的优势,可实现AML的早期诊断与复发风险预测,但需大样本临床研究验证。其中,SERS技术作为新兴非侵入性方法,首次在AML中展示了通过分子光谱特征区分患者与健康对照、识别复发风险的潜力,为MRD检测的非侵入化发展提供了新方向;DNA甲基化评分模型首次将表观遗传特征与AML疾病负荷关联,拓展了MRD检测的标志物类型。