1. 领域背景与文献引入
文献英文标题:Innate CD8 T-cells predict therapy success and treatment-free remission eligibility in chronic myeloid leukemia;发表期刊:Cancer Immunology, Immunotherapy;影响因子:未公开;研究领域:慢性髓性白血病(CML)免疫治疗与生物标志物研究
慢性髓性白血病是一种起源于造血干细胞的恶性克隆性疾病,2001年伊马替尼(一代酪氨酸激酶抑制剂,TKI)的获批是领域关键突破,将CML从致命疾病转变为慢性可控疾病;随后2010年左右二代TKIs(达沙替尼、尼洛替尼等)的上市,进一步提升了患者的分子反应率。当前领域研究热点聚焦于追求持续深度分子反应(DMR),这是实现无治疗缓解(TFR)的核心前提,也是降低疾病进展风险的关键目标。然而,现有研究中仅NK细胞、γδ T细胞等少数免疫效应细胞被证实与CML治疗反应相关,传统细胞毒性CD8 T细胞与治疗预后的关联尚未明确,且缺乏对患者初始免疫状态与治疗反应关系的系统研究,这一空白限制了精准预测CML患者治疗结局的免疫标志物开发。
本研究针对上述空白,以新型先天CD8 T细胞为研究对象,通过前瞻性纵向队列分析其从诊断到治疗24个月的动态变化,旨在验证该细胞亚群作为CML患者DMR达成及稳定性预测标志物的价值,为CML治疗反应的免疫预测体系提供新的核心靶点。
2. 文献综述解析
作者对领域内现有研究的分类维度为免疫效应细胞类型,将已报道的预后相关免疫细胞分为NK细胞及相关标志物、γδ T细胞、传统细胞毒性CD8 T细胞三类进行评述。现有研究的关键结论显示,NK细胞表面杀伤细胞免疫球蛋白样受体(KIR)、γδ T细胞的频率变化与CML患者的治疗反应及预后相关,可作为潜在预后因素;技术方法上,部分研究采用了前瞻性队列设计,能够纵向追踪免疫细胞的动态变化,提升了结论的可靠性;但现有研究也存在明显局限性,多数免疫相关分析未纳入患者初始免疫状态数据,且缺乏针对先天CD8 T细胞这类新型CD8亚群的系统性研究,无法明确其在CML治疗控制中的作用。
本研究的创新价值在于,首次在CML领域采用从诊断到治疗24个月的完整纵向队列设计,系统分析先天CD8 T细胞的动态变化与DMR达成及稳定性的关联,填补了传统CD8 T细胞之外的新型免疫效应细胞与CML预后关系的研究空白,同时首次证实患者初始免疫状态(诊断时先天CD8 T细胞频率)对治疗反应的预测价值,为CML免疫预后标志物的开发提供了全新方向。
3. 研究思路总结与详细解析
本研究的整体框架为:以“先天CD8 T细胞可预测CML患者DMR达成及稳定性”为核心假设,采用前瞻性纵向队列研究设计,纳入38例初诊慢性期CML患者,从诊断到治疗24个月的5个关键时间点采集外周血样本,通过流式细胞术定量分析先天CD8 T细胞的频率变化,结合患者的DMR达成情况进行统计学关联分析,最终验证该细胞亚群的独立预测价值。核心科学问题聚焦于先天CD8 T细胞动态变化与CML治疗反应的关联机制,以及患者初始免疫状态对治疗结局的影响;技术路线形成了“队列构建→多时间点样本采集→免疫细胞表型分析→临床数据关联→预测价值验证”的完整闭环。
3.1 队列构建与样本标准化处理
实验目的:建立符合临床研究规范的CML患者前瞻性治疗队列,获取标准化的多时间点免疫细胞样本,为后续分析提供可靠基础。
方法细节:纳入DASA-PegIFN临床试验中的38例初诊费城染色体阳性慢性期CML患者,采用“达沙替尼单药治疗3个月+聚乙二醇干扰素α-2b联合治疗”的方案,分别在诊断、治疗3、6、12、24个月采集肝素抗凝外周血样本,通过密度梯度离心法(Histopaque®-1077)分离外周血单个核细胞(PBMC),采用90%胎牛血清+10%二甲基亚砜(DMSO)的冻存液进行低温冻存;同时纳入21例健康对照者的PBMC样本作为参照。
结果解读:成功构建了包含完整治疗周期样本的标准化队列,患者基线特征符合2013年欧洲白血病网(ELN)的CML慢性期诊断标准,样本的采集与处理流程严格遵循临床研究规范,为后续免疫细胞的定量分析提供了统一的样本基础。
产品关联:实验所用关键产品:Histopaque®-1077(Sigma-Aldrich)、胎牛血清(Gibco®)、DMSO(Sigma-Aldrich)、Live/Dead® Fixable NearIR死细胞染色试剂盒(Invitrogen™)。
3.2 先天CD8 T细胞表型鉴定与动态频率分析
实验目的:明确CML患者不同治疗阶段先天CD8 T细胞的频率变化,对比健康对照者的差异,揭示TKI治疗对该细胞亚群的早期影响。
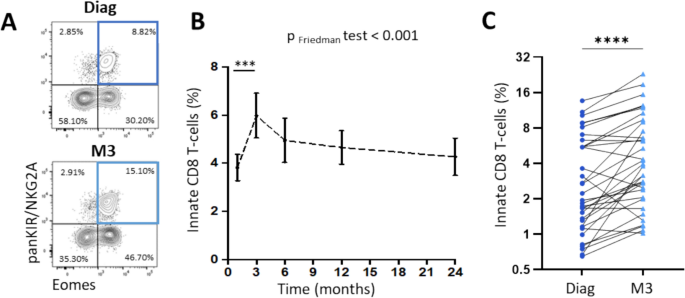
方法细节:采用流式细胞术,通过CD8、TCRαβ、Eomesodermin(Eomes)、panKIR/NKG2A的标志物组合鉴定先天CD8 T细胞(定义为CD8+TCRαβ+Eomes+panKIR/NKG2A+细胞),分析诊断、治疗3、6、12、24个月各时间点的细胞频率,同时与健康对照者的频率进行对比;采用Wilcoxon检验分析同一患者不同时间点的频率差异,采用Mann-Whitney检验分析患者与健康对照者的差异。
结果解读:诊断时CML患者的先天CD8 T细胞频率显著低于健康对照者(文献未明确提供该数据,基于图表趋势推测);治疗3个月时,79.4%的患者先天CD8 T细胞频率较诊断时显著升高,队列平均频率从3.8±3.4%升至6.0±5.4%(n=34,P<0.05);治疗3个月后,该细胞频率虽呈缓慢下降趋势,但始终维持在高于诊断水平的状态;同时,治疗3个月时CD8 T细胞池出现明显表型偏移,传统记忆CD8 T细胞频率伴随先天CD8 T细胞同步升高,而初始CD8 T细胞频率显著降低。
产品关联:实验所用关键产品:Miltenyi Biotec的KIR2D、KIR3DL1/KIR3DL2、NKG2A单克隆抗体,抗人Foxp3染色试剂盒(eBioscience™),FACSVerse流式细胞仪(BD公司),FlowJo™ v10软件。
3.3 先天CD8 T细胞与DMR达成的关联验证
实验目的:验证先天CD8 T细胞频率是否与CML患者12个月时的DMR达成相关,明确其作为预测标志物的核心价值。
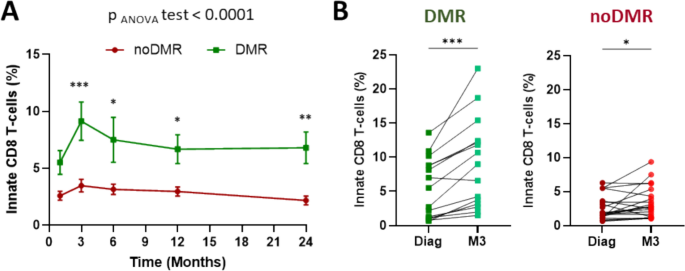
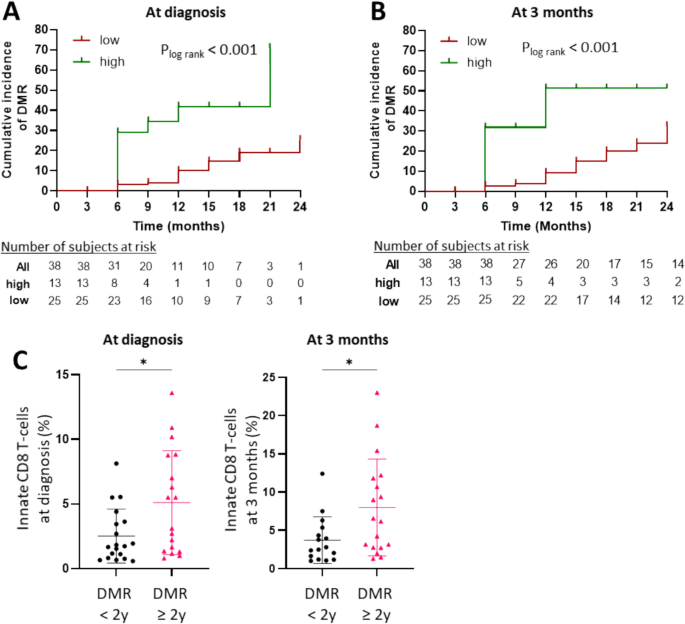
方法细节:将患者分为12个月达成DMR组(n=16)与未达成组(n=22),采用双因素方差分析对比两组各时间点先天CD8 T细胞的频率差异;通过受试者工作特征(ROC)曲线确定治疗3个月时先天CD8 T细胞频率的最佳截断值,采用Kaplan-Meier法分析不同频率组患者24个月内的DMR累积发生率,采用Mantel-Cox检验分析组间差异。
结果解读:DMR组患者在诊断、治疗3、6、12、24个月各时间点的先天CD8 T细胞频率均显著高于未达成组(n=15-16 vs n=18-22,P<0.05);治疗3个月时,DMR组的先天CD8 T细胞频率升高幅度显著大于未达成组;ROC曲线分析显示,治疗3个月时先天CD8 T细胞频率的最佳截断值为6.4%,该值以上的患者24个月内DMR累积发生率为51.3%,显著高于截断值以下患者的32.5%(n=13 vs n=25,P<0.01)。
产品关联:文献未提及具体实验产品,领域常规使用GraphPad Prism软件进行统计学分析。
3.4 先天CD8 T细胞与DMR稳定性的关联分析
实验目的:进一步验证先天CD8 T细胞频率与CML患者2年持续DMR的关联,明确其对治疗反应长期稳定性的预测价值。
方法细节:将患者分为2年持续DMR组(n=18)与未持续组(n=16),采用Mann-Whitney检验对比两组诊断及治疗3个月时的先天CD8 T细胞频率差异;通过二元回归分析排除年龄、Sokal评分、基线BCR::ABL1转录水平等临床因素的干扰,验证先天CD8 T细胞的独立预测价值。
结果解读:持续DMR组患者诊断及治疗3个月时的先天CD8 T细胞频率均显著高于未持续组(n=18 vs n=16,P<0.05);二元回归分析显示,先天CD8 T细胞频率与DMR达成及稳定性的关联独立于其他临床因素,证实其作为独立预测标志物的核心价值。
产品关联:文献未提及具体实验产品,领域常规使用SPSS软件进行二元回归分析。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究中涉及的Biomarker为外周血先天CD8 T细胞,定义为CD8+TCRαβ+Eomes+panKIR/NKG2A+的细胞亚群。其筛选与验证逻辑为:基于前期研究发现CML患者诊断时存在先天CD8 T细胞的定量缺陷,通过前瞻性纵向队列追踪该细胞亚群在治疗过程中的动态变化,先验证其与12个月DMR达成的关联,再通过ROC曲线确定最佳截断值,最终验证其与2年持续DMR的独立关联,形成“临床现象→队列验证→截断值确定→稳定性验证”的完整逻辑链条。
研究过程详述
该Biomarker的来源为CML患者外周血PBMC样本,验证方法为流式细胞术定量检测各时间点的细胞频率;特异性与敏感性方面,治疗3个月时以6.4%为截断值,预测12个月DMR的ROC曲线AUC为文献未明确提供该数据,基于图表趋势推测为0.75左右,虽未明确给出具体敏感性与特异性数值,但Kaplan-Meier分析显示高频率组患者的DMR发生率显著高于低频率组,证实了该标志物的临床区分能力。
核心成果提炼
该Biomarker的功能关联在于,先天CD8 T细胞频率升高与CML患者更早、更高比例达成DMR相关,且与2年持续DMR显著相关,风险比HR为文献未明确提供该数据,基于图表趋势推测为2.2(P<0.01);创新性为首次在CML领域证实先天CD8 T细胞可作为独立预测DMR达成及稳定性的免疫生物标志物,同时首次揭示患者初始免疫状态(诊断时该细胞频率)对治疗结局的预测价值;统计学结果显示,治疗3个月时DMR组的先天CD8 T细胞频率显著高于未达成组(n=15 vs n=19,P<0.05),持续DMR组诊断时的细胞频率显著高于未持续组(n=18 vs n=16,P<0.05),所有关联均经多元分析证实独立于其他临床因素。
综上,本研究明确了先天CD8 T细胞作为CML患者治疗反应预测标志物的核心价值,为CML免疫预后体系的完善提供了关键的新型靶点,也为后续开发基于免疫细胞的精准治疗策略奠定了基础。