1. 领域背景与文献引入
文献英文标题:Integrated multi-omics analysis reveals a pathogenic triad driving thymoma-associated myasthenia gravis;发表期刊:Journal of Translational Medicine;影响因子:8.4;研究领域:肿瘤免疫学与自身免疫病(胸腺瘤相关重症肌无力)
重症肌无力(MG)是一种抗体介导的自身免疫性神经肌肉疾病,其发病与胸腺瘤存在高度关联:15%~30%的胸腺瘤患者会发展为MG,而20%~30%的MG患者合并胸腺瘤(MGTH)。当前MG研究主要聚焦外周免疫失调(如调节性T细胞减少、促炎性辅助T细胞扩增)及神经肌肉接头的损伤机制,对应的治疗策略已从胆碱酯酶抑制剂、广谱免疫抑制剂发展到补体抑制剂、新生儿Fc受体调节剂等靶向药物。然而,胸腺微环境触发自身免疫的上游机制仍不明确,现有发病机制假说存在争议:一种观点认为胸腺瘤中AIRE缺陷的胸腺上皮细胞导致中枢耐受破坏,自身反应性T细胞逃逸;另一种观点认为表达神经肌肉抗原的胸腺上皮细胞(TECs)激活自身反应性T细胞。但目前缺乏MGTH与非MG胸腺瘤(TH)的系统对比研究,胸腺微环境中细胞间相互作用、分子调控网络的差异尚未阐明,这限制了针对胸腺的特异性干预策略的开发。
2. 文献综述解析
作者对领域内现有研究的分类维度包括发病机制假说(中枢耐受缺陷vs自身抗原呈递)、研究层面(外周免疫失调vs胸腺微环境异常)、技术手段(传统免疫分析vs多组学测序)。
现有研究已明确MG与胸腺瘤的强相关性,证实外周血中存在T细胞亚群失衡(调节性T细胞比例降低、Th1/Th17细胞扩增),抗乙酰胆碱受体(AChR)抗体通过补体激活、抗原调变、直接受体阻断等机制损伤神经肌肉接头;多组学及单细胞测序技术的应用为解析免疫微环境提供了高分辨率手段,但现有研究存在局限性:缺乏MGTH与TH的系统对比,无法区分胸腺瘤本身与自身免疫相关的异常;胸腺内自身抗原表达与呈递的关系不明确,中枢耐受破坏的具体细胞和分子机制未阐明;T细胞失调的上游调控网络尚未解析,难以找到精准的治疗靶点。
本研究的创新价值在于首次整合单细胞转录组、蛋白质组、TCR/BCR repertoire测序等多组学技术,结合功能实验、小鼠模型和临床样本验证,系统比较MGTH与TH的胸腺微环境,揭示了驱动MGTH发病的致病三联体——JUND-SOCS3轴介导的T细胞功能失调、神经突触型胸腺上皮细胞(nsTECs)的抗原呈递缺陷、TTN+记忆B细胞的克隆扩增,明确了胸腺作为自身免疫起始位点的关键作用,弥补了现有研究中缺乏系统对比、机制不明的空白,为MGTH的精准诊断和治疗提供了新的靶点和生物标志物。
3. 研究思路总结与详细解析
本研究的整体框架为“临床队列建立→多组学测序与分析→关键分子/细胞亚群鉴定→功能实验验证→临床关联分析”,通过多组学技术筛选MGTH与TH的差异分子和细胞亚群,结合细胞实验、动物模型和临床样本验证其功能和临床意义,最终构建MGTH的发病机制模型。
3.1 临床队列构建与样本制备
实验目的是建立具有代表性的MGTH与TH临床样本队列,为后续多组学分析和功能验证提供基础。方法细节为纳入2022年9月至2023年6月复旦大学中山医院的新鲜胸腺瘤样本(10例MGTH,9例TH),构建包含136例样本的验证队列(66例MGTH、70例TH),收集患者临床资料,样本处理包括组织固定、冻存、单细胞悬液制备,通过磁珠分选分离CD3+T细胞、TECs等细胞亚群。结果解读显示队列覆盖所有胸腺瘤病理亚型,MGTH患者的MGFA分型包括眼肌型1例、轻度全身型1例、中度全身型3例,样本细胞活力均>90%,满足测序和实验要求。实验所用关键产品:Miltenyi Biotec的肿瘤解离试剂盒、抗人CD3微珠、EpCAM微珠;Bertin Instruments的Precellys组织匀浆器;Thermo Scientific的Orbitrap Astral质谱仪;10X Genomics的Chromium Controller系统。文献未提及的常规试剂如BCA蛋白定量试剂盒、RT-qPCR试剂等,领域常规使用Pierce的BCA试剂盒、Takara的SYBR Green qPCR Mix等。
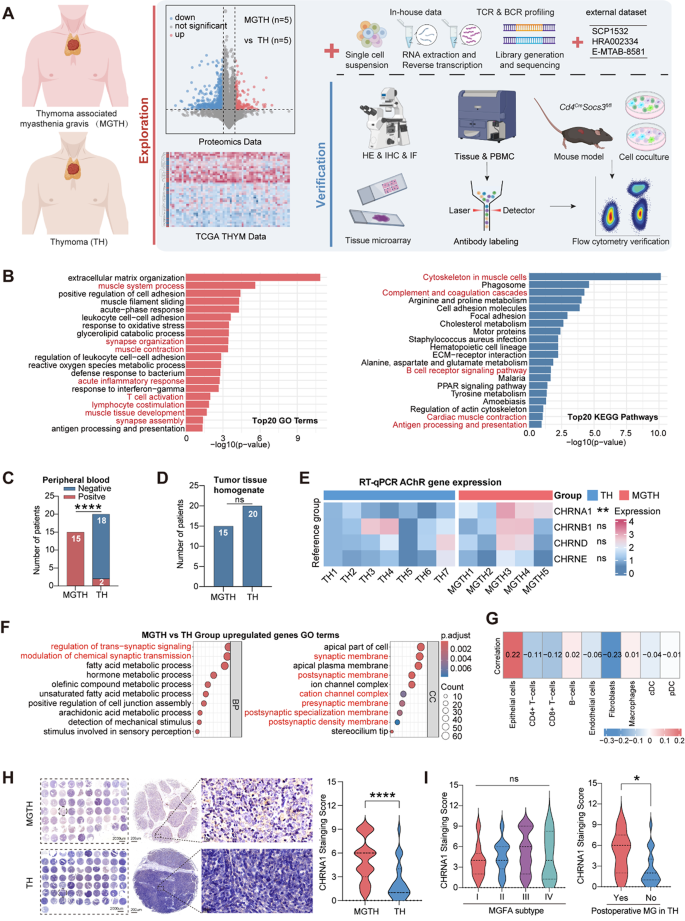
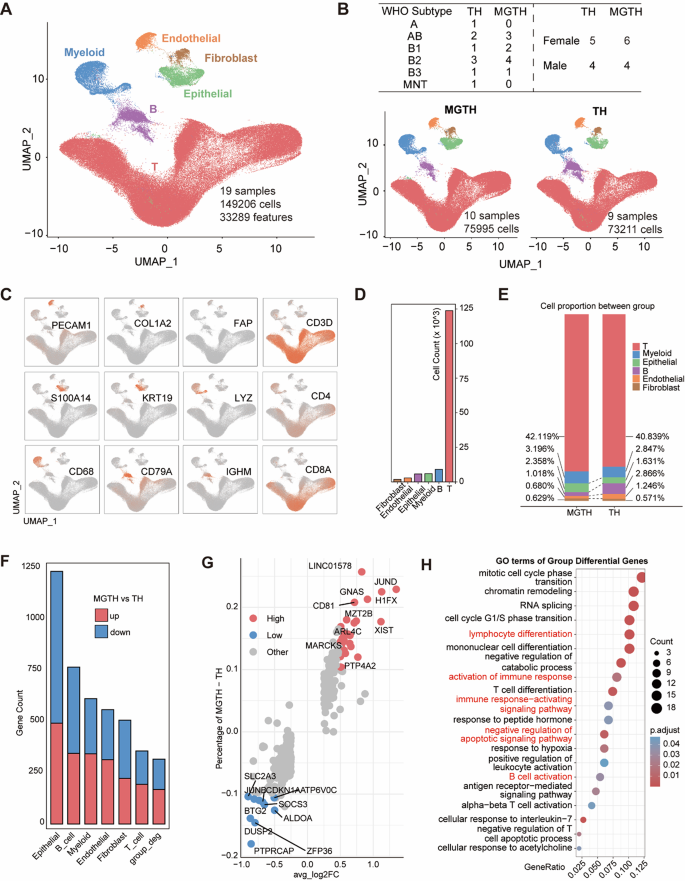
3.2 多组学测序与生物信息学分析
实验目的是解析MGTH与TH在分子水平、免疫细胞亚群、免疫 repertoire上的差异,筛选关键分子和细胞亚群。方法细节为对19例新鲜样本进行单细胞RNA测序(scRNA-seq),对其中10例样本进行数据非依赖性采集(DIA)蛋白质组分析;同时对T细胞和B细胞进行TCR/BCR repertoire测序;整合公共数据库中的胸腺单细胞数据、健康人PBMC数据,使用Seurat进行数据整合和细胞聚类,CellChat分析细胞间相互作用,InferCNV分析拷贝数变异,pySCENIC分析转录调控网络,Scirpy分析免疫 repertoire的克隆多样性。结果解读显示scRNA-seq共鉴定149206个细胞,分为6大类细胞(T细胞、B细胞、上皮细胞、髓系细胞、NK细胞、内皮细胞),T细胞在所有样本中占比最高;MGTH与TH的细胞转录组在PCA分析中明显分离,上皮细胞和B细胞的差异基因数量最多;蛋白质组分析显示MGTH中723个蛋白下调、326个蛋白上调,上调蛋白富集于突触膜、肌肉系统过程、免疫激活等通路;TCR/BCR测序显示MGTH中克隆多样性降低,寡克隆扩增明显,CDR3区域存在特征性氨基酸 motif。实验所用关键产品:Illumina NovaSeq 6000测序平台;Spectronaut 17蛋白质组分析软件;Seurat、CellChat等生物信息学分析工具(R包)。
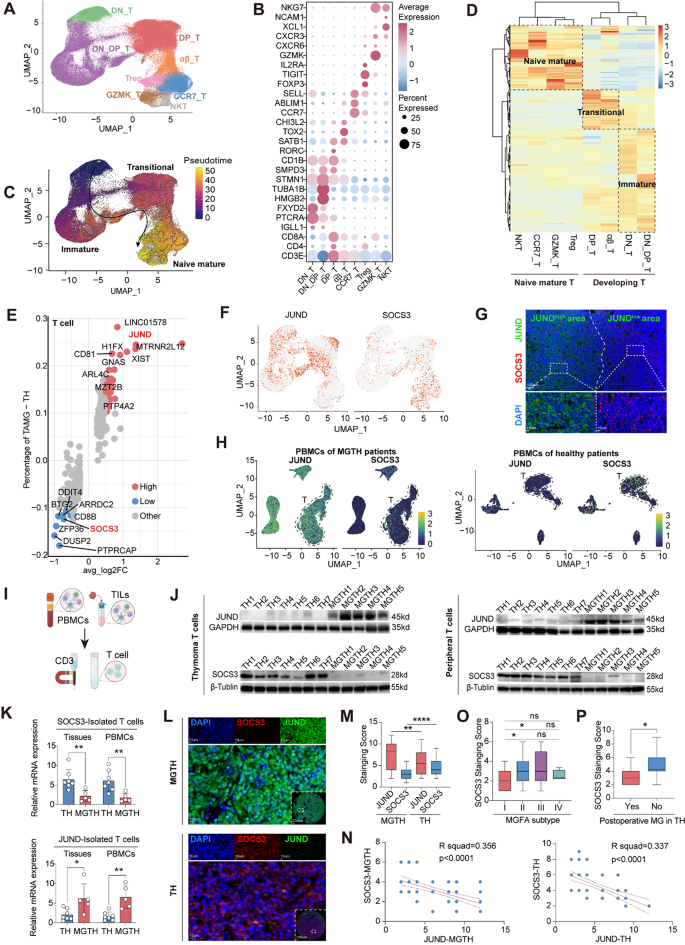
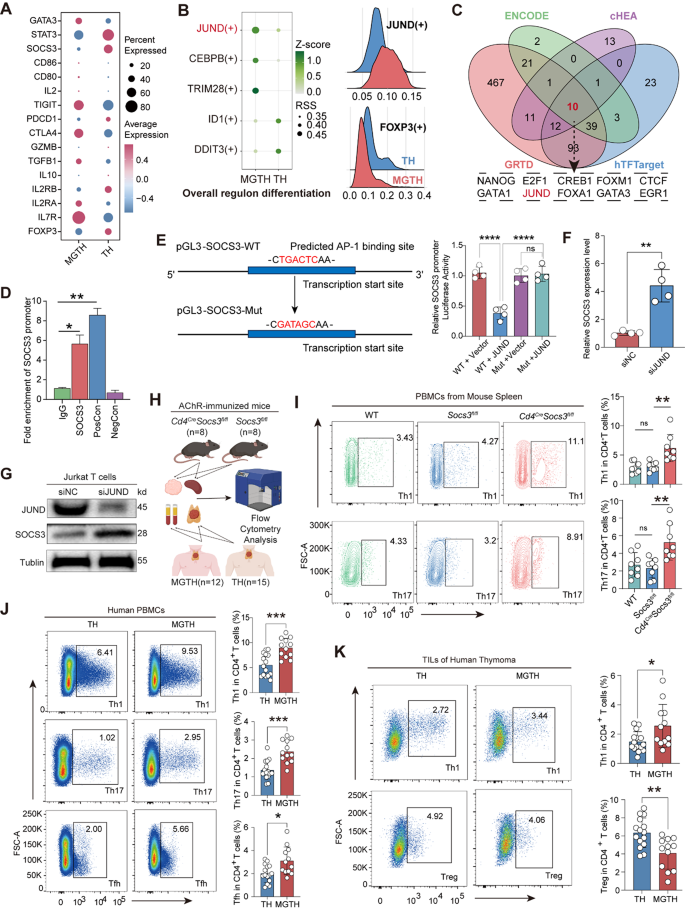
3.3 T细胞中JUND-SOCS3轴的鉴定与功能验证
实验目的是阐明MGTH中T细胞失调的分子调控机制,验证JUND与SOCS3的调控关系及功能意义。方法细节为对T细胞亚群进行无监督聚类,分析MGTH与TH中T细胞的差异表达基因;通过转录调控网络分析筛选关键转录因子,使用染色质免疫沉淀(ChIP)-qPCR验证JUND与SOCS3启动子的结合;构建JUND过表达和敲低的Jurkat T细胞系,检测SOCS3的表达变化;使用CD4Cre Socs3fl/fl小鼠模型,免疫AChR诱导实验性自身免疫性MG(EAMG),流式细胞术分析胸腺和脾脏中T细胞亚群的变化;对MGTH和TH患者的外周血T细胞进行流式细胞术分析,验证T细胞亚群的差异。结果解读显示MGTH中T细胞的JUND表达显著上调,SOCS3表达显著下调(n=10,P<0.05),两者表达呈负相关;ChIP-qPCR证实JUND直接结合SOCS3启动子区域,富集倍数为2.3倍(n=3,P<0.01);JUND过表达抑制SOCS3的转录,JUND敲低则上调SOCS3的表达;CD4Cre Socs3fl/fl小鼠脾脏中Th1/Th17细胞比例显著高于对照组(n=8,P<0.01),而胸腺中T细胞亚群无明显差异;MGTH患者外周血中Th1/Th17/Tfh细胞比例显著高于TH患者(n=15 vs n=12,P<0.05);低SOCS3表达与术后MG危象的发生相关(HR=3.2,P=0.002)。实验所用关键产品:Active Motif的抗JUND抗体;Thermo Fisher的Protein A/G磁珠;Yeasen的ChIP DNA纯化试剂盒;Jackson Laboratory的CD4Cre Socs3fl/fl小鼠;BD FACS Fortessa流式细胞仪。
3.4 神经突触型胸腺上皮细胞(nsTECs)的鉴定与功能验证
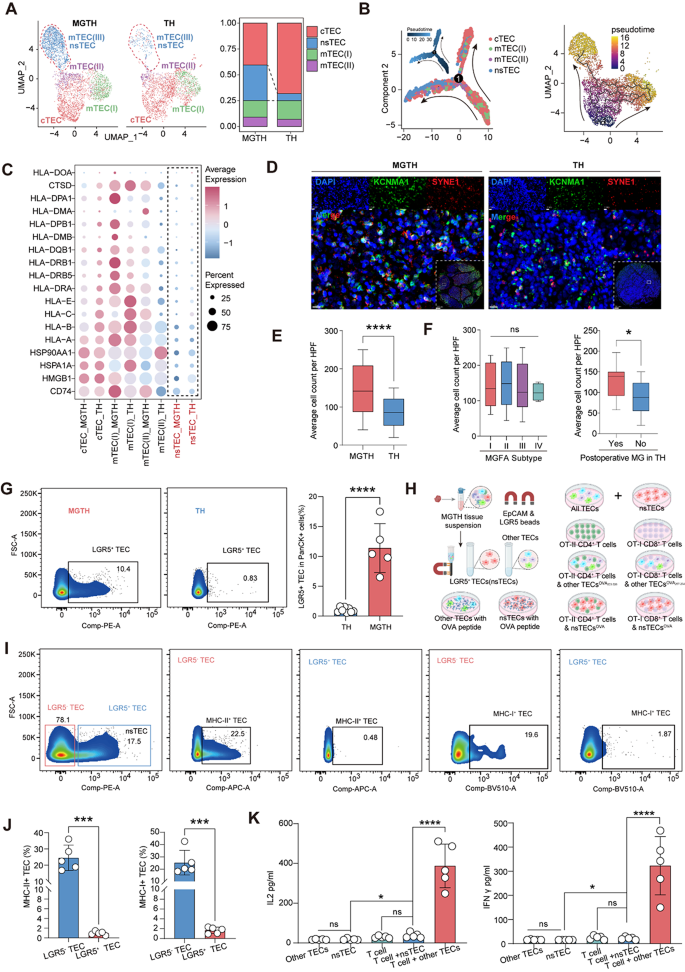
实验目的是明确胸腺上皮细胞在MGTH中的异常变化,验证其抗原呈递功能缺陷。方法细节为对上皮细胞进行重聚类,鉴定特异性富集于MGTH的TEC亚群(nsTECs);通过流式细胞术分析LGR5(nsTECs的表面标记)+TECs的比例;分离LGR5+和LGR5- TECs,检测MHC-I/II的表达;将OVA肽脉冲的TECs与OT-I/OT-II T细胞共培养,通过ELISA检测IL-2(CD4+T细胞激活标志物)和IFN-γ(CD8+T细胞激活标志物)的分泌水平;使用免疫荧光验证nsTECs的标记基因表达。结果解读显示重聚类鉴定出4个TEC亚群,其中nsTECs(mTEC-III)在MGTH中的比例为15.2%(n=10),显著高于TH的3.1%(n=9,P<0.001);nsTECs高表达突触相关基因(如SYNE1、KCNMA1),HLA-I/II表达显著降低(HLA-I表达率:21.3% vs 68.7%,n=5,P<0.001);功能实验显示,LGR5+ TECs与OT-I/OT-II T细胞共培养后,IL-2和IFN-γ的分泌水平显著低于LGR5- TECs(n=3,P<0.01),表明nsTECs的抗原呈递能力缺陷;免疫荧光证实SYNE1和KCNMA1在MGTH中共同表达。实验所用关键产品:Miltenyi Biotec的抗人LGR5微珠;AKOYA Biosciences的Opal多色免疫组化试剂盒;Yeasen的IL-2、IFN-γ ELISA试剂盒;Zeiss LSM 880共聚焦显微镜。
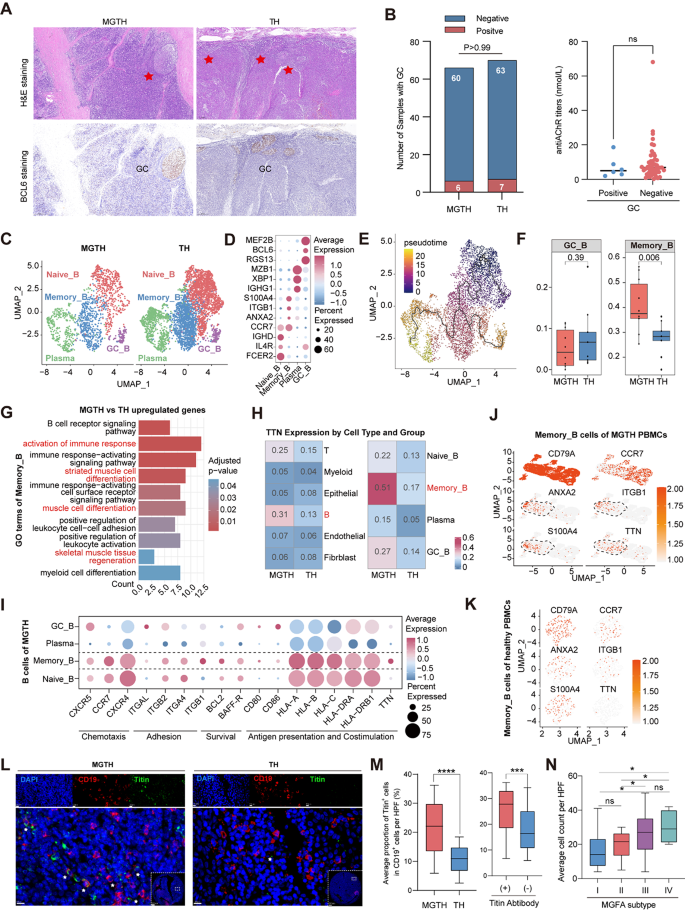
3.5 TTN+记忆B细胞的鉴定与临床关联分析
实验目的是解析B细胞在MGTH中的异常变化,明确其临床意义。方法细节为对B细胞进行重聚类,分析MGTH与TH中B细胞亚群的差异;通过scRNA-seq和免疫荧光检测TTN在B细胞中的表达;检测MGTH和TH患者外周血中的抗titin抗体滴度,分析TTN+记忆B细胞比例与临床指标的相关性。结果解读显示B细胞分为4个亚群( naive B细胞、记忆B细胞、成熟B细胞、生发中心B细胞),MGTH中记忆B细胞的比例显著高于TH(n=10 vs n=9,P<0.05);MGTH中记忆B细胞高表达TTN,TTN+记忆B细胞的比例为22.5%(n=10),显著高于TH的4.7%(n=9,P<0.001);外周血中TTN+记忆B细胞的比例与抗titin抗体滴度正相关(r=0.76,P<0.001),与MGFA严重程度正相关(AUC=0.88,95%CI 0.79-0.97,敏感性83.3%,特异性85.7%);免疫荧光证实MGTH中TTN+B细胞的数量显著高于TH。实验所用关键产品:BD FACS Canto II流式细胞仪;Hangzhou Omumway Medical Laboratory的抗AChR抗体检测试剂盒;AKOYA Biosciences的Opal多色免疫组化试剂盒。
4. Biomarker研究及发现成果解析
本研究中涉及的Biomarker包括分子标志物(JUND、SOCS3)、细胞亚群标志物(nsTECs、TTN+记忆B细胞),筛选与验证逻辑为“多组学筛选→细胞实验验证→动物模型验证→临床样本验证”,形成完整的证据链。
分子标志物JUND和SOCS3通过scRNA-seq筛选出表达差异,经蛋白质组验证,ChIP-qPCR证实调控关系,细胞实验和小鼠模型验证功能,临床样本验证与预后的关联:JUND在MGTH T细胞中的表达水平较TH上调2.1倍(n=10,P<0.05),SOCS3下调1.8倍(n=10,P<0.05),低SOCS3表达与术后MG危象发生的风险比(HR)为3.2(P=0.002)。细胞亚群标志物nsTECs通过scRNA-seq鉴定为MGTH特异性富集的亚群,流式细胞术验证其比例差异(MGTH中15.2% vs TH中3.1%,n=10 vs 9,P<0.001),功能实验证实其抗原呈递缺陷;TTN+记忆B细胞通过scRNA-seq筛选,免疫荧光和流式细胞术验证其在MGTH中的扩增(22.5% vs 4.7%,n=10 vs 9,P<0.001),ROC曲线分析显示其对MG严重程度的预测AUC为0.88(95%CI 0.79-0.97),敏感性83.3%,特异性85.7%,与外周血抗titin抗体滴度正相关(r=0.76,P<0.001)。
核心成果提炼:JUND-SOCS3轴作为T细胞失调的关键调控分子,是MGTH的潜在治疗靶点,SOCS3表达水平可作为术后MG危象的预后标志物;nsTECs是MGTH特异性的胸腺上皮细胞亚群,其抗原呈递缺陷导致中枢耐受破坏,是自身免疫起始的关键位点;TTN+记忆B细胞是MG严重程度的预后标志物,可用于患者分层。本研究的创新性在于首次发现JUND-SOCS3轴在MGTH T细胞中的调控作用,首次鉴定nsTECs这一新型胸腺上皮细胞亚群,首次明确TTN+记忆B细胞在MGTH中的临床意义,为MGTH的精准诊断和治疗提供了新的方向。