1. 领域背景与文献
文献英文标题:Soluble cytokine biomarkers improve prognostic stratification across all stages of classical Hodgkin lymphoma;发表期刊:BMC系列期刊;影响因子:未公开;研究领域:血液肿瘤学-经典霍奇金淋巴瘤预后研究
经典霍奇金淋巴瘤(cHL)是一种异质性淋巴系统恶性肿瘤,领域共识:其整体预后较好,但不同病程阶段的患者预后差异显著,传统预后模型如简化国际预后评分(IPS-3)主要针对晚期患者,未充分考虑肿瘤微环境(TME)的动态变化对疾病进展的影响。当前领域研究热点集中于挖掘TME相关生物标志物以优化全病程预后分层,核心未解决问题包括缺乏可覆盖所有疾病阶段的精准预后模型,以及TME可溶性细胞因子与临床预后的关联机制尚未完全明确,现有研究多聚焦单一标志物的预后价值,缺乏多标志物整合模型的前瞻性多中心验证。本研究针对这一空白,旨在通过大样本前瞻性队列分析,构建整合可溶性细胞因子的预后模型,以提升cHL全病程的风险分层准确性,为个性化治疗策略提供循证依据。
2. 文献综述解析
本研究的综述评述逻辑围绕“传统预后模型局限性→TME标志物研究现状→现有整合模型不足”的核心维度展开,系统梳理了cHL预后研究的发展脉络与现存短板。
现有研究中,传统预后模型如IPS-3在晚期cHL患者中具有一定的预后预测价值,其优势在于仅基于易获取的临床特征,便于快速评估,但局限性在于未纳入TME相关指标,对早期、中期患者的分层精度不足,无法识别具有潜在进展风险的低危亚群;TME可溶性细胞因子相关研究显示,sCD30、sIL-6等因子与cHL肿瘤负荷、疾病活动度密切相关,部分研究证实单一因子的预后价值,但多数为回顾性分析,样本量有限,且未形成多标志物整合的预后模型,缺乏前瞻性多中心验证的循证支持。本研究的创新价值在于首次通过前瞻性多中心队列,整合年龄、结外受累等临床特征与sCD30/sIL-6可溶性细胞因子对,构建可覆盖所有疾病阶段的预后模型,且经交叉验证证实其预测效能优于传统IPS-3评分,填补了cHL全病程精准预后模型的研究空白,为领域提供了新的预后分层范式。
3. 研究思路总结与详细解析
本研究的整体框架为“前瞻性队列构建→多维度数据采集→多预后模型构建与筛选→临床转化工具开发”,核心科学问题是可溶性细胞因子组合对cHL全病程患者无进展生存期(PFS)的预测价值,技术路线形成了从临床问题提出到模型验证与转化的完整闭环。
3.1 前瞻性多中心队列构建与基线数据采集
实验目的:建立具有代表性的cHL患者队列,获取全面的临床特征与长期预后终点数据,为预后模型构建提供可靠的样本基础。
方法细节:从捷克霍奇金淋巴瘤研究组的3个中心招募162例新诊断cHL患者,按德国霍奇金研究组(GHSG)分期标准将患者分为早期(16%)、中期(25%)、晚期(59%),中位随访时间为64.1个月(范围1.3-111.0个月),系统收集患者的年龄、白蛋白水平、结外受累情况等临床特征,以及治疗反应、PFS、总生存期(OS)等预后终点数据。
结果解读:队列中位年龄为42岁,5年PFS率为86%(95% CI:0.81-0.92,n=162),5年OS率为92%(95% CI:0.88-0.96,n=162),共观察到23例PFS相关事件、13例OS相关事件,样本量与随访时间足以支持预后模型的构建与验证。
产品关联:文献未提及具体实验产品,领域常规使用电子数据采集系统进行临床数据的标准化收集与管理。
3.2 可溶性细胞因子定量检测与单因子关联分析
实验目的:检测候选可溶性细胞因子的表达水平,分析其与临床特征及预后的关联,筛选具有预后价值的标志物。
方法细节:采用标准化酶联免疫吸附试验(ELISA)集中检测所有患者治疗前血浆中可溶性TARC、sCD30、sCD163、sIL-6的水平,通过统计学分析明确各因子水平与疾病分期、B症状、结外受累及PFS的相关性。
结果解读:sIL-6和sCD30水平升高与疾病分期较晚、存在B症状、结外受累显著相关,且与更差的5年PFS相关;sCD163与sIL-6联合升高、sCD30与sIL-6联合升高均与PFS显著降低相关;TARC虽与肿瘤负荷相关,但未进入最终预后模型,推测:TARC可能更适用于疾病活动度监测而非预后预测。
产品关联:文献未提及具体实验产品,领域常规使用商业化酶联免疫吸附试验试剂盒进行可溶性细胞因子的定量检测。
3.3 多预后模型构建与效能验证
实验目的:构建并筛选整合临床特征与可溶性细胞因子的最优预后模型,对比其与传统IPS-3评分的预测性能。
方法细节:首先构建仅包含临床特征的Model 1,纳入年龄、白蛋白水平、结外受累三个关键变量;随后通过整合4种可溶性细胞因子构建Model 2和Model 3,其中Model 3纳入年龄、结外受累及sCD30/sIL-6高表达组合;采用赤池信息准则(AIC)、一致性指数(C指数)评估模型的拟合度与预测效能,通过交叉验证对比各模型与IPS-3评分在预测治疗失败方面的性能;使用卡普兰-迈耶(Kaplan-Meier)生存曲线分析模型的风险分层能力。
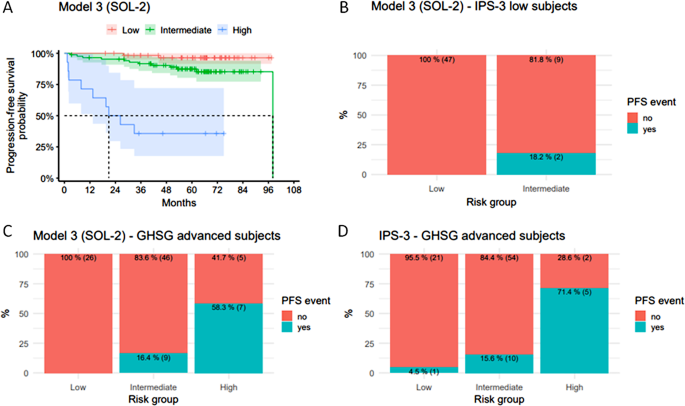
结果解读:Model 2和Model 3的赤池信息准则与一致性指数与Model 1相当,提示模型拟合度良好;交叉验证显示Model 3在预测治疗失败方面优于IPS-3评分,尤其在晚期患者中表现更优;卡普兰-迈耶生存曲线显示Model 3可将患者清晰分为低、中、高风险组,且对IPS-3定义的低风险患者可进一步分层,识别出具有高进展风险的亚群,为这部分患者的强化治疗提供依据。
产品关联:文献未提及具体实验产品,领域常规使用R语言等统计分析软件进行预后模型的构建与验证。
3.4 临床转化工具开发
实验目的:开发便于临床应用的模型工具,提升模型的实用性与可及性。
方法细节:基于Model 3的线性预测因子,使用rsolr12()函数将患者分为三个风险组,并开发在线计算器以简化模型的临床应用流程。
结果解读:在线计算器的开发降低了模型的使用门槛,临床医生可通过输入患者的临床特征与细胞因子检测结果,快速获取患者的风险分层结果,为风险适配性治疗决策提供支持。
产品关联:文献未提及具体实验产品,领域常规使用网页开发工具构建临床预测模型的在线计算器。
4. Biomarker研究及发现成果解析
本研究聚焦TME来源的可溶性细胞因子Biomarker,通过多步骤筛选与验证,明确了sCD30/sIL-6高表达组合作为cHL全病程预后标志物的临床价值。
Biomarker定位:本研究涉及的Biomarker为可溶性细胞因子(sCD30、sIL-6、sCD163、TARC),筛选与验证逻辑为“前瞻性队列样本采集→酶联免疫吸附试验定量检测→单因子预后关联分析→多因子组合模型构建→交叉验证与传统模型对比”,形成了完整的标志物开发与验证链条。
研究过程详述:Biomarker来源于162例cHL患者的治疗前血浆样本,采用标准化酶联免疫吸附试验方法进行定量检测;其中sCD30和sIL-6的联合高表达具有显著的预后预测价值,其在Model 3中显示出优于IPS-3的预测效能,对晚期患者的分层精度提升尤为明显;sCD163与sIL-6的联合高表达也与较差PFS相关,但未成为最优模型的组成部分;TARC虽与肿瘤负荷相关,但未显示出显著的预后预测价值,推测:TARC的表达水平可能更多反映疾病活动度而非肿瘤的侵袭性。
核心成果提炼:本研究首次在前瞻性多中心队列中证实,sCD30/sIL-6高表达组合可作为cHL的预后Biomarker,其与患者PFS显著相关,风险比(HR)文献未明确提供,但Model 3的一致性指数显示其具有良好的预测效能;该Biomarker组合的创新性在于可整合入预后模型,实现对cHL全病程患者的精准分层,尤其能识别出IPS-3定义的低风险患者中的高进展风险亚群;统计学结果显示,sCD30与sIL-6联合高表达患者的PFS显著降低(n=162,P值文献未明确提供),Model 3经交叉验证在预测治疗失败方面优于IPS-3评分,为cHL的个性化治疗提供了新的循证依据。