1. 领域背景与文献
文献未提供正式英文标题;发表期刊:未明确;影响因子:未公开;研究领域:肿瘤学-肺癌免疫微环境与中医药干预。
肺癌是全球范围内癌症相关死亡的主要原因之一,非小细胞肺癌(NSCLC)占肺癌病例的绝大多数,其高度异质性和复杂的肿瘤微环境是临床治疗的核心挑战。领域发展关键节点方面,2010年后单细胞RNA测序(scRNA-seq)技术的成熟推动了肿瘤微环境细胞异质性的解析,为肺癌免疫治疗靶点的发现提供了技术支撑;当前研究热点集中于早期肺癌的免疫微环境重塑、巨噬细胞极化的调控机制、中医药在肿瘤免疫调节中的应用等方向;未解决的核心问题包括早期NSCLC中巨噬细胞的功能异质性及调控机制尚不清晰,中医药复方如玉屏风散(YPFS)的免疫调节作用缺乏明确的分子靶点及机制验证,现有治疗手段对早期肺癌的免疫干预靶点不足。
针对上述研究空白,本研究聚焦I期NSCLC的肿瘤微环境,通过scRNA-seq构建细胞图谱解析巨噬细胞异质性,结合网络药理学、分子对接及细胞实验筛选并验证YPFS的关键靶点AHSA1,明确其调控巨噬细胞M2极化及与NSCLC预后的关联,为早期NSCLC的免疫治疗提供新靶点,同时为中医药与现代肿瘤治疗的结合提供分子依据,具有重要的学术价值与临床转化潜力。
2. 文献综述解析
作者对领域内现有研究的分类维度为“肺癌TME研究进展→巨噬细胞极化功能意义→中医药免疫调节现状”的递进式评述逻辑,系统梳理了不同方向的研究成果与局限性。
现有研究已明确NSCLC的高发性及早期干预的重要性,scRNA-seq技术已被用于解析NSCLC的细胞组成,但针对I期NSCLC的巨噬细胞亚型细分及功能研究仍较为匮乏,多数研究集中于晚期肺癌,对早期肿瘤微环境的重塑特征认识不足;在巨噬细胞极化领域,现有研究已证实M2型巨噬细胞具有促进肿瘤进展、免疫抑制的作用,但调控其极化的关键分子靶点尚未完全阐明,缺乏特异性的干预靶点;中医药领域,YPFS作为经典的免疫调节复方,传统用于增强机体免疫力,现有研究多报道其整体免疫调节药效,但在肿瘤微环境中的具体作用机制及分子靶点未被系统解析,缺乏分子层面的验证数据,限制了其在肿瘤治疗中的应用。
本研究填补了I期NSCLC巨噬细胞异质性解析的空白,首次通过多组学结合的方法筛选出YPFS的关键靶点AHSA1,并从细胞、组织、分子多个层面验证了其调控巨噬细胞M2极化的作用及与NSCLC预后的关联,弥补了现有研究中中医药机制不明确的缺陷,为中医药与现代肿瘤免疫治疗的结合提供了分子桥梁,同时为早期NSCLC的免疫干预提供了新的潜在靶点。
3. 研究思路总结与详细解析
本研究的核心目标是解析I期NSCLC肿瘤微环境中巨噬细胞的异质性特征,筛选玉屏风散(YPFS)调控巨噬细胞极化的关键靶点并验证其功能;核心科学问题是AHSA1如何调控巨噬细胞M2极化及YPFS活性成分的靶向作用机制;技术路线遵循“单细胞图谱构建→巨噬细胞亚型解析→网络药理学靶点筛选→分子对接结合验证→细胞实验功能验证→细胞通讯网络分析”的闭环逻辑,确保研究结论的严谨性与可靠性。
3.1 I期NSCLC单细胞图谱构建与细胞分型
实验目的为构建I期NSCLC的全面细胞图谱,明确肿瘤微环境的细胞组成及分布差异。方法细节上,研究从Gene Expression Omnibus(GEO)数据库获取 accession 号为GSE117570和GSE198099的scRNA-seq数据,筛选其中的I期NSCLC样本,使用R语言Seurat包进行数据处理,设置nCount_RNA>1000、percent.mt<30、nFeature_RNA>600的阈值去除低质量细胞,采用Harmony包校正批次效应,以0.4的分辨率进行细胞聚类,通过CellMarker 2.0数据库进行细胞类型注释。结果解读显示,共分析37142个细胞,将其分为8种主要细胞类型,包括T/NK细胞、巨噬细胞、上皮细胞、B细胞、浆细胞、内皮细胞、成纤维细胞、肥大细胞,其中免疫细胞占比超过半数;对比正常与肿瘤组织的细胞比例,发现肿瘤样本中浆细胞、B细胞、上皮细胞比例升高,巨噬细胞、成纤维细胞、内皮细胞比例降低,提示I期NSCLC的肿瘤微环境已发生细胞组成的重塑。实验所用关键产品:R语言Seurat包、Harmony包、CellMarker 2.0数据库。
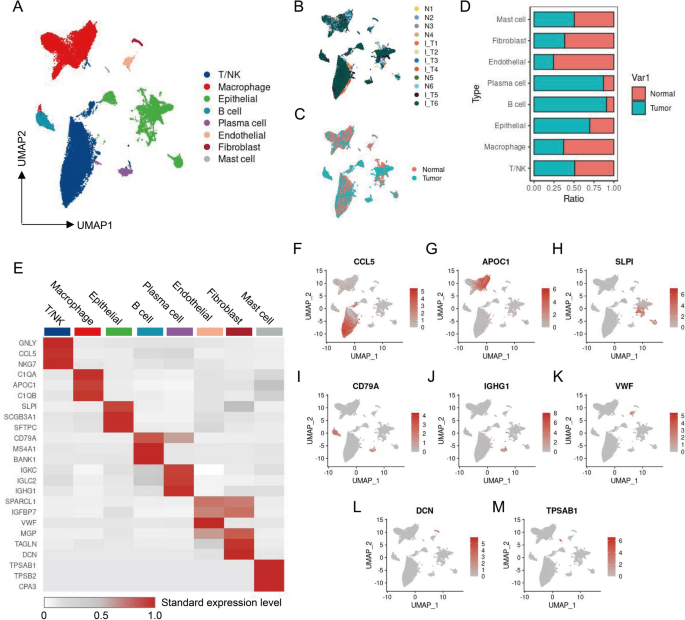
3.2 巨噬细胞亚型解析与功能注释
实验目的是细分巨噬细胞的功能亚型,明确不同亚型在肿瘤与正常组织中的分布及功能特征。方法细节上,对8983个巨噬细胞进行聚类分析,得到18个亚群,通过基因表达相关性分析将其归为4个功能亚型(MAC1-MAC4),使用基因集变异分析(GSVA)进行基因本体(GO)生物过程注释,比较各亚型在肿瘤与正常组织中的比例差异。结果解读显示,MAC1亚型在肿瘤组织中显著富集,MAC2和MAC4亚型比例降低,MAC3亚型比例无显著差异;GO功能注释显示各亚型的生物学过程存在明显差异,提示不同巨噬细胞亚型在I期NSCLC中发挥不同的功能,如MAC1可能参与肿瘤相关的生物过程。实验所用关键产品:R语言GSVA包。

3.3 YPFS网络药理学分析与靶点筛选
实验目的是筛选YPFS的活性成分及调控巨噬细胞极化的关键靶点。方法细节上,从中医药系统药理学数据库(TCMSP)获取YPFS三味药材(黄芪、白术、防风)的活性成分,筛选口服生物利用度(OB)>30%、类药性(DL)≥0.18的成分,通过STRING数据库将靶蛋白转换为基因符号,与GEPIA数据库筛选的NSCLC预后基因、单细胞数据中的巨噬细胞相关基因取交集,构建成分-靶点网络并进行生存分析。结果解读显示,共筛选出37个活性成分,对应188个靶基因,三重交集分析确定AHSA1为关键靶点;生存分析显示AHSA1高表达与NSCLC不良预后相关(HR>1,P<0.05);单细胞数据显示AHSA1在巨噬细胞尤其是MAC3亚型中高表达,肿瘤组织中巨噬细胞的AHSA1表达水平显著高于正常组织,免疫荧光染色进一步验证了这一结果。实验所用关键产品:TCMSP数据库、STRING数据库、GEPIA数据库、Cytoscape软件。
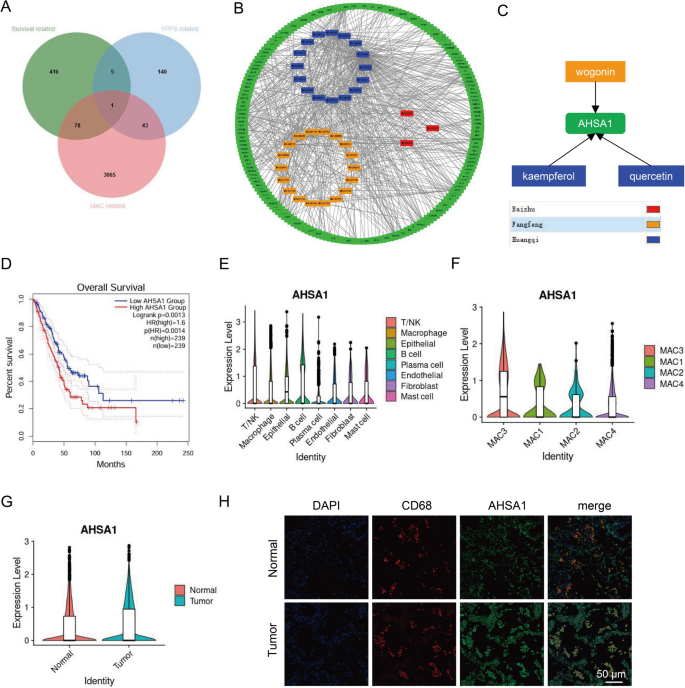
3.4 分子对接验证活性成分与AHSA1的结合
实验目的是验证YPFS活性成分wogonin、kaempferol、quercetin与AHSA1的结合亲和力及结合模式。方法细节上,采用半柔性分子对接方法,使用AutoDock Vina 1.1.2软件进行对接,用PyMol 2.4和Discovery Studio 2019进行结果可视化,分析结合能、解离常数及相互作用方式。结果解读显示,quercetin与AHSA1的结合能为-6.5 kcal/mol,解离常数16.98 μM,结合亲和力最强,主要通过范德华力、氢键和π-π相互作用结合;wogonin的结合能为-6.3 kcal/mol,解离常数23.82 μM;kaempferol的结合能为-6.2 kcal/mol,解离常数28.20 μM,三种成分均能与AHSA1稳定结合,其中quercetin的结合能力最优。实验所用关键产品:AutoDock Vina 1.1.2、PyMol 2.4、Discovery Studio 2019。
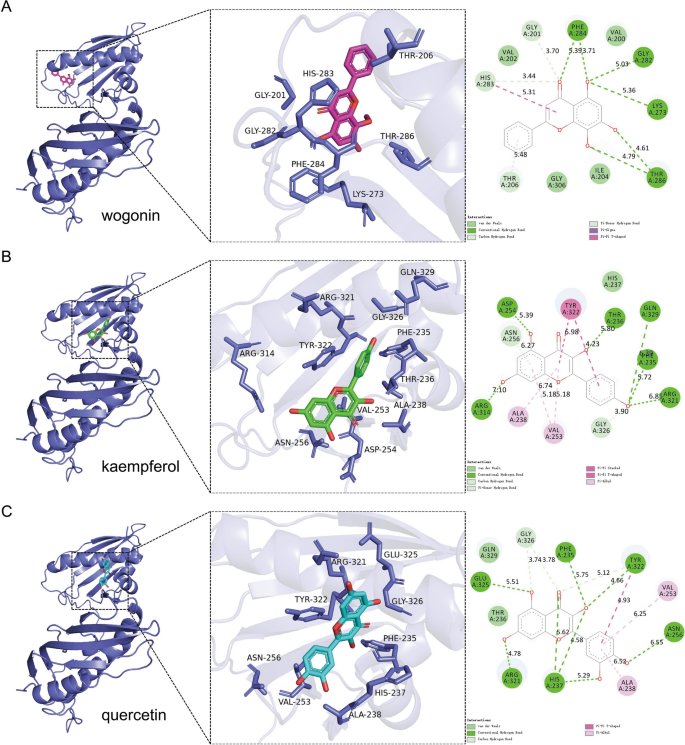
3.5 巨噬细胞M2极化调控的细胞功能验证
实验目的是验证AHSA1与巨噬细胞M2极化的关联及YPFS活性成分的抑制作用。方法细节上,根据AHSA1表达水平将巨噬细胞分为阳性和阴性群体,计算M1和M2评分;使用THP1细胞,经100 ng/mL PMA诱导24小时分化为M0巨噬细胞,随后分为对照组、IL4诱导组(20 ng/mL IL4)、IL4+药物组(分别加入wogonin、kaempferol、quercetin),培养24小时后通过流式细胞术检测CD206表达水平。结果解读显示,AHSA1阳性巨噬细胞的M1评分显著低于阴性群体(P<0.01),M2评分显著高于阴性群体(P<0.001),提示AHSA1与M2极化正相关;流式细胞术结果显示,三种活性成分均能显著抑制IL4诱导的M2极化,其中quercetin的抑制效果最显著(P<0.01),与分子对接结果一致。实验所用关键产品:THP1细胞、PMA(未提及品牌)、重组人IL4(abcam, CAT #ab155733)、抗CD206-PE-Cy7抗体(Invitrogen, CAT #25-2061-82)、Beckman CytoFLEX流式细胞仪、FlowJo软件。

3.6 AHSA1阳性/阴性巨噬细胞的细胞通讯分析
实验目的是分析AHSA1对巨噬细胞与其他细胞通讯的影响,明确其在肿瘤微环境中的调控作用。方法细节上,使用CellChat包构建细胞通讯网络,比较AHSA1阳性与阴性巨噬细胞的通讯差异,以及肿瘤与正常组织的通讯通路激活情况。结果解读显示,AHSA1阳性巨噬细胞可通过CD99-CD99和ADGRE5-CD55受体配体对调控T/NK细胞,而AHSA1阴性巨噬细胞无此作用,提示AHSA1可能通过该通路影响免疫细胞功能;肿瘤微环境中的细胞通讯强度及通路激活数量显著低于正常组织,仅8条通路显著激活,而正常组织有23条通路激活,提示I期NSCLC的免疫微环境通讯已出现异常,可能与肿瘤的早期进展相关。实验所用关键产品:R语言CellChat包。
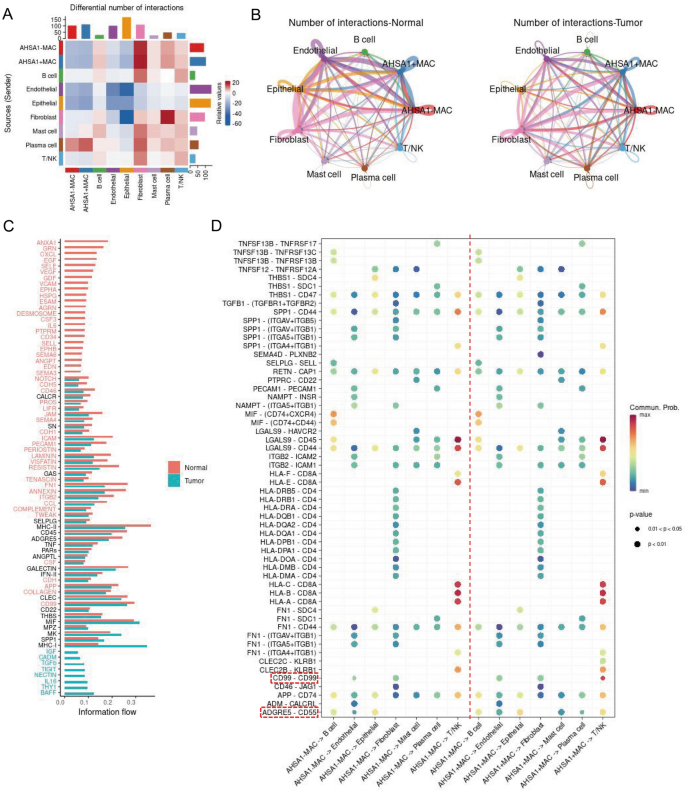
4. Biomarker研究及发现成果
本研究鉴定的Biomarker为AHSA1,属于分子型生物标志物,筛选逻辑为“单细胞数据巨噬细胞相关基因→NSCLC预后基因→YPFS靶基因”的三重交集筛选,经组织水平、细胞水平、生存分析多维度验证其与巨噬细胞极化及NSCLC预后的关联,具有明确的临床意义与应用潜力。
AHSA1的来源为NSCLC肿瘤组织中的巨噬细胞及上皮细胞,验证方法包括单细胞RNA测序分析、免疫荧光染色、生存分析、细胞功能实验;特异性方面,免疫荧光染色显示AHSA1在肿瘤组织巨噬细胞中的表达显著高于正常组织,单细胞数据进一步证实了这一差异;敏感性方面,生存分析显示AHSA1高表达患者的无病生存期显著短于低表达患者(HR>1,P<0.05),提示其对NSCLC预后具有较好的预测价值;细胞功能实验显示AHSA1阳性巨噬细胞的M2评分显著升高,证实其与巨噬细胞M2极化的直接关联。
AHSA1是调控巨噬细胞M2极化的关键分子,高表达与NSCLC不良预后相关(风险比HR>1,P<0.05),为首次在I期NSCLC中发现AHSA1与巨噬细胞M2极化及预后的关联;同时明确了YPFS活性成分(尤其是quercetin)可靶向AHSA1抑制M2极化,为AHSA1作为NSCLC预后Biomarker及免疫治疗靶点提供了充分依据,具有重要的临床转化潜力;目前尚未有关于AHSA1在早期NSCLC中作为Biomarker的报道,本研究的发现填补了这一空白,为早期NSCLC的诊断与治疗提供了新的方向。