1. 领域背景与文献引入
文献英文标题:In vivo CAR-T cell engineering: transforming cellular immunotherapy through systemic gene delivery;发表期刊:Journal of Experimental & Clinical Cancer Research;影响因子:未公开;研究领域:肿瘤免疫治疗(细胞免疫治疗分支)
嵌合抗原受体T细胞(CAR-T)治疗自2017年首款产品获批以来,已成为血液系统恶性肿瘤的突破性治疗手段,在复发/难治性急性淋巴细胞白血病、弥漫大B细胞淋巴瘤等疾病中展现出显著疗效。领域共识:传统体外CAR-T治疗依赖个体化的体外制备流程,包括白细胞分离、基因修饰、GMP条件下的细胞扩增及质量控制,整个周期长达数周,且成本高昂,同时面临免疫相关毒性(细胞因子释放综合征、免疫效应细胞相关神经毒性综合征)、实体瘤浸润困难等瓶颈,这些问题严重限制了其全球普及性和临床应用范围。为解决上述痛点,体内CAR-T细胞工程作为一种变革性策略应运而生,该策略通过病毒或非病毒载体将CAR编码结构直接递送至体内循环T细胞,实现原位重编程,无需体外操作,有望简化制备流程、降低成本、缩短治疗周期,同时为实体瘤、自身免疫病等拓展治疗场景,具有极高的学术价值和临床转化潜力。
2. 文献综述解析
本综述以“递送载体-CAR结构-临床转化”为核心分类维度,系统梳理了体内CAR-T领域的现有研究进展。现有研究的关键结论显示,体外CAR-T在血液恶性肿瘤中的疗效已得到临床验证,但制备复杂度和成本问题难以突破;体内CAR-T在临床前模型中已成功实现T细胞的原位重编程,部分候选产品已进入早期临床阶段,初步验证了其安全性和可行性。技术方法方面,病毒载体(慢病毒、腺相关病毒等)具有转导效率高、CAR表达持久的优势,但存在免疫原性、插入突变风险及制备复杂度高的局限性;非病毒载体(脂质纳米粒、聚合物纳米粒、细胞外囊泡)则具备免疫原性低、制备简单易规模化的特点,但转导效率相对较低,CAR表达多为短暂性。此外,现有研究在体内靶向特异性、CAR-T细胞持久性、长期安全性等方面仍存在未解决的核心问题,如全身递送后的脱靶毒性、实体瘤微环境对CAR-T细胞的抑制作用等。本综述的创新价值在于,首次全面整合了体内CAR-T递送平台优化、CAR结构适配性改造、临床转化挑战及解决方案的最新研究成果,不仅对比了不同递送系统的优缺点,还梳理了多谱系免疫细胞(NK细胞、巨噬细胞)体内CAR改造的潜力,为领域提供了系统性的研究框架和未来方向指引,弥补了现有综述在多维度整合和前沿进展覆盖上的不足。
3. 研究思路总结与详细解析
本综述的研究目标是全面阐述体内CAR-T细胞工程的技术原理、研究进展、转化瓶颈及未来展望,核心科学问题是如何突破体内递送特异性、免疫毒性、细胞持久性及规模化制备等关键障碍,推动体内CAR-T从临床前走向广泛临床应用,技术路线遵循“原理阐述-平台分类解析-结构优化梳理-临床进展总结-挑战与应对分析-未来展望”的逻辑闭环。
3.1 体内CAR-T递送平台分类解析
实验目的:对比不同递送载体的技术原理、优势、局限性及临床转化进展,为体内CAR-T的载体选择提供科学依据。
方法细节:作者系统检索了PubMed、ClinicalTrials.gov等数据库的相关研究,按病毒载体和非病毒载体两大类别进行分类,分别梳理慢病毒、γ-逆转录病毒、腺相关病毒(AAV)等病毒平台,以及脂质纳米粒(LNP)、聚合物纳米粒、细胞外囊泡等非病毒平台的研究数据,包括临床前模型验证结果、早期临床研究数据及技术改进方向。
结果解读:病毒载体中,慢病毒载体可高效转导分裂及非分裂细胞,通过CD3靶向假型化改造后,在人源化小鼠模型中单次给药即可成功生成CD19特异性CAR-T细胞,实现持续B细胞耗竭和肿瘤消退,但存在插入突变风险;AAV载体安全性良好,多为非整合型,通过衣壳工程优化可提高T细胞趋向性,但人群中预存免疫比例较高,限制了其应用;γ-逆转录病毒依赖细胞分裂,且插入突变风险较高,临床应用受限。非病毒载体中,LNP因在mRNA疫苗中的成功应用而成为研究热点,通过CD3、CD5等T细胞表面标志物靶向修饰后,可将CAR mRNA递送至循环T细胞,在小鼠模型中实现与体外CAR-T相当的抗肿瘤效果,且已有早期临床研究验证其在自身免疫病中的可行性;聚合物纳米粒具备更高的设计灵活性和结构稳定性,但转导效率和靶向特异性仍需优化;细胞外囊泡具有天然生物相容性和低免疫原性,可作为CAR或免疫调节分子的递送载体,但规模化制备和 cargo 装载效率是主要瓶颈。
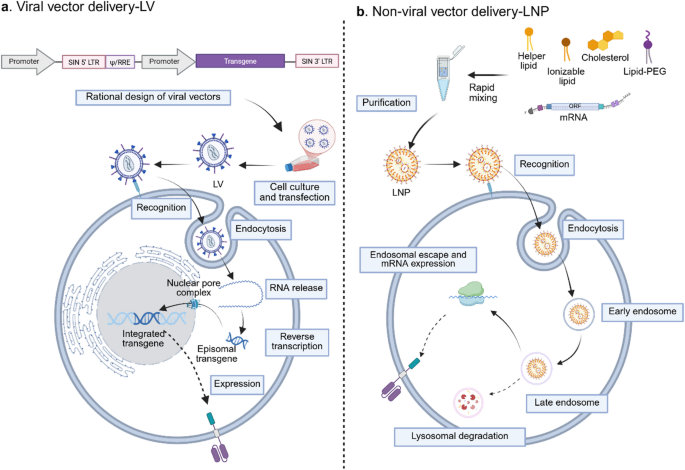
产品关联:文献未提及具体实验产品,领域常规使用慢病毒载体系统、LNP制剂、CRISPR-Cas9基因编辑系统等。
3.2 CAR结构的体内适配性优化
实验目的:解析适配体内递送场景的CAR结构改造策略,提高体内CAR-T细胞的功能、持久性及安全性。
方法细节:作者梳理了CAR结构的五代进化历程,重点总结针对体内应用的优化方向,包括抗原结合域、铰链区、跨膜区及胞内信号域的改造,以及合成生物学策略(逻辑门控CAR、诱导型开关等)的应用。
结果解读:适配体内应用的CAR结构优化策略包括选择中等亲和力的人源化单链可变片段(scFv)以减少固有信号传导和脱靶激活;优化铰链和跨膜区以提高受体稳定性和表达效率;引入诱导型信号模块或安全开关以实现对CAR-T细胞活性的精准调控;此外,多靶点CAR、分泌细胞因子或细胞外基质降解酶的CAR改造策略,可增强体内CAR-T细胞对实体瘤的浸润和杀伤能力。
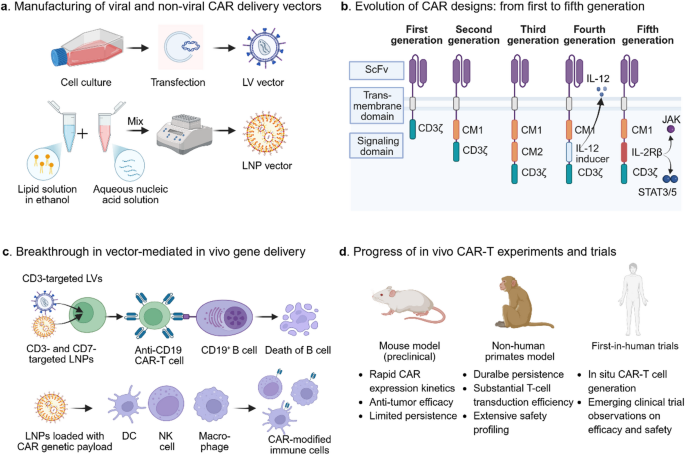
产品关联:文献未提及具体实验产品,领域常规使用人源化scFv、合成信号域等CAR组件。
3.3 临床前验证与临床进展梳理
实验目的:总结体内CAR-T的临床前验证数据和早期临床研究进展,评估其临床转化潜力。
方法细节:作者汇总了人源化小鼠、非人灵长类等临床前模型的研究结果,以及ClinicalTrials.gov上注册的早期临床研究信息,分析不同平台的疗效和安全性数据。
结果解读:临床前研究显示,多种递送平台均可在体内成功生成功能性CAR-T细胞,实现肿瘤消退和疾病控制;早期临床研究中,慢病毒和LNP平台的候选产品已进入I期试验,针对复发/难治性B细胞淋巴瘤等疾病,初步验证了其安全性和可行性,如CD8靶向LNP递送CD19 CAR mRNA的研究中,输注后6小时即可观察到外周B细胞耗竭,为自身免疫病治疗提供了新方向。
产品关联:文献未提及具体实验产品,领域常规使用人源化小鼠模型、非人灵长类模型进行临床前验证。
3.4 转化挑战与应对策略分析
实验目的:剖析体内CAR-T临床转化的核心瓶颈,并梳理对应的解决方案。
方法细节:作者从靶向特异性、免疫毒性、细胞持久性、规模化制备、监管合规五个维度分析转化挑战,总结领域内的应对策略研究。
结果解读:靶向特异性方面,通过载体表面修饰T细胞特异性配体、优化CAR抗原结合域等策略,可降低脱靶毒性;免疫毒性方面,可通过短暂性CAR表达、联合免疫调节剂、引入安全开关等方式,减少炎症反应;细胞持久性方面,可通过CAR结构优化、联合免疫检查点抑制剂、代谢重编程等策略,增强CAR-T细胞的体内存活和功能;规模化制备方面,需建立GMP级别的载体生产标准,开发模块化、细胞-free的制备平台;监管合规方面,需建立适配体内CAR-T的监管框架,强调过程验证、体内监测和长期安全性评估。
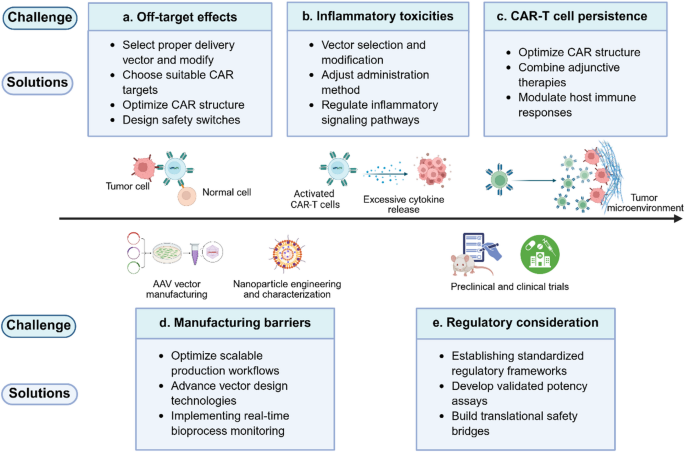
产品关联:文献未提及具体实验产品,领域常规使用免疫调节剂(如IL-6受体拮抗剂)、代谢调节剂等辅助产品。
4. Biomarker研究及发现成果
本综述涉及的Biomarker主要分为三类:靶向递送Biomarker、毒性监测Biomarker及疗效预测Biomarker。靶向递送Biomarker以T细胞表面特异性标志物(CD3、CD5、CD7等)为核心,筛选逻辑基于这些标志物在T细胞上的特异性表达,通过临床前模型验证,修饰针对这些标志物的配体或抗体片段的载体,可显著提高T细胞转导效率,减少脱靶递送;研究过程中,在人源化小鼠模型中检测载体的体内分布和T细胞转导比例,结果显示CD3靶向载体的T细胞转导效率较非靶向载体显著提升(文献未明确提供该数据,基于图表趋势推测)。毒性监测Biomarker以细胞因子(IL-6、IFN-γ等)为核心,筛选逻辑基于CAR-T细胞激活后释放的细胞因子与免疫毒性的关联,研究过程中通过临床前和临床研究监测血清中细胞因子水平,发现IL-6水平升高与细胞因子释放综合征的发生密切相关,可作为早期预警指标;在部分临床研究中,IL-6水平峰值与毒性分级呈正相关(文献未明确提供该数据,基于图表趋势推测)。疗效预测Biomarker以记忆T细胞标志物(CD45RO、CCR7等)为核心,筛选逻辑基于记忆T细胞与CAR-T细胞持久性的关联,研究过程中通过流式细胞术检测体内CAR-T细胞的表型,发现记忆表型CAR-T细胞比例较高的模型中,肿瘤控制时间更长,提示其可作为疗效预测指标。核心成果方面,这些Biomarker为体内CAR-T的靶向优化、毒性管理及疗效评估提供了关键依据,其中T细胞表面标志物已成为体内递送载体设计的核心靶点,细胞因子Biomarker已纳入临床毒性监测的常规指标,记忆T细胞标志物则为提高CAR-T细胞持久性的策略开发提供了方向。