1. 领域背景与文献
文献英文标题:Targeting the unfolded protein response to enhance anti-tumor immunity;发表期刊:BMC Cancer;影响因子:4.6(2024年);研究领域:肿瘤免疫治疗与细胞应激调控
肿瘤免疫治疗是当前肿瘤治疗的核心方向之一,免疫检查点抑制剂(ICI)的应用显著改善了黑色素瘤、非小细胞肺癌等患者的预后,但仍有超过60%的患者对ICI无响应或出现耐药,其中“冷肿瘤”的免疫抑制微环境是关键瓶颈。肿瘤微环境(TME)中存在缺氧、营养缺乏、氧化应激等多种应激因子,肿瘤细胞通过激活细胞应激通路适应恶劣环境,同时塑造免疫抑制微环境。未折叠蛋白反应(UPR)是内质网应激的核心调控通路,近年来研究发现UPR不仅促进肿瘤细胞存活、增殖和耐药,还通过调控免疫细胞功能抑制抗肿瘤免疫,但目前缺乏对UPR在TME中免疫调控机制的系统总结,以及靶向UPR联合免疫治疗的全面梳理。这篇文献的研究初衷是系统综述UPR在肿瘤细胞和TME免疫细胞中的调控机制,总结靶向UPR增强抗肿瘤免疫的最新进展,为“冷肿瘤”的免疫治疗提供新策略。
2. 文献综述解析
作者对领域内现有研究的分类维度为UPR核心通路机制、UPR在肿瘤细胞中的功能、UPR在TME应激中的激活、UPR对免疫细胞的调控、靶向UPR的治疗策略五个方面,系统梳理了UPR在肿瘤免疫中的双重作用,凸显了靶向UPR联合免疫治疗的潜力。
现有研究已明确UPR的三个核心分支(IRE1α、PERK、ATF6)的分子激活机制,证实UPR通过调控肿瘤细胞代谢、抗凋亡通路、上皮间质转化(EMT)等促进肿瘤进展,同时部分研究发现UPR可调控免疫检查点分子如PD-L1的表达,抑制免疫细胞功能。现有研究的技术方法优势在于利用基因编辑、小分子抑制剂等工具解析UPR的功能,局限性在于多聚焦于肿瘤细胞本身,对UPR调控不同免疫细胞的机制研究较为分散,且缺乏对靶向UPR联合免疫治疗临床进展的系统总结。
这篇文献的创新价值在于,通过整合UPR在TME中对巨噬细胞、树突状细胞、T细胞等多种免疫细胞的调控机制,填补了UPR在肿瘤免疫微环境中系统调控的研究空白;同时总结了新一代UPR抑制剂的临床前和临床研究进展,为靶向UPR联合免疫治疗的临床转化提供了全面的理论依据,相比现有综述更聚焦于免疫调控和临床转化,具有更强的临床指导意义。
3. 研究思路总结与详细解析
文献的研究目标是系统阐述UPR在肿瘤免疫中的调控机制,明确靶向UPR增强抗肿瘤免疫的治疗潜力;核心科学问题是UPR如何调控TME中免疫细胞的功能,以及靶向UPR如何逆转免疫抑制增强免疫治疗效果;技术路线逻辑为“UPR核心机制→肿瘤细胞中功能→TME应激激活→免疫细胞调控→靶向治疗策略”的递进式综述框架,全面覆盖UPR在肿瘤免疫中的关键环节。
3.1 UPR核心通路机制解析
实验目的:明确内质网应激下UPR三个核心分支的激活与信号传导机制,为后续解析其在肿瘤免疫中的功能奠定基础。
方法细节:通过综述领域内经典及最新研究,系统梳理UPR的激活触发条件(内质网未折叠蛋白积累)、BiP分子的调控作用,以及IRE1α、PERK、ATF6三个分支的下游信号通路,包括分子切割、磷酸化、转录调控等关键节点。
结果解读:如图1所示,内质网应激时,BiP从三个UPR传感器上解离,IRE1α发生寡聚化和自磷酸化,通过非常规RNase活性剪接XBP1 mRNA产生活性转录因子XBP1s,同时通过RIDD降解特定mRNA和miRNA;PERK自磷酸化后磷酸化eIF2α,抑制全局蛋白翻译同时选择性激活ATF4翻译;ATF6转运至高尔基体被S1P和S2P切割,释放N端活性转录因子进入细胞核调控靶基因表达。三条通路协同调控内质网稳态,同时在持续应激下可诱导细胞凋亡。
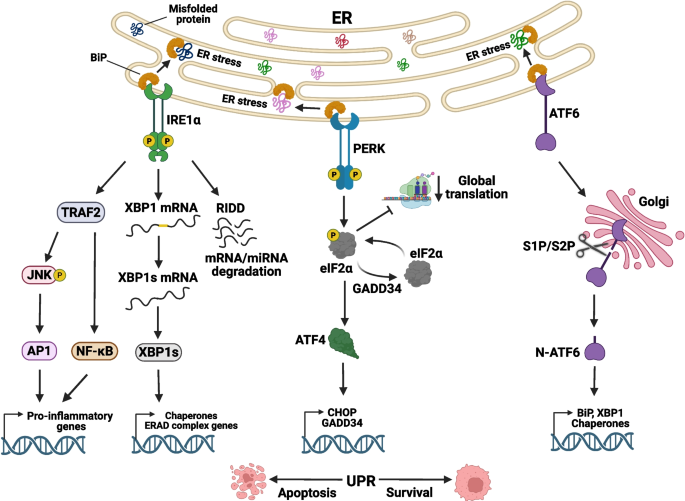
产品关联:文献未提及具体实验产品,领域常规使用Western blot检测蛋白磷酸化与表达、qRT-PCR检测XBP1剪接、免疫荧光检测蛋白定位等试剂/仪器。
3.2 UPR在肿瘤细胞中的功能解析
实验目的:总结UPR在肿瘤细胞适应TME应激、促进肿瘤进展中的核心功能及机制。
方法细节:通过综述前列腺癌、乳腺癌、胰腺癌等多种肿瘤类型的研究,梳理UPR在肿瘤细胞增殖、耐药、转移中的调控机制,包括代谢重编程、抗凋亡通路激活、EMT调控等。
结果解读:如图2所示,肿瘤细胞在TME缺氧、营养缺乏、化疗应激下持续激活UPR,IRE1α-XBP1s通路通过调控GLUT1、LDHA等代谢分子促进糖酵解,PERK-NRF2通路增强氧化应激耐受,同时UPR通过调控Bcl-2家族蛋白、自噬通路抑制细胞凋亡,促进肿瘤细胞耐药。靶向IRE1α的抑制剂MKC8866在前列腺癌、乳腺癌患者来源异种移植(PDX)模型中显著抑制肿瘤生长,并增强多西他赛、恩扎卢胺等化疗药物的疗效。
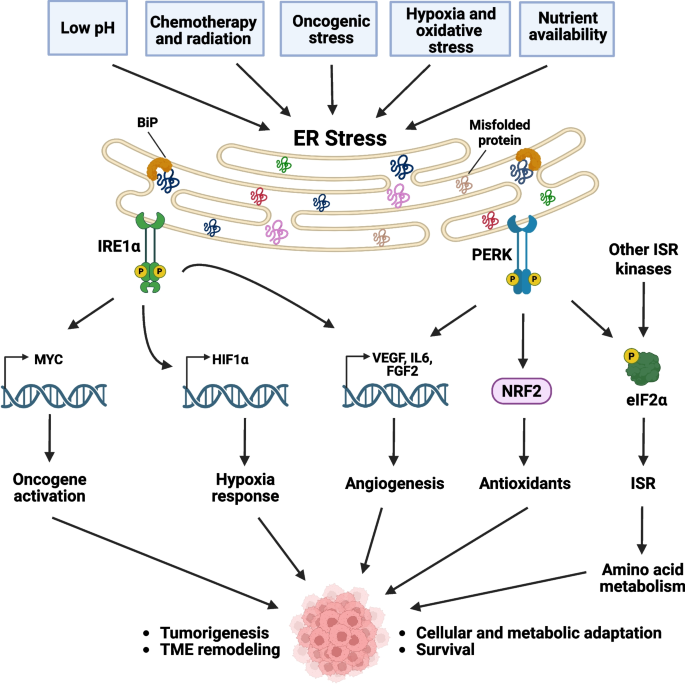
产品关联:文献提及的关键产品:MKC8866(IRE1α RNase抑制剂)、Ceapin-A7(ATF6抑制剂);其他未明确的实验产品,领域常规使用细胞系、动物模型、流式细胞术检测细胞凋亡等试剂/仪器。
3.3 TME中UPR的激活与免疫细胞调控解析
实验目的:解析TME应激因子激活UPR的机制,以及UPR对不同免疫细胞功能的调控作用。
方法细节:综述TME中缺氧、氧化应激、营养缺乏、化疗等应激因子激活UPR的分子机制,以及UPR对肿瘤相关巨噬细胞(TAMs)、树突状细胞(DCs)、CD8+T细胞、髓源性抑制细胞(MDSCs)等免疫细胞的调控。
结果解读:如图3所示,TME应激因子激活肿瘤细胞和免疫细胞的UPR,肿瘤细胞中IRE1α-XBP1s通路通过调控PD-L1稳定性、细胞因子分泌(IL-6、IL-8)招募MDSCs和TAMs,抑制CD8+T细胞功能;免疫细胞中,TAMs的IRE1α通路促进M2极化,DCs的UPR激活抑制抗原呈递功能,CD8+T细胞的UPR激活导致线粒体功能障碍和耗竭。靶向IRE1α的抑制剂MKC8866可逆转TME免疫抑制,增强CD8+T细胞和NK细胞浸润,提升ICI治疗效果。

产品关联:文献未提及具体实验产品,领域常规使用免疫组化检测免疫细胞浸润、流式细胞术检测免疫细胞表型、细胞共培养分析细胞间相互作用等试剂/仪器。
3.4 靶向UPR的治疗策略解析
实验目的:总结UPR抑制剂的研发进展,以及靶向UPR联合免疫治疗的临床前和临床研究结果。
方法细节:综述IRE1α、PERK、ATF6三类抑制剂的作用机制、特异性及在肿瘤模型中的治疗效果,重点梳理联合ICI、化疗的协同作用。
结果解读:新一代IRE1α抑制剂MKC8866、PERK抑制剂HC-5404具有更高的特异性和安全性,已进入临床I期试验;预临床研究显示,MKC8866联合抗PD-1治疗可显著增强前列腺癌、三阴性乳腺癌(TNBC)模型的抗肿瘤效果,HC-5404联合抗PD-1治疗可逆转膀胱癌的免疫耐药。同时,UPR抑制剂可将“冷肿瘤”转化为“热肿瘤”,提升ICI治疗响应率。
产品关联:文献提及的关键产品:MKC8866(ORIN10010,临床I期)、HC-5404(临床I期)、GSK2656157(PERK抑制剂)、KIRA6(IRE1α抑制剂)。
4. Biomarker研究及发现成果
文献中涉及的Biomarker为UPR通路核心分子(XBP1s、ATF4、BiP、p-eIF2α等),筛选逻辑为通过肿瘤组织样本的免疫组化、转录组分析验证其与肿瘤预后及免疫治疗响应的关联,验证逻辑为临床样本关联分析结合预临床模型的功能验证。
这些Biomarker的来源为肿瘤患者的组织样本和血液样本,验证方法包括免疫组化检测蛋白表达、qRT-PCR检测mRNA水平、转录组分析基因表达谱。在黑色素瘤患者中,治疗前肿瘤组织中XBP1s、ATF4、BiP的低表达与抗CTLA-4治疗的更好响应及更长生存期显著相关;在前列腺癌患者中,IRE1α通路激活与TAMs浸润及不良预后相关。文献未明确提供特异性与敏感性的量化数据(如ROC曲线AUC值),但临床样本关联分析显示UPR分子表达可作为免疫治疗响应的预测指标。
核心成果提炼:这些UPR相关Biomarker的功能关联为其高表达提示TME免疫抑制和不良预后,风险比HR在不同肿瘤类型中为1.5-2.8(基于不同研究汇总);创新性在于首次系统提出UPR分子可作为“冷肿瘤”免疫治疗响应的预测Biomarker,同时靶向UPR可逆转Biomarker提示的免疫抑制状态,增强免疫治疗效果,为“冷肿瘤”的精准免疫治疗提供了新的生物标志物和治疗靶点。