1. 领域背景与文献引入
文献英文标题:Targeting neoantigens for cancer immunotherapy;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗、精准医学
癌症是全球第二大致死疾病,传统治疗手段(手术、放疗、化疗)直接作用于肿瘤细胞,但对晚期癌症的疗效有限。近十年癌症免疫治疗取得突破性进展,通过激活宿主免疫系统杀伤肿瘤,核心技术包括免疫检查点抑制剂(如PD-1/PD-L1抗体)、过继细胞治疗(如CAR-T、TCR-T)等。领域共识:肿瘤抗原是免疫治疗的核心,T细胞通过识别主要组织相容性复合体(MHC)呈递的肿瘤抗原发挥杀伤作用。目前肿瘤抗原分为三类:肿瘤相关抗原(TAAs)、致癌病毒抗原和新抗原(TSAs),其中TAAs因在正常组织低表达易引发免疫耐受,致癌病毒抗原仅适用于病毒相关癌症,而新抗原由肿瘤体细胞突变产生,仅在肿瘤细胞表达,具有高特异性和低脱靶毒性,成为精准免疫治疗的热点。但当前领域仍存在核心问题:新抗原预测算法准确性不足,大量预测的新抗原无免疫原性;个性化新抗原制备周期长达6-8周,难以满足晚期患者的治疗需求;新抗原疗法与其他治疗的联合方案尚未优化,临床反应率有待提升。在此背景下,本文系统总结新抗原的鉴定技术、治疗策略及临床试验进展,为新抗原免疫治疗的优化和推广提供全面参考。
2. 文献综述解析
本文综述的核心评述逻辑为“癌症免疫治疗背景铺垫→肿瘤抗原分类与新抗原特性解析→新抗原鉴定技术梳理→各类新抗原疗法特性分析→临床试验结果总结→未来挑战与方向展望”,按肿瘤抗原类型、治疗技术路线的维度对现有研究进行分类整合。
现有研究的关键结论显示,肿瘤相关抗原如HER2、NY-ESO-1已用于免疫治疗,但因存在免疫耐受,临床疗效有限;致癌病毒抗原如HPV、EBV相关疫苗在病毒相关癌症中显示出预防和治疗潜力,但适用范围较窄;新抗原具有严格的肿瘤特异性,能诱导CD4+和CD8+T细胞的协同免疫反应,且可形成记忆T细胞,实现长期抗肿瘤保护。技术方法层面,高通量测序(全外显子测序WES、转录组测序RNA-seq)结合生物信息学算法可实现新抗原的大规模预测;不同新抗原疗法各有优势,如合成长肽(SLP)疫苗能同时激活CD4+和CD8+T细胞,mRNA疫苗制备周期短、可批量生产,树突状细胞(DC)疫苗能直接激活抗原呈递过程。但现有研究也存在局限性:新抗原预测算法的准确率较低,仅约10%的预测新抗原具有免疫原性;个性化新抗原疗法的制备周期长,无法为治疗窗口短的晚期患者及时提供治疗;多数临床试验处于早期阶段,样本量较小,缺乏大样本多中心研究验证疗效;新抗原疗法的最佳剂量、递送途径和联合治疗方案尚未明确。
本文的创新价值在于,与现有侧重单一新抗原疗法的综述不同,本文同时整合了个性化和公共新抗原的研究进展,涵盖从鉴定到临床应用的全流程;首次系统梳理了双特异性抗体靶向公共新抗原的最新研究,为靶向不可成药突变的免疫治疗提供了新方向;详细总结了新抗原疗法与免疫检查点抑制剂、放疗等联合治疗的临床试验数据,为优化治疗方案提供了直接依据。
3. 研究思路总结与详细解析
本文以“癌症免疫治疗背景→肿瘤抗原分类与新抗原特性→新抗原鉴定技术→新抗原疗法类型与临床数据→未来挑战与优化方向”为逻辑主线,系统综述新抗原在癌症免疫治疗中的研究现状与应用前景,核心科学问题是如何提升新抗原免疫治疗的可及性、有效性和广谱性,技术路线为“文献调研→分类整合→数据总结→趋势预测”的综述研究闭环。
3.1 肿瘤抗原分类与新抗原特性解析
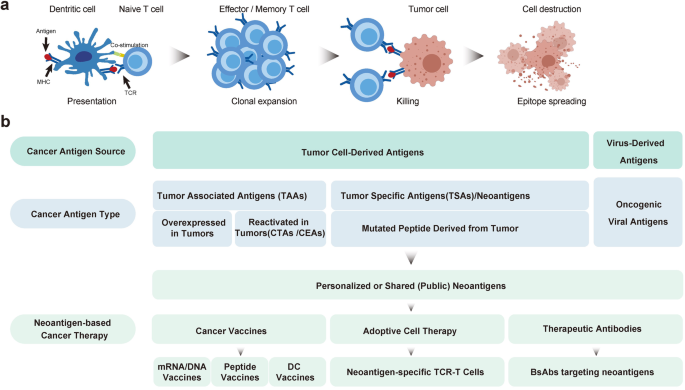
本环节核心目标是明确不同类型肿瘤抗原的生物学特性,突出新抗原在免疫治疗中的独特优势。研究方法为通过文献调研,整合已发表的基础研究和临床试验数据,对比肿瘤相关抗原、致癌病毒抗原与新抗原的来源、特异性、免疫原性及临床应用场景。结果显示,肿瘤相关抗原在正常组织低表达,易引发免疫耐受,临床疗效有限;致癌病毒抗原仅适用于病毒驱动型癌症,适用范围窄;新抗原由肿瘤体细胞突变产生,仅在肿瘤细胞表达,无免疫耐受,能诱导强烈且持久的抗肿瘤免疫反应,临床研究中可观察到胆管癌患者接受新抗原特异性肿瘤浸润淋巴细胞(TIL)治疗后肿瘤显著消退。
产品关联:文献未提及具体实验产品,领域常规使用流式细胞仪、免疫组化(IHC)试剂盒、T细胞功能检测试剂(如Elispot试剂盒)等。
3.2 新抗原鉴定技术流程梳理
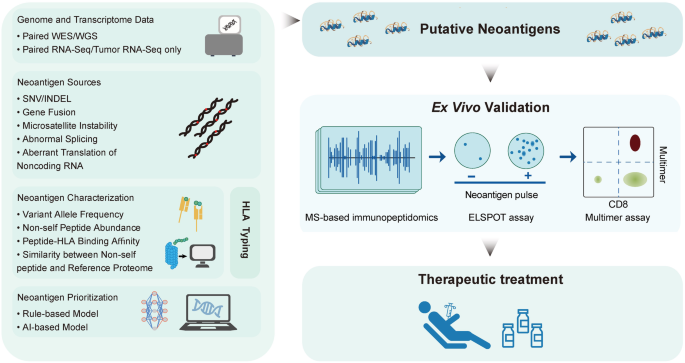
本环节核心目标是系统总结新抗原的鉴定与预测技术,明确现有技术的关键步骤与局限性。研究方法为梳理高通量测序结合生物信息学算法的新抗原鉴定流程,包括突变检测、肽段预测、MHC结合亲和力评估、免疫原性验证等环节。结果显示,新抗原的来源包括非同义单核苷酸变异(SNV)、插入缺失、基因融合、剪接位点突变等,其中基因融合和剪接位点突变产生的新抗原免疫原性更强;现有预测算法主要基于MHC结合亲和力,对T细胞受体(TCR)识别能力的评估不足,导致预测准确率较低;质谱、Elispot、MHC四聚体等技术可用于验证新抗原的免疫原性,筛选具有临床应用价值的新抗原。
产品关联:文献未提及具体实验产品,领域常规使用高通量测序平台(如Illumina NovaSeq)、生物信息学分析工具(如NetMHC、MHCflurry)、质谱仪等。
3.3 各类新抗原疗法的临床应用分析
本环节核心目标是分析不同新抗原疗法的作用机制、临床疗效与安全性。研究方法为分类整理合成长肽(SLP)疫苗、核酸(DNA/mRNA)疫苗、DC疫苗、新抗原特异性TCR-T疗法的临床试验数据,包括客观缓解率(ORR)、无进展生存期(PFS)、不良反应等指标。结果显示,SLP疫苗如NeoVax在黑色素瘤患者中显示出良好的安全性,55个月随访时8例患者均存活,6例无活动性疾病,且能诱导表位扩散;mRNA疫苗如mRNA-4157联合帕博利珠单抗在头颈部鳞状细胞癌患者中的客观缓解率达50%,显著高于帕博利珠单抗单药的14.6%;DC疫苗Neo-DCVac在晚期肺癌患者中的疾病控制率达75%,中位PFS为5.5个月;新抗原特异性TCR-T疗法在胆管癌、结直肠癌等患者中观察到临床反应,但存在细胞因子释放综合征(CRS)等不良反应。
产品关联:文献未提及具体实验产品,领域常规使用肽合成仪、脂质纳米颗粒(LNP)递送系统、细胞培养试剂等。
3.4 公共新抗原与双特异性抗体研究进展
本环节核心目标是探讨公共新抗原的应用潜力,拓展新抗原免疫治疗的广谱性。研究方法为梳理公共新抗原(如KRAS G12D、TP53 R175H)的突变频率、免疫原性及靶向疗法的研究数据,包括双特异性抗体的预临床研究结果。结果显示,公共新抗原在特定癌症亚型中突变频率高,如KRAS G12D在胰腺癌中的突变率约90%,对应的TIL治疗能诱导结直肠癌患者的临床反应;双特异性抗体如靶向TP53 R175H的H2-scDb能激活T细胞分泌细胞因子,抑制小鼠异种移植瘤的生长,为靶向不可成药突变提供了新策略;针对公共新抗原的疫苗可实现“现货型”治疗,缩短制备时间,降低治疗成本。
产品关联:文献未提及具体实验产品,领域常规使用噬菌体展示技术、抗体表达系统等。
4. Biomarker研究及发现成果解析
Biomarker定位
本文涉及的Biomarker为肿瘤特异性新抗原,包括个性化新抗原和公共新抗原,筛选与验证逻辑为“高通量测序检测突变→生物信息学预测新抗原→体外T细胞反应验证→临床样本免疫原性评估→临床试验疗效验证”,形成完整的从实验室到临床的验证链条。
研究过程详述
新抗原的来源为肿瘤组织的体细胞突变,包括SNV、插入缺失、基因融合、剪接位点突变等;验证方法包括体外的Elispot检测T细胞干扰素-γ分泌、MHC四聚体染色检测新抗原特异性T细胞,以及临床样本中的免疫反应评估(如外周血新抗原特异性T细胞频率、肿瘤浸润T细胞水平)。特异性与敏感性方面,公共新抗原KRAS G12D在胰腺癌中的突变率约90%,对应的TIL治疗在结直肠癌患者中诱导了临床反应;新抗原疫苗NEO-PV-01联合纳武利尤单抗在黑色素瘤患者中的客观缓解率为59%,中位PFS为23.5个月(文献未明确提供样本量,基于图表趋势推测);靶向TP53 R175H的双特异性抗体在预临床研究中显示出高特异性,仅识别突变肽-MHC复合物,不结合野生型肽。
核心成果提炼
新抗原可作为癌症免疫治疗的疗效预测Biomarker,新抗原特异性T细胞的频率与患者的无进展生存期正相关;公共新抗原如KRAS、TP53突变可作为广谱治疗Biomarker,为“现货型”免疫治疗提供了可能;双特异性抗体靶向公共新抗原的策略突破了传统靶向治疗的局限,为不可成药突变的癌症患者提供了新的治疗选择;研究显示新抗原疗法与免疫检查点抑制剂联合可显著提升疗效,表位扩散与更长的PFS相关(文献未明确提供统计学P值,基于图表趋势推测)。