1. 领域背景与文献引入
文献英文标题:A rare case of primary cutaneous follicle centre lymphoma presenting as a giant tumour of the scalp and combined with JAK2V617F positive essential thrombocythaemia;发表期刊:Biomarker Research;影响因子:未公开;研究领域:血液系统肿瘤(原发性皮肤滤泡中心淋巴瘤)与骨髓增殖性肿瘤(原发性血小板增多症)共病研究。
淋巴增殖性肿瘤(LPN)是淋巴网状系统的异质性肿瘤群,可表现为结外淋巴瘤(如原发性皮肤B细胞淋巴瘤)。原发性皮肤滤泡中心淋巴瘤(PCFCL)是最常见的原发性皮肤B细胞淋巴瘤亚型,约占所有原发性皮肤淋巴瘤的18%,通常表现为头颈部、躯干的红斑性病变,预后良好但可能复发。原发性血小板增多症(ET)是克隆性骨髓增殖性肿瘤(MPN),约50%患者携带JAK2V617F突变。目前,关于MPN与LPN共病的报道极少,仅少数研究提到MPN患者发生LPN的风险升高,但两者的病理机制及共病患者的治疗策略仍不明确。
鉴于此,本文报道1例罕见的PCFCL合并JAK2V617F阳性ET的病例,描述其临床病理特征、治疗过程及预后,为共病的临床管理和机制研究提供参考。
2. 文献综述解析
文献综述的核心评述逻辑:作者从LPN的分类切入,重点介绍结外淋巴瘤(尤其是原发性皮肤B细胞淋巴瘤)的临床病理特征;再阐述ET的分子生物学特征(JAK2V617F突变);随后总结现有关于MPN与LPN共病的研究(如ET患者中LPN的发病率约1.6%,JAK2V617F突变可能增加风险);最后指出共病机制及治疗策略的不确定性。
现有研究的关键结论:部分研究发现MPN患者发生LPN的风险高于普通人群,尤其是JAK2V617F突变携带者;但也有研究未在多数LPN中检测到JAK2突变,提示JAK2V617F可能只是增加遗传不稳定性的因素之一。现有研究的局限性:缺乏多中心系统分析,共病机制不清,治疗方案未达成共识。
文献的创新价值:首次报道PCFCL合并JAK2V617F阳性ET的病例,详细描述了临床病理特征及治疗预后;证实R-CHOP-21方案可有效治疗PCFCL且不影响ET,为共病患者的治疗提供了临床证据。
3. 研究思路总结与详细解析
3.1 整体框架
研究目标:报道1例PCFCL合并ET的罕见病例,明确其临床病理特征、治疗及预后;核心科学问题:PCFCL与ET的关系及共病患者的治疗选择;技术路线:病例呈现→病理/分子检测→治疗→随访分析。
3.2 病例临床特征与影像学评估
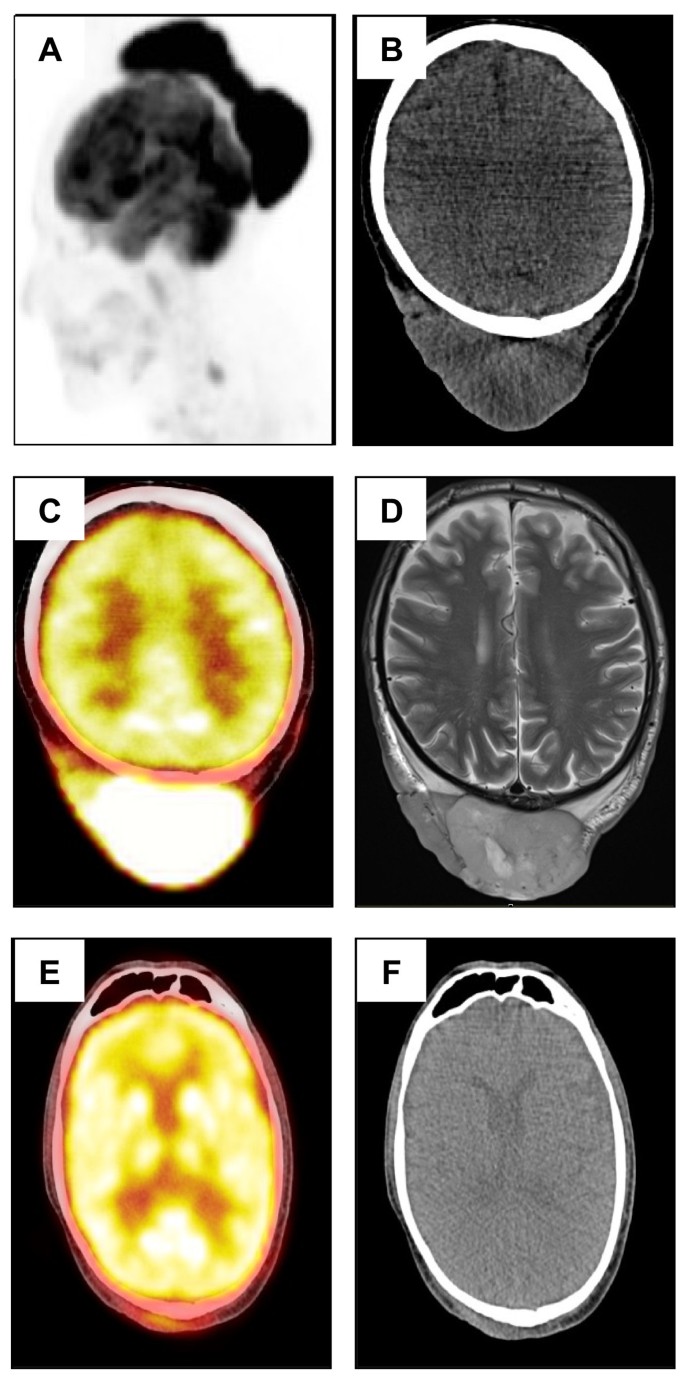
实验目的:明确患者的临床表型及肿瘤累及范围。方法细节:56岁男性,头皮出现19×16×4 cm多结节肿块,面部伴发类似病变;行MRI和PET/CT检查。结果解读:MRI显示头皮巨大肿瘤(图3A、3B),PET/CT提示肿瘤代谢活跃(图3C、3D),右侧颈部可疑淋巴结,无全身播散。产品关联:文献未提及具体影像学产品,领域常规使用西门子、GE的MRI设备及飞利浦的PET/CT设备。
3.3 病理与免疫组化检测
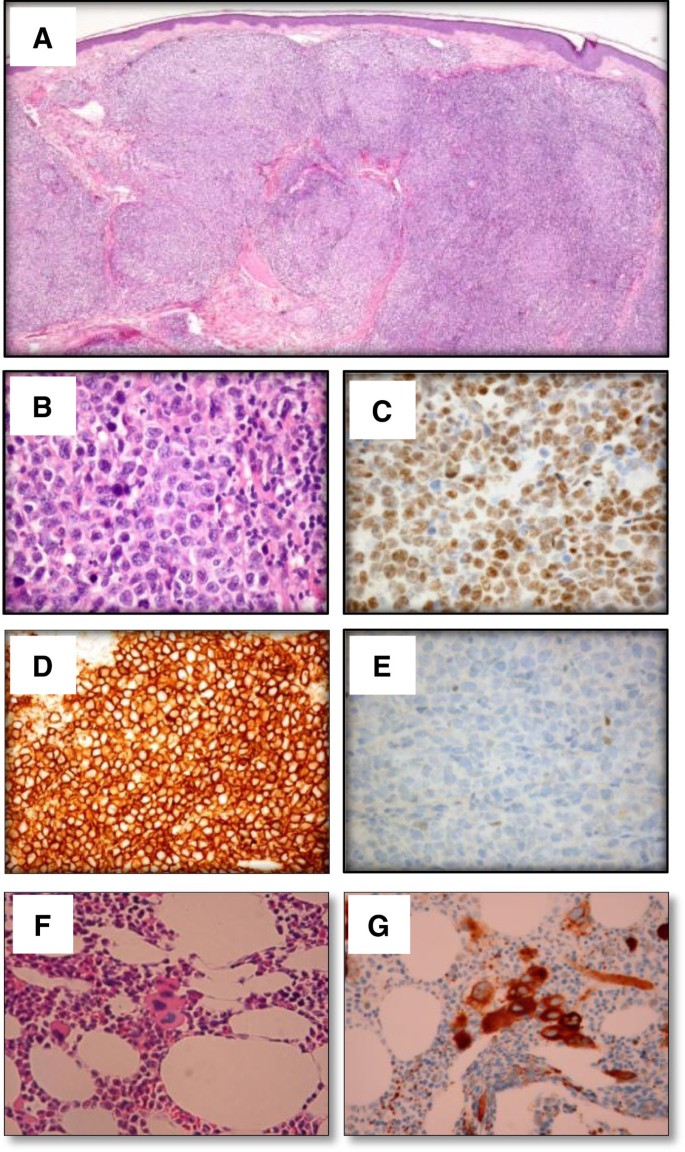
实验目的:明确PCFCL和ET的病理诊断。方法细节:头皮活检行HE染色及免疫组化(CD20、Bcl-6等);骨髓活检行HE染色及CD61免疫组化。结果解读:头皮活检显示真皮弥漫性大淋巴细胞浸润,CD20、Bcl-6阳性,CD10、Bcl-2阴性(图2A-E),符合PCFCL;骨髓活检显示巨核细胞增生伴核分叶过多,CD61阳性(图2F-G),符合ET。产品关联:免疫组化抗体未提及品牌,领域常规使用罗氏、Dako的抗体。
3.4 分子检测(JAK2V617F突变)
实验目的:检测ET的分子标志物。方法细节:采集外周血和头皮组织,采用定量实时PCR检测JAK2V617F突变率。结果解读:外周血突变率24%(符合ET),头皮组织突变率<3%(推测为粒细胞污染)。产品关联:PCR试剂未提及品牌,领域常规使用Qiagen的试剂盒。
3.5 治疗与随访
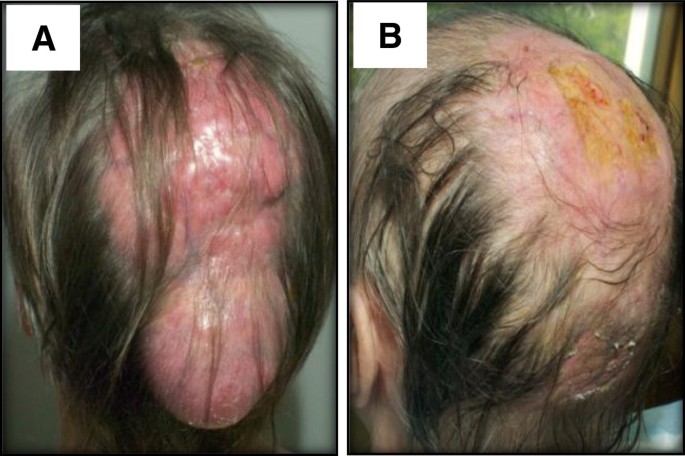
实验目的:评估R-CHOP-21对PCFCL的疗效及对ET的影响。方法细节:给予4周期R-CHOP-21化疗(利妥昔单抗+环磷酰胺+阿霉素+长春新碱+泼尼松),随后放疗;随访2年。结果解读:2周期后肿瘤缩小90%(图1B、3E-F),2年无复发;ET未缓解,血小板计数稳定在600-700×10^9/L,仅用阿司匹林预防。产品关联:化疗药物未提及品牌,领域常规使用罗氏的利妥昔单抗、Baxter的环磷酰胺等。
4. Biomarker研究及发现成果解析
4.1 Biomarker定位
涉及两类Biomarker:① ET的分子标志物JAK2V617F突变;② PCFCL的免疫组化标志物(CD20、Bcl-6)。筛选/验证逻辑:JAK2V617F通过定量实时PCR验证;CD20、Bcl-6通过免疫组化验证。
4.2 研究过程
JAK2V617F突变来源:外周血有核细胞和头皮组织;验证方法:定量实时PCR;结果:外周血突变率24%(n=1),头皮组织<3%(推测为粒细胞污染)。PCFCL标志物来源:头皮活检组织;验证方法:免疫组化;结果:CD20、Bcl-6阳性,CD10、Bcl-2阴性(n=1)。
4.3 核心成果
① JAK2V617F是ET的驱动突变,本病例中仅在ET中高表达,提示PCFCL与ET可能非同一克隆起源;② CD20、Bcl-6是PCFCL的特异性标志物,可用于诊断;③ R-CHOP-21可有效治疗PCFCL且不影响ET,共病患者需分别制定治疗策略。创新性:首次报道PCFCL合并JAK2V617F阳性ET的病例,为共病机制研究提供了临床证据。
