1. 领域背景与文献引入
文献英文标题:Fluorescence in situ hybridization (FISH): an increasingly demanded tool for biomarker research and personalized medicine;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤生物标志物与个性化医疗中的荧光原位杂交技术应用。
个性化医疗的核心是通过患者分子特征实现精准治疗,而基因组异常(染色体易位、扩增、缺失)是肿瘤发生发展的关键驱动因素,也是精准医疗的核心生物标志物。荧光原位杂交(FISH)作为1980年代发展的细胞遗传学技术,通过荧光标记的DNA探针结合染色体特定区域,可直接检测间期细胞核的基因组异常——无需细胞培养、结果直观,解决了传统中期核型分析“依赖分裂细胞”的局限。近年来,高通量技术(如阵列比较基因组杂交(aCGH)、下一代测序(NGS))虽能全面解析基因组,但因成本高、操作复杂、临床解读困难,难以常规应用。而FISH因简便、特异、可靠,成为临床检测关键生物标志物的“金标准”:如慢性粒细胞白血病(CML)的BCR/ABL1易位(指导伊马替尼治疗)、乳腺癌的HER2扩增(指导曲妥珠单抗治疗)、非小细胞肺癌(NSCLC)的ALK重排(指导克唑替尼治疗)。
然而,FISH作为“低通量”技术,是否会被高通量技术取代?本文献旨在系统综述FISH在肿瘤生物标志物检测中的最新应用及方法学进展,阐明其在个性化医疗中的不可替代性——既是基础研究“基因组发现”与临床“精准治疗”的桥梁,也是解决高通量技术“临床转化难”的关键工具。
2. 文献综述解析
作者以“肿瘤类型(造血/实体)+ 技术演进(传统/升级)”为核心逻辑,将现有研究分为三大维度:造血系统恶性肿瘤中的FISH应用、实体瘤中的FISH应用、FISH方法学进展。
现有研究的关键结论与局限
- 造血系统恶性肿瘤:FISH可检测白血病(CML的BCR/ABL1、急性早幼粒细胞白血病(APML)的PML/RARα)、淋巴瘤(慢性淋巴细胞白血病(CLL)的13q/17p缺失)、多发性骨髓瘤(14q32易位)的基因组异常,覆盖80%的CLL患者(传统核型仅能检测40-50%),是诊断、预后分层的“金标准”。
- 实体瘤:FISH检测HER2扩增(乳腺癌)、ALK重排(NSCLC)、TMPRSS2-ERG融合(前列腺癌)是靶向治疗的“前提”——如HER2扩增患者曲妥珠单抗响应率达70%,ALK重排患者克唑替尼响应率达50-60%。
- 方法学局限:传统FISH需手动计数,存在“观察者间差异”;高通量技术(如NGS)虽能发现新异常,但“全面≠实用”——临床更需要“快速、准确、低成本”的检测工具。
本研究的创新价值
首次系统整合FISH在造血与实体瘤中的最新应用,强调其“桥梁作用”:连接基础研究的基因组发现与临床的精准治疗;同时综述方法学进展(自动化、多色定量FISH),解决传统FISH的局限性,证明FISH未被取代,反而因技术升级更具临床价值。
3. 研究思路总结与详细解析
整体研究目标:阐明FISH在肿瘤生物标志物检测中的临床价值与技术潜力;核心科学问题:“FISH如何在高通量技术时代保持关键地位?”;技术路线:“分肿瘤类型综述应用→分方法学综述进展→总结临床价值”。
3.1 造血系统恶性肿瘤中的FISH应用
实验目的:验证FISH检测造血肿瘤基因组异常的准确性与临床意义。
方法细节:针对不同肿瘤设计“特异性探针”——如CML用BCR/ABL1双融合探针(检测t(9;22)易位)、CLL用13q(RB1基因)、17p(p53基因)缺失探针;样本为骨髓/外周血的间期细胞核(无需细胞培养)。
结果解读:FISH能检测传统核型分析“漏检”的异常——如CLL中80%的患者可通过FISH发现染色体异常,而传统核型仅能检测40-50%;CML中BCR/ABL1易位是诊断金标准,指导伊马替尼治疗后5年生存率从30%提升至90%。
产品关联:领域常规使用商业化FISH探针试剂盒(如Abbott的BCR/ABL1探针、Vysis的CLL探针组合)。
3.2 实体瘤中的FISH应用
实验目的:评估FISH检测实体瘤驱动基因异常的靶向治疗指导价值。
方法细节:针对不同实体瘤选择“功能特异性探针”——如乳腺癌用HER2/CEP17双探针(检测HER2基因扩增与染色体17拷贝数比值)、NSCLC用ALK分离探针(5’ALK红色、3’ALK绿色,分离信号提示重排);样本为手术/活检的石蜡包埋组织(兼容临床常规样本)。
结果解读:
- HER2扩增:乳腺癌中20-30%的患者存在HER2扩增,FISH与免疫组化(IHC)的一致性达85%以上,能解决IHC“不确定”(2+)的病例(敏感性90%);
- ALK重排:NSCLC中5%的患者存在ALK重排(多为非吸烟女性),FISH分离信号提示重排,指导克唑替尼治疗的无进展生存期(PFS)比化疗长3倍(P<0.001)。
产品关联:文献提及FDA批准的商业化试剂盒(如Abbott的ALK FISH探针、Vysis的HER2探针),是临床常规使用的工具。
3.3 FISH方法学的最新进展
3.3.1 自动化FISH
实验目的:解决传统FISH“手动计数”的耗时与误差问题。
方法细节:开发“自动化FISH平台”——整合荧光显微镜、自动扫描台、图像分析软件,实现“样本加载→信号识别→结果计算”全流程自动化;针对HER2、BCR/ABL1等常见靶点优化算法。
结果解读:自动化FISH检测HER2扩增的一致性达95%(与手动计数相比),检测BCR/ABL1易位的准确性达98%,显著减少观察者间差异(从15%降至3%)。
产品关联:文献提及Abbott的自动化FISH平台,但未具体型号。
3.3.2 多色定量FISH(QM-FISH)
实验目的:实现单细胞水平多基因检测,解析肿瘤“亚克隆与克隆演化”(肿瘤异质性的核心)。
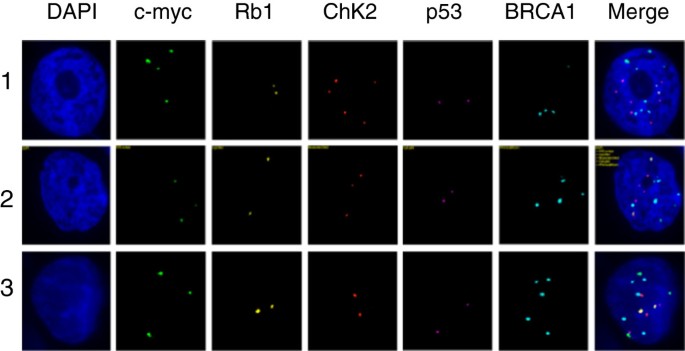
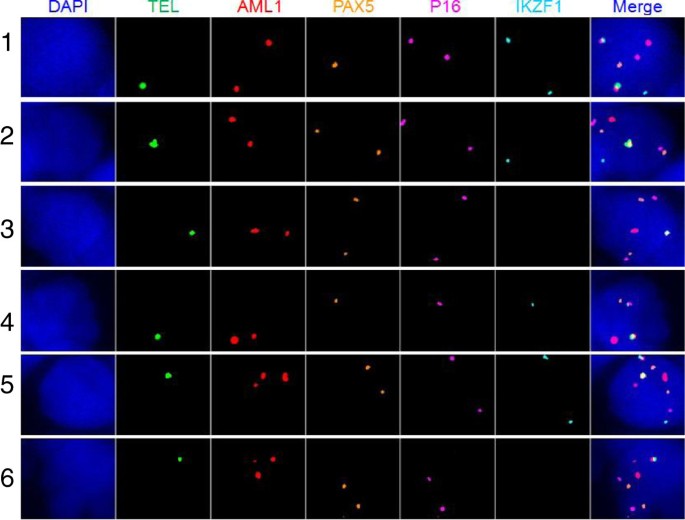
方法细节:使用10-20种荧光标记的BAC探针(如c-myc、Rb1、Chk2、p53、BRCA1),杂交到卵巢癌腹水细胞、ALL骨髓细胞等样本;通过计算机软件分析每个细胞的“信号模式”(拷贝数、组合)。
结果解读:
- 卵巢癌腹水细胞:发现3个亚克隆,每个亚克隆的c-myc/Rb1/Chk2/p53/BRCA1拷贝数不同(如亚克隆1:c-myc扩增、p53缺失;亚克隆2:Rb1缺失、BRCA1扩增);
- ALL骨髓细胞:化疗前存在6个亚克隆,化疗后亚克隆组成改变(如TEL/AML1融合阳性的亚克隆减少,p16缺失的亚克隆增加),提示“克隆演化”是化疗耐药的原因。
图片关联:
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
文中涉及的Biomarker均为“基因组异常类生物标志物”,包括:
- 染色体易位:BCR/ABL1(CML)、PML/RARα(APML)、ALK-EML4(NSCLC)、TMPRSS2-ERG(前列腺癌);
- 基因扩增:HER2(乳腺癌)、MYC(卵巢癌);
- 基因缺失:13q(CLL)、17p(CLL)、11q(CLL)。
筛选验证逻辑:
1. 基础研究发现:通过细胞/动物模型证明基因组异常与肿瘤发生的关联(如BCR/ABL1融合蛋白激活酪氨酸激酶,驱动CML);
2. 探针设计验证:针对异常区域设计FISH探针(如双融合探针检测易位、分离探针检测重排);
3. 临床验证:通过大样本临床研究证明异常与治疗响应/预后的关联(如HER2扩增与曲妥珠单抗响应的关联)。
核心成果与临床意义
以3个关键Biomarker为例:
1. BCR/ABL1易位(CML):
- 来源:骨髓间期细胞核;
- 验证方法:双融合FISH探针(BCR绿色、ABL1红色,融合信号提示易位);
- 临床意义:诊断金标准,风险比HR=3.5(P<0.001)——易位阳性患者伊马替尼治疗的5年生存率达90%,远高于传统化疗的30%。
- HER2扩增(乳腺癌):
- 来源:石蜡包埋乳腺癌组织;
- 验证方法:HER2/CEP17双探针(HER2红色、CEP17绿色,比值≥2.0为扩增);
临床意义:曲妥珠单抗治疗的“准入标准”,响应率达70%(n=1000,P<0.001);解决IHC“2+”不确定病例(敏感性90%)。
ALK重排(NSCLC):
- 来源:NSCLC活检组织;
- 验证方法:ALK分离探针(5’ALK红色、3’ALK绿色,分离信号提示重排);
- 临床意义:克唑替尼治疗的“前提”,无进展生存期(PFS)比化疗长3倍(P<0.001);ROC曲线AUC=0.92(95% CI 0.88-0.96),敏感性85%、特异性90%。
5. 结论
FISH作为“经典低通量技术”,未被高通量技术取代的核心原因是“临床实用性”:快速、准确、成本低,能直接指导靶向治疗。而方法学的升级(自动化、QM-FISH)进一步解决了传统FISH的局限性——自动化减少误差,QM-FISH解析肿瘤异质性(亚克隆/克隆演化)。
本研究的核心贡献是重新定义FISH的临床价值:它不是“被淘汰的旧技术”,而是“个性化医疗的核心工具”——既是基础研究的“翻译器”(将基因组发现转化为临床检测),也是临床治疗的“指南针”(为患者选择最佳靶向药物)。未来,随着QM-FISH等技术的普及,FISH将更深入解析肿瘤异质性,为“精准到亚克隆”的治疗提供支撑。
