1. 领域背景与文献引入
文献英文标题:Expression of p52, a non-canonical NF-kappaB transcription factor, is associated with poor ovarian cancer prognosis;发表期刊:Biomarker Research;影响因子:未公开;研究领域:卵巢癌预后生物标志物、非经典NF-κB信号通路。
卵巢癌是全球女性第五大癌症死亡原因,也是妇科肿瘤中死亡率最高的类型,5年生存率不足50%。其核心挑战在于晚期诊断(约70%患者初诊时为Ⅲ/Ⅳ期)和化疗耐药(多数患者最终对铂类药物产生耐药并复发)。近年来,PARP抑制剂、VEGF抑制剂等靶向治疗虽改善了部分患者预后,但仍需更精准的预后标志物和治疗靶点。核因子-κB(NF-κB)信号通路是炎症与癌症的关键桥梁,调控肿瘤生长、耐药和免疫逃逸,分为经典通路(以p65/p50二聚体为主,介导急性炎症反应)和非经典通路(以p52/RelB二聚体为主,调控细胞发育与慢性炎症)。现有研究中,经典通路的p65在卵巢癌中的预后意义仍存争议(部分研究显示高表达与不良预后相关,大样本研究却发现高核p65与更好生存相关);非经典通路的p52虽在乳腺癌、肺癌等肿瘤中被证实与不良预后相关,且体外/体内研究提示其通过促进卵巢癌细胞增殖、干细胞自我更新参与肿瘤进展,但尚无临床研究验证其与卵巢癌预后的关联。
针对这一研究空白,本研究通过检测临床卵巢癌样本中p52和p65的表达,分析其与患者生存结局的关联,旨在明确p52的预后价值,为卵巢癌的靶向治疗提供新方向。
2. 文献综述解析
作者以“经典与非经典NF-κB通路的预后意义”为核心评述逻辑,按通路分类总结现有研究,并指出其局限性:
现有研究总结
- 经典通路p65:多项小样本研究(33-85例)显示p65高表达与卵巢癌不良预后相关,但大样本研究(324例高分级浆液性癌)发现高核p65与更好生存相关,差异源于样本量、 covariates调整及表达阈值的不同。
- 非经典通路p52:在乳腺癌、肺癌等肿瘤中,p52高表达与不良预后相关;体外研究显示其通过促进卵巢癌细胞增殖、转移参与肿瘤进展,但无临床研究验证其与卵巢癌预后的关联。
- 技术局限性:现有研究多未区分胞质与核表达的功能差异(核表达代表通路激活),未调整临床 covariates,且未同时分析经典与非经典通路的相互作用。
创新价值论证
本研究首次在196例卵巢癌临床样本中同时检测p52(非经典)和p65(经典)的胞质与核表达,通过半定量H-score和多变量调整分析,明确p52的独立预后价值;并在高分级浆液性癌亚组(卵巢癌最常见、最致命的亚型)中验证了结果的稳健性,弥补了非经典NF-κB通路在卵巢癌预后研究中的空白。
3. 研究思路总结与详细解析
本研究采用回顾性队列设计,技术路线为“样本制备→蛋白表达检测→临床关联分析→预后验证”,目标是探讨p52和p65表达与卵巢癌预后的关联,核心科学问题是“非经典NF-κB通路p52是否为卵巢癌的独立预后因子”。
3.1 研究队列与样本制备
实验目的:建立具有临床代表性的卵巢癌组织样本队列。
方法细节:纳入Vanderbilt大学医学中心(VUMC)组织库(TROC)中1994-2004年接受初始分期/减瘤术的原发性上皮性卵巢肿瘤样本,排除非上皮性、转移性或复发性肿瘤后,最终纳入196例(177例浸润性,19例交界性);每例样本选取4个1mm的肿瘤核心制作组织微阵列(TMA),排除肿瘤细胞<100个的核心;所有样本按2014年WHO分类重新评估组织学类型,临床数据(分期、分级、治疗、生存结局)通过电子病历(EMR)和REDCap数据库提取。
结果解读:纳入样本的临床特征符合卵巢癌分布——70.3%为晚期(Ⅲ/Ⅳ期)、73.5%为高分级、72.9%为浆液性癌,中位年龄58.3岁,中位总体生存(OS)3.6年,中位无进展生存(PFS)1.6年。
实验所用关键产品:TMA制备用常规甲醛固定石蜡包埋(FFPE)组织,文献未提及具体试剂盒。
3.2 免疫组化检测p52与p65表达
实验目的:定量检测卵巢癌组织中p52(非经典)和p65(经典)的胞质与核表达。
方法细节:p52采用Santa Cruz的C-5小鼠单克隆抗体(货号sc-7386),p65采用Santa Cruz的F-6小鼠单克隆抗体(货号sc-8008);IHC染色后,用Ariol SL-50数字病理平台自动分析,计算H-score(百分比阳性细胞×染色强度:弱=1、中=2、强=3,范围0-300),并按中位数将表达分为高、低两组。
结果解读:p52和p65主要表达于肿瘤细胞胞质,核表达较低(p52中位胞质H-score=135.9,核=1.0;p65中位胞质H-score=154.3,核=2.7);两者的胞质与核表达呈显著正相关(p52 Spearman rho=0.69,p<0.001;p65 rho=0.78,p<0.001),但p52与p65的表达相关性较低(胞质rho=0.23,核rho=0.25,均p<0.001)。
图片展示:文献中Fig.1展示了p52和p65的代表性IHC染色结果,胞质表达为主,核表达用黄色箭头标注(
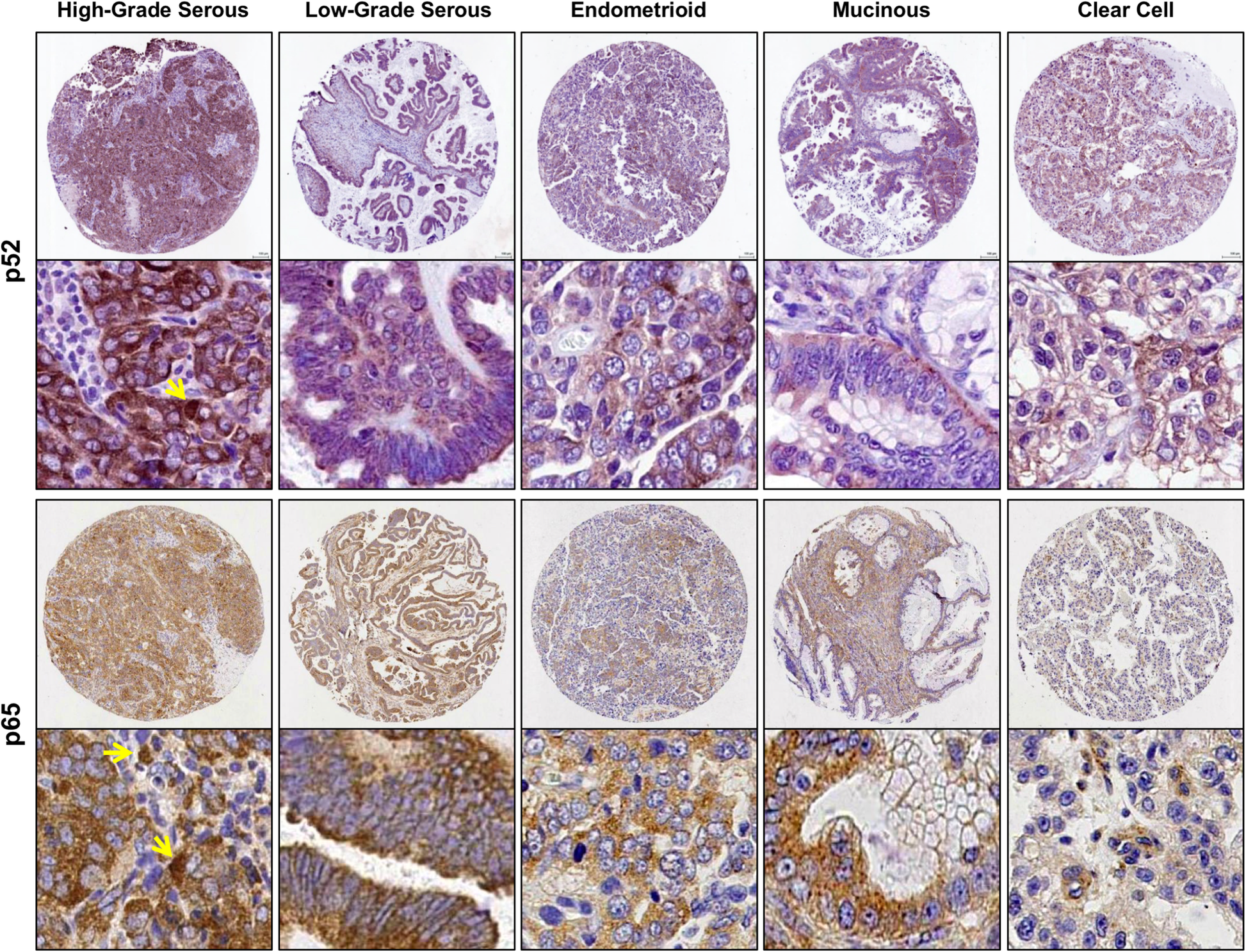
)。
实验所用关键产品:p52抗体(Santa Cruz,sc-7386)、p65抗体(Santa Cruz,sc-8008)、Ariol SL-50数字病理成像系统。
3.3 表达与临床特征的关联分析
实验目的:分析p52/p65表达与卵巢癌临床特征的关系。
方法细节:用Kruskal-Wallis检验比较不同临床亚组(分级、分期、组织学类型、化疗状态)的H-score差异,Bonferroni校正多重比较。
结果解读:p52高表达(中位数以上)与高分级(p<0.001)、晚期(p<0.05)、浆液性癌(p<0.001)及接受化疗(p<0.05)显著相关;p65高表达与高分级(p<0.05)、浆液性癌(p<0.001)相关,但与分期无显著关联。调整多重比较后,p52和p65的高表达仍与高分级、浆液性癌显著相关(p≤0.00357)。
实验所用关键产品:统计分析用R软件(survminer、ggplot2包)和SAS系统。
3.4 生存结局的关联分析
实验目的:验证p52/p65表达与卵巢癌生存结局的关联。
方法细节:用Kaplan-Meier法绘制生存曲线(Log-Rank检验差异),Cox比例风险模型计算风险比(HR)及95%置信区间(CI),调整年龄、分期、组织学类型、化疗等临床 covariates;进一步分析胞质/核表达的联合效应(只要胞质或核表达高于中位数即定义为高表达),并在高分级浆液性癌亚组(n=118)中验证结果。
结果解读:
- Kaplan-Meier分析显示,p52高胞质/核表达均与更差的PFS(Log-Rank p<0.001)和OS(Log-Rank p<0.001)相关,而p65无显著关联;
- 多变量调整后,p52高胞质表达与PFS(HR=1.54,95%CI 1.09-2.18,n=196,p=0.015)、OS(HR=1.53,95%CI 1.07-2.18,n=196,p=0.019)显著相关,高核表达与PFS(HR=1.67,95%CI 1.15-2.42,n=196,p=0.006)、OS(HR=1.49,95%CI 1.02-2.17,n=196,p=0.041)显著相关;
- 联合胞质/核表达后,p52仍与PFS(HR=1.91,95%CI 1.23-2.96,n=196,p=0.004)、OS(HR=1.70,95%CI 1.09-2.66,n=196,p=0.021)显著相关,且独立于p65的表达(调整p65后HR仍显著);
- 在高分级浆液性癌亚组中,p52高表达与PFS(HR=1.91,95%CI 1.23-2.96,n=118,p=0.004)、OS(HR=1.70,95%CI 1.09-2.66,n=118,p=0.021)仍显著相关。
实验所用关键产品:统计分析用R软件(survminer、ggplot2包)和SAS系统。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究的生物标志物为非经典NF-κB转录因子p52,作为卵巢癌的预后生物标志物,筛选逻辑为“基于现有非经典通路的促癌机制→临床样本检测表达→关联生存结局→验证独立性”。
研究过程详述
- Biomarker来源:原发性卵巢肿瘤组织;
- 验证方法:IHC检测胞质/核表达,H-score半定量(0-300),中位数二分法定义高/低表达;
- 特异性与敏感性:虽未直接提供ROC曲线的AUC值,但生存分析显示p52的预后关联具有统计学显著性(如联合表达的PFS HR=1.91,95%CI 1.23-2.96,p=0.004);
- 样本量:196例(其中高分级浆液性癌118例)。
核心成果提炼
- 预后价值:p52是卵巢癌(尤其是高分级浆液性癌)的独立预后生物标志物,高表达与更差的PFS(HR=1.91,95%CI 1.23-2.96,p=0.004)和OS(HR=1.70,95%CI 1.09-2.66,p=0.021)相关;
- 独立性:p52的预后关联独立于经典通路p65的表达;
- 创新性:首次在临床样本中证明非经典NF-κB通路p52的卵巢癌预后价值,为靶向非经典通路的卵巢癌治疗(如抑制p52的加工或核转运)提供了理论基础。
综上,本研究明确了p52作为卵巢癌预后生物标志物的价值,填补了非经典NF-κB通路在卵巢癌研究中的空白,为卵巢癌的精准预后评估和靶向治疗提供了新依据。
