1. 领域背景与文献引入
文献英文标题:Microbiome multi-omics analysis reveals novel biomarkers and mechanisms linked with CD etiopathology;发表期刊:Biomarker Research;影响因子:未公开;研究领域:炎症性肠病(IBD)肠道微生物组与发病机制。
炎症性肠病(IBD)是一类以慢性肠道炎症为特征的疾病,主要包括克罗恩病(CD)和溃疡性结肠炎(UC),其发病与遗传、环境及肠道微生物组失调密切相关。近年来研究表明,肠道微生物组的结构和功能异常是IBD的核心驱动因素:一方面,有益菌(如产丁酸盐的Faecalibacterium prausnitzii)减少导致抗炎代谢物(如丁酸盐)水平下降,削弱肠道屏障功能;另一方面,有害菌(如黏附侵袭性大肠杆菌,AIEC)富集通过激活Th1/Th17通路引发慢性炎症。然而,现有研究存在三大空白:1)多基于单一组学(如宏基因组),难以解析“微生物-代谢-宿主炎症”的协同机制;2)CD与UC的微生物组差异未充分阐明——UC的微生物变化更微妙,CD的失调更严重但具体机制不清;3)临床缺乏高特异性CD生物标志物,难以早期诊断和精准治疗。
针对上述空白,本研究采用宏基因组、宏转录组及代谢组的多组学整合策略,对CD患者、UC患者及健康对照(HC)的粪便样本进行分析,旨在:1)鉴定CD特异性微生物及代谢生物标志物;2)阐明微生物失调通过代谢重编程及毒力因子表达促进CD炎症的机制;3)区分CD与UC的微生物组差异。研究结果为CD诊断提供了新型生物标志物,也为理解微生物组在CD发病中的作用提供了全面视角。
2. 文献综述解析
作者对现有研究的评述逻辑围绕“IBD亚型差异-微生物组变化-机制关联”展开:首先,现有研究一致认为CD患者肠道微生物多样性显著降低,有益菌(如F. prausnitzii)减少、有害菌(如E. coli、Ruminococcus gnavus)增加,但UC仅涉及少数物种(如Clostridiaceae bacterium OM08-6BH)的变化,提示两者发病机制存在本质差异;其次,丁酸盐的抗炎作用已被证实,但丙酸盐对AIEC毒力的调控仅在体外报道,缺乏患者样本的体内验证;最后,AIEC的毒力因子(如ompA)通过促进细菌黏附侵袭参与CD炎症,但多组学整合研究尚未揭示“微生物代谢-毒力因子-宿主反应”的动态关联。
现有研究的局限性包括:1)单一组学为主,难以解析微生物组的“功能活性”及“代谢输出”;2)缺乏大样本验证队列,生物标志物临床适用性不足;3)对UC的微生物机制研究较少,难以区分IBD亚型。
本研究的创新点在于:1)首次用多组学整合分析CD患者样本,关联“微生物-代谢-毒力”机制;2)发现Faecalimonas umbilicata这一CD特异性新型物种;3)阐明AIEC利用天冬氨酸和丙酸盐促进毒力的体内机制;4)明确CD的微生物失调程度远重于UC,为IBD亚型精准治疗提供依据。
3. 研究思路总结与详细解析
本研究整体框架为“队列设计-多组学数据生成-数据分析-多组学整合-验证”,核心科学问题是“CD中微生物失调如何通过代谢重编程及毒力因子表达驱动炎症”,技术路线遵循“发现-验证-机制解析”闭环。
3.1 队列设计与样本收集
实验目的:建立涵盖不同疾病状态及人群的发现队列与验证队列,保证结果通用性。
方法细节:发现队列包括67名HC、67名CD患者(缓解期,HBI<4)、77名UC患者(缓解期,CAI<4),排除抗生素使用2个月内的个体;验证队列包括497名HC和141名CD患者(来自3个独立队列,含术后及新发CD患者)。所有参与者提供粪便样本用于多组学分析。
结果解读:发现队列覆盖IBD主要亚型及健康人群,验证队列涵盖不同临床表型CD患者,确保结果外部有效性。
产品关联:文献未提及具体样本收集产品,领域常规使用粪便保存管(如OMNIgene•GUT)稳定微生物及RNA。
3.2 多组学数据生成
实验目的:获取宏基因组(物种组成)、宏转录组(功能通路活性)及代谢组(代谢物水平)数据,为整合分析提供基础。
方法细节:1)宏基因组:200 mg粪便用胍基硫氰酸盐提取DNA,Illumina HiSeq测序(平均4.12 Gb/sample);2)宏转录组:250 mg粪便用TE缓冲液裂解,RNeasy Mini Kit(Qiagen)提取总RNA,Ribo-zero Magnetic kit去除rRNA,Illumina HiSeq测序(平均4.28 Gb/sample);3)代谢组:100 mg粪便用磷酸盐缓冲液提取代谢物,与TSP(内参)混合后,用400 MHz Bruker Advanced Spectrometer(配低温探头)进行NMR分析,Chenomx软件鉴定并定量23种代谢物。
结果解读:宏基因组覆盖1381种微生物,宏转录组解析355条代谢通路,代谢组定量短链脂肪酸(如丁酸盐、丙酸盐)及氨基酸(如天冬氨酸),为后续分析提供全面数据。
产品关联:实验所用关键产品:Qiagen的RNeasy® Mini Kit(货号74104)、Illumina HiSeq平台、Bruker 400 MHz谱仪、Chenomx NMR Suite(v8.11)。
3.3 微生物差异丰度分析与机器学习建模
实验目的:鉴定CD特异性微生物物种,构建诊断模型。
方法细节:1)差异丰度分析:用ANCOM-BC工具比较CD与HC、CD与UC的物种丰度差异(校正性别、年龄等混杂因素);2)机器学习建模:基于差异物种构建两种随机森林模型——模型1含174种差异物种,模型2含10种最富集(如Faecalimonas umbilicata、E. coli)和10种最depletion(如F. prausnitzii)的物种,五折交叉验证评估性能,并在验证队列中验证。
结果解读:1)CD与HC相比,156种物种富集、18种depletion(图1),其中Faecalimonas umbilicata是未报道过的CD富集物种(log₂FC=-9.8,FDR=5.8×10⁻¹⁸);2)模型2在验证队列中的AUC为0.942,表现出高诊断性能(图1C)。
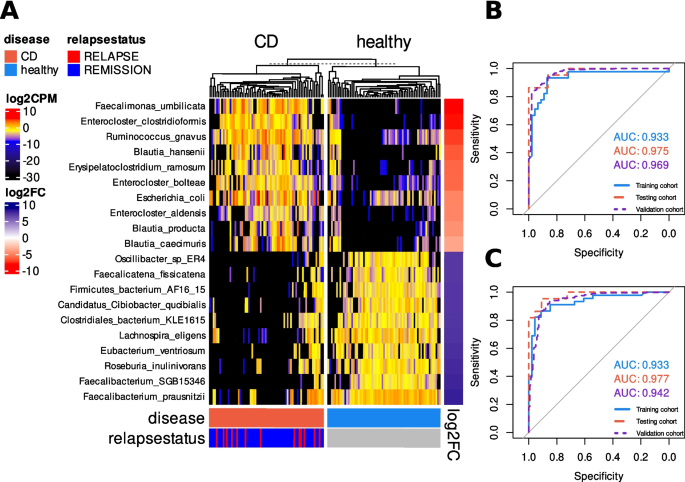
产品关联:使用MetaPhlAn(v4.0.3)注释物种,HumanN(v3.6)分析功能,R语言caret包构建模型。
3.4 宏转录组与代谢组分析
实验目的:揭示CD中微生物代谢通路及代谢物的变化,关联“微生物功能-代谢输出”。
方法细节:1)宏转录组:用HumanN分析差异表达通路(混合效应线性模型);2)代谢组:用Mann-Whitney U test比较代谢物水平差异,OPLS-DA模型鉴定CD状态的关键代谢物。
结果解读:1)宏转录组:CD与HC相比,50条通路差异表达——丁酸盐合成通路(F. prausnitzii介导)depletion,丙酸盐合成通路(P108-PWY)富集(图2A、B);2)代谢组:CD中天门冬氨酸、丁酸盐水平降低(p<0.05),乙醇、葡萄糖水平升高(图3A),OPLS-DA显示这些代谢物是CD的关键贡献因子(图3B)。
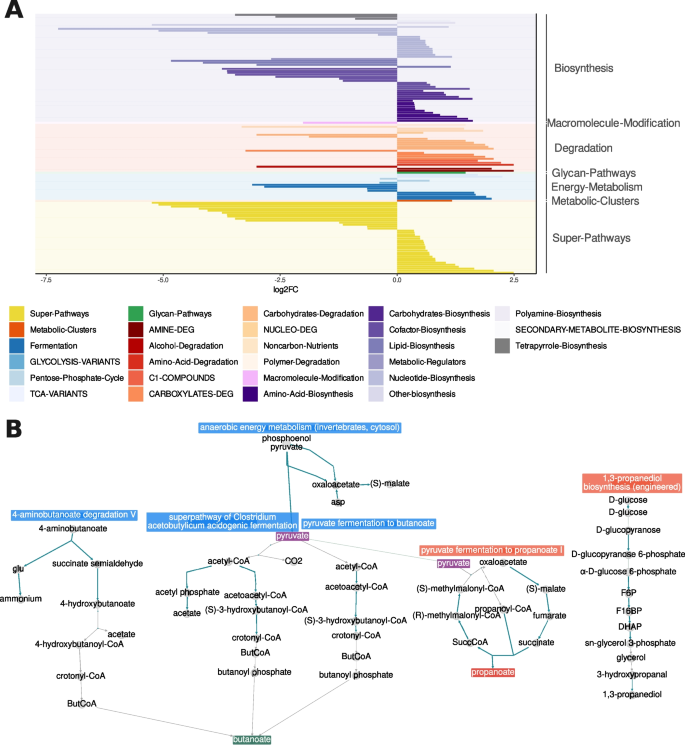
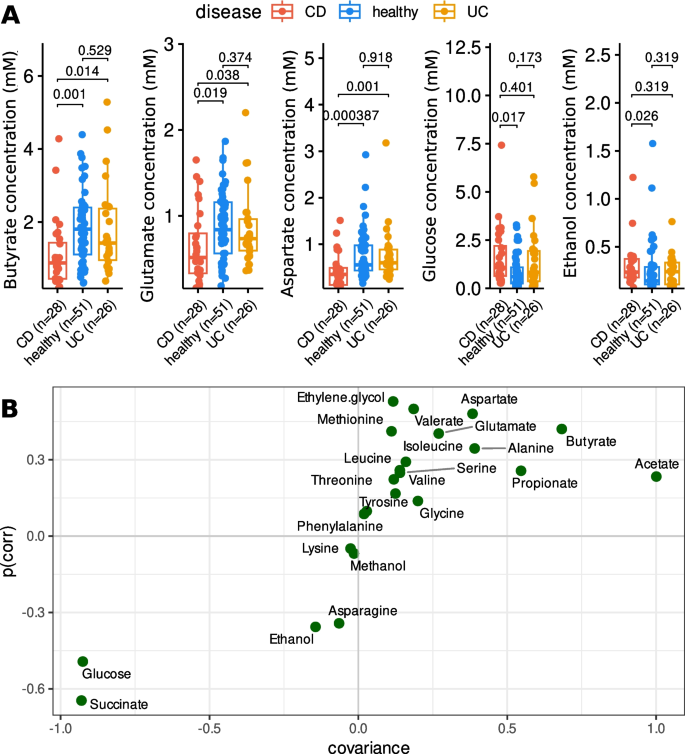
产品关联:使用nlme包进行混合效应分析,ropls包进行OPLS-DA建模。
3.5 微生物毒力因子分析
实验目的:研究CD中毒力因子的表达变化,关联“毒力因子-宿主炎症”机制。
方法细节:将宏基因组(DNA)和宏转录组(RNA)数据映射到VFDB数据库,用Bowtie2(v2.5.1)比对(过滤q-score<30的reads),混合效应线性模型分析差异表达。
结果解读:CD患者毒力因子表达显著高于HC和UC(图4A、B),其中9种来自E. coli的毒力因子(如ompA)富集——这些因子参与细菌黏附和侵袭(图4C),提示AIEC在CD炎症中的关键作用。
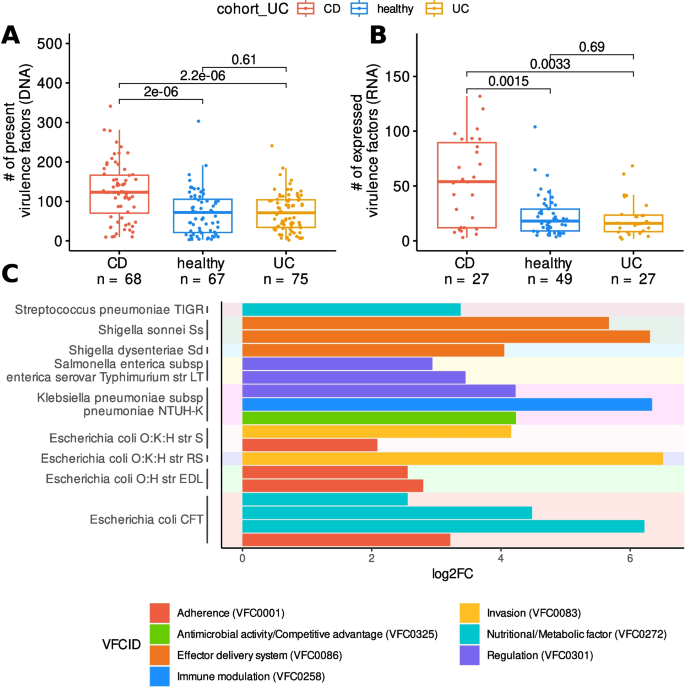
产品关联:使用Bowtie2比对,VFDB(2022版)注释毒力因子。
3.6 多组学整合分析
实验目的:整合多组学数据,揭示“微生物-代谢-毒力”协同机制。
方法细节:1)关联差异物种与代谢通路:分析E. coli与天冬氨酸消耗通路的关联;2)关联代谢通路与代谢物:分析P108-PWY(丙酸盐合成)与丙酸盐水平的关联;3)关联代谢物与毒力因子:分析丙酸盐与ompA表达的关联。
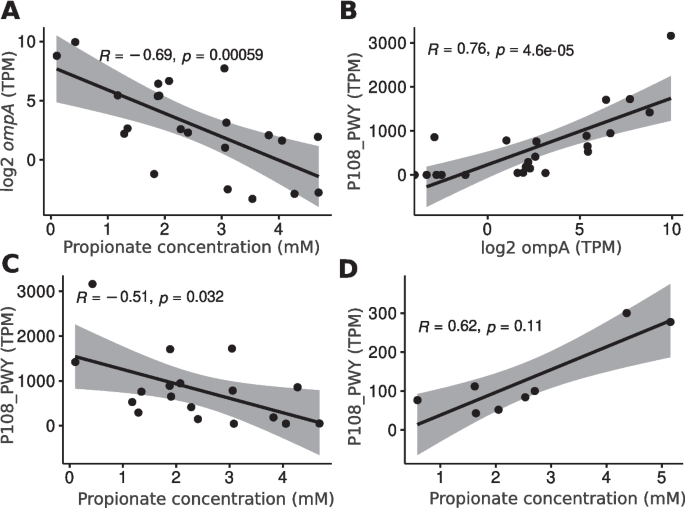
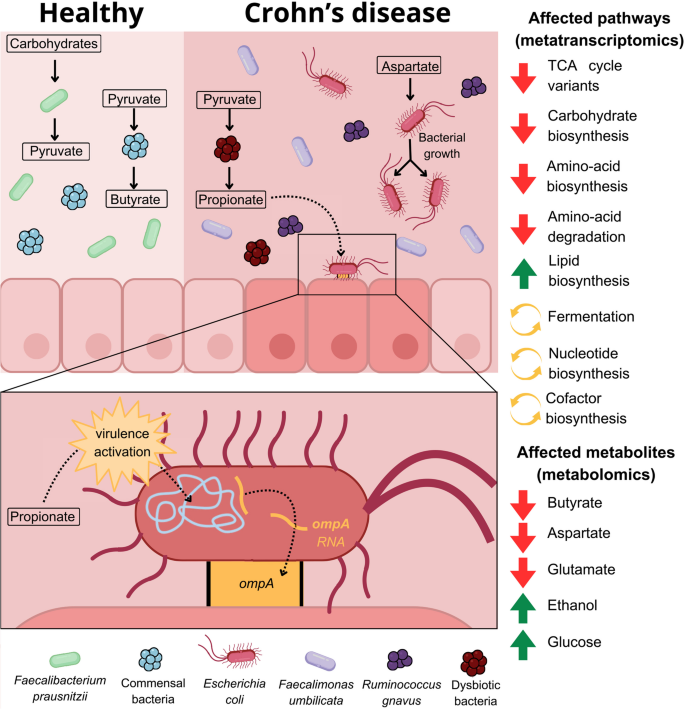
结果解读:1)E. coli在CD中富集,其介导的天冬氨酸消耗通路激活,导致天冬氨酸水平降低(削弱肠道屏障);2)P108-PWY通路在CD中激活,但丙酸盐未积累(图5B),反而与ompA表达负相关(图5A)——提示丙酸盐被用于ompA表达,促进E. coli侵袭;3)整合机制:E. coli富集→天冬氨酸消耗→肠道屏障受损;丙酸盐合成→ompA表达→细菌侵袭→宿主炎症(图6)。
产品关联:使用Spearman相关性分析关联多组学数据,无具体商业产品。
4. Biomarker研究及发现成果解析
Biomarker定位:本研究鉴定的CD生物标志物包括四类:1)20种核心物种组成的微生物面板(10种富集、10种depletion);2)新型物种Faecalimonas umbilicata;3)代谢物(天冬氨酸、丁酸盐);4)毒力因子ompA。筛选与验证逻辑为“发现队列筛选-机器学习建模-验证队列验证”:ANCOM-BC筛选差异物种,随机森林建模,独立队列验证;代谢物及毒力因子通过差异分析及关联分析确认。
研究过程详述:1)微生物面板:发现队列筛选174种差异物种,进一步筛选10种最富集(如Faecalimonas umbilicata、E. coli)和10种最depletion(如F. prausnitzii)的物种组成面板,验证队列AUC=0.942;2)Faecalimonas umbilicata:CD中显著富集(log₂FC=-9.8,FDR=5.8×10⁻¹⁸),为新型CD特异性物种;3)代谢物:天冬氨酸(CD中降低,p<0.05)、丁酸盐(CD中降低,p<0.05),OPLS-DA显示其为CD关键贡献因子;4)毒力因子ompA:CD中表达升高(p<0.05),与丙酸盐负相关(Spearman R=-0.69,FDR=0.01)。
核心成果提炼:1)20种物种面板是高特异性CD诊断Biomarker,验证集AUC=0.942,优于现有标志物;2)Faecalimonas umbilicata是新型CD物种Biomarker,为早期诊断提供新靶点;3)天冬氨酸、丁酸盐是CD肠道屏障受损的代谢标志物;4)ompA是AIEC促进CD炎症的功能标志物,其表达依赖丙酸盐代谢。这些成果首次通过多组学整合揭示CD新型Biomarker及机制,为精准治疗提供理论依据。
