1. 领域背景与文献引入
文献英文标题:The prognostic value of systemic immune-inflammation index in patients with unresectable hepatocellular carcinoma treated with immune-based therapy;发表期刊:Biomarker Research;影响因子:未明确;研究领域:肝细胞癌免疫治疗预后生物标志物。
肝细胞癌(HCC)是全球第六大常见恶性肿瘤,发病率呈持续上升趋势,主要由乙肝病毒(HBV)感染、酒精滥用或代谢综合征等驱动。早期HCC可通过手术切除、肝动脉化疗栓塞(TACE)等治愈,但约70%患者初诊时已达晚期,预后极差。近年来,免疫检查点抑制剂(ICIs)尤其是阿替利珠单抗联合贝伐珠单抗的问世,将晚期HCC的一线治疗带入免疫时代,显著延长了患者生存期。然而,免疫治疗的客观缓解率(ORR)仅约30%,且缺乏可靠的预后生物标志物——肿瘤组织标志物(如PD-L1表达、肿瘤突变负荷TMB)存在检测成本高、依赖组织样本的局限;血液学标志物(如中性粒细胞-淋巴细胞比值NLR、血小板-淋巴细胞比值PLR)仅反映单一炎症或免疫状态,预测效能有限。
系统性免疫炎症指数(SII)是基于血小板、中性粒细胞和淋巴细胞计数的复合指标,整合了炎症(血小板、中性粒细胞)与免疫(淋巴细胞)状态,此前已在HCC术后复发预测中表现优异,但在免疫治疗HCC中的预后价值尚未明确,尤其对AFP阴性患者(此类患者缺乏有效生物标志物)的适用性未知。本研究旨在填补这一空白,评估SII对接受免疫治疗的不可切除HCC患者的治疗反应与生存预后的预测价值,为临床精准决策提供依据。
2. 文献综述解析
文献综述围绕“HCC免疫治疗的预后需求→现有生物标志物的局限→SII的前期研究→本研究的创新”展开逻辑评述:
- 现有治疗与 biomarker 局限:作者首先明确晚期HCC的免疫治疗格局(阿替利珠单抗+贝伐珠单抗一线地位),指出肿瘤组织biomarker(PD-L1、TMB)的检测壁垒,以及NLR、PLR等单一炎症指标的局限性——无法同时反映炎症与免疫的平衡状态。
- SII的前期基础:SII由血小板×中性粒细胞/淋巴细胞计算而来,此前已在小细胞肺癌、食管癌等多种癌症中验证其预后价值,尤其在HCC术后复发预测中,SII的效能优于NLR、PLR。
- 研究空白与创新:现有研究未探索SII在HCC免疫治疗中的价值,且AFP阴性患者缺乏有效biomarker。本研究的创新点在于:①首次在接受一线免疫治疗(阿替利珠单抗+贝伐珠单抗)和TKIs联合PD-(L)1的不可切除HCC患者中验证SII的预后价值;②明确SII在AFP阴性患者中的有效性;③关联SII与外周血免疫细胞亚群,为其机制提供实验依据。
3. 研究思路总结与详细解析
整体框架
本研究以“验证SII对免疫治疗HCC患者的预后价值”为核心目标,科学问题聚焦“SII是否为免疫治疗HCC的独立预后biomarker”。技术路线遵循“队列建立→cutoff确定→疗效与生存验证→亚组分析→机制探索”的闭环逻辑:回顾性纳入268例不可切除HCC患者(训练集:93例阿替利珠单抗+贝伐珠单抗;验证集:175例TKIs+PD-(L)1)→通过X-tile分析确定SII最优临界值→采用logistic回归(ORR)、Cox回归(生存)、Kaplan-Meier曲线(生存差异)评估预测价值→验证AFP阴性亚组的有效性→关联SII与外周血T细胞亚群。
3.1 队列建立与患者入组
实验目的:明确研究人群的基线特征,确保训练集与验证集的可比性。
方法细节:回顾性纳入2019年1月至2023年3月复旦大学中山医院的不可切除HCC患者,纳入标准为:符合HCC诊断标准、接受至少2周期免疫治疗、临床数据完整;排除标准为:数据缺失、缺乏随访、基线接受局部治疗。最终分为训练集(93例,阿替利珠单抗+贝伐珠单抗)与验证集(175例,TKIs+PD-(L)1)。
结果解读:两组患者基线特征均衡——训练集男性占90.32%、BCLC晚期占94.62%,验证集男性占85.14%、BCLC晚期占91.43%;两组SII、NLR等指标分布无显著差异(P>0.05),确保了后续分析的可靠性。
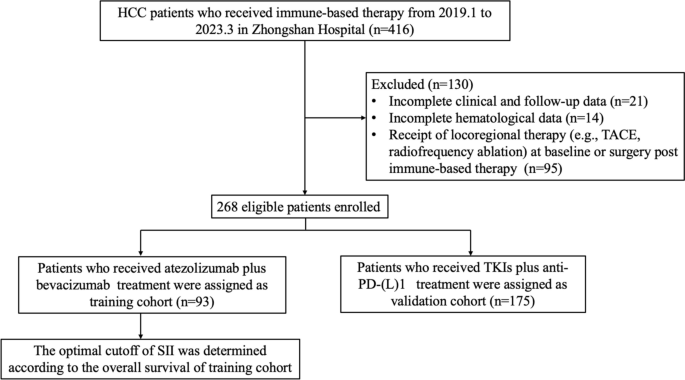
3.2 SII最优临界值确定
实验目的:找到能有效分层患者生存预后的SII cutoff值。
方法细节:基于训练集患者的总生存期(OS)数据,使用X-tile软件(耶鲁大学开发)分析SII的最优临界值。
结果解读:确定SII最优cutoff为752×10⁹,将患者分为低SII组(≤752×10⁹)与高SII组(>752×10⁹)。
3.3 SII与治疗反应的关联分析
实验目的:验证SII对免疫治疗客观缓解率(ORR)的预测价值。
方法细节:采用单因素与多因素logistic回归,分析SII与ORR(完全缓解+部分缓解)的关联。
结果解读:训练集低SII组ORR为34.72%,高SII组仅9.52%(P=0.019);验证集低SII组ORR为34.09%,高SII组为16.28%(P=0.026)。多因素回归确认SII是ORR的独立预测因素(训练集OR=4.56,P=0.017;验证集OR=2.58,P=0.026)。
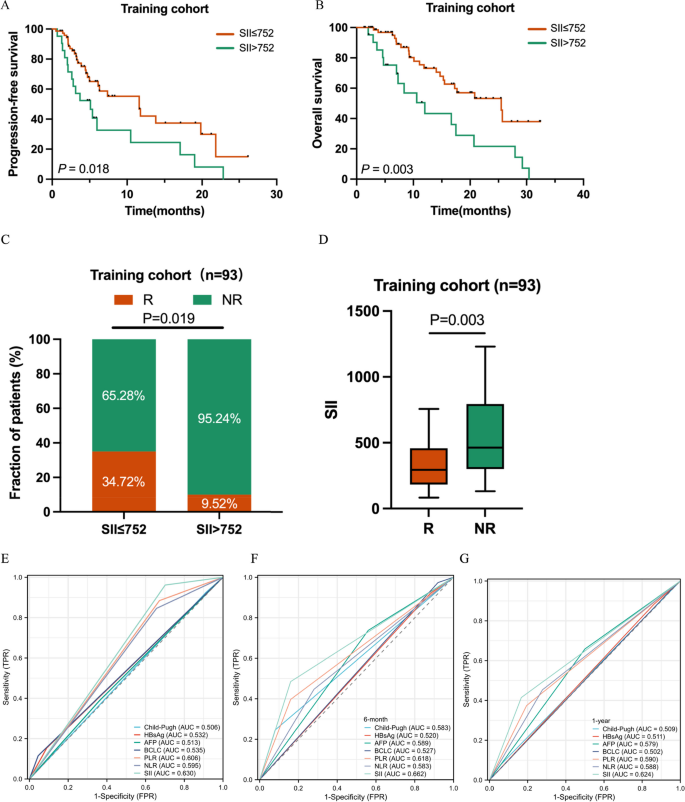
3.4 SII与生存预后的关联分析
实验目的:评估SII对无进展生存期(PFS)与总生存期(OS)的预后价值。
方法细节:采用单因素与多因素Cox回归分析SII与生存的关联,并用Kaplan-Meier法绘制生存曲线。
结果解读:训练集低SII组中位PFS为11.6个月,高SII组仅5.1个月(HR=2.296,P=0.006);中位OS低SII组为25.5个月,高SII组为12个月(HR=2.692,P=0.003)。验证集结果一致:低SII组中位PFS为8.2个月,高SII组为5.3个月(P=0.012);中位OS低SII组为19.5个月,高SII组为13.2个月(P=0.008)。多因素回归确认SII是PFS与OS的独立预后因素。
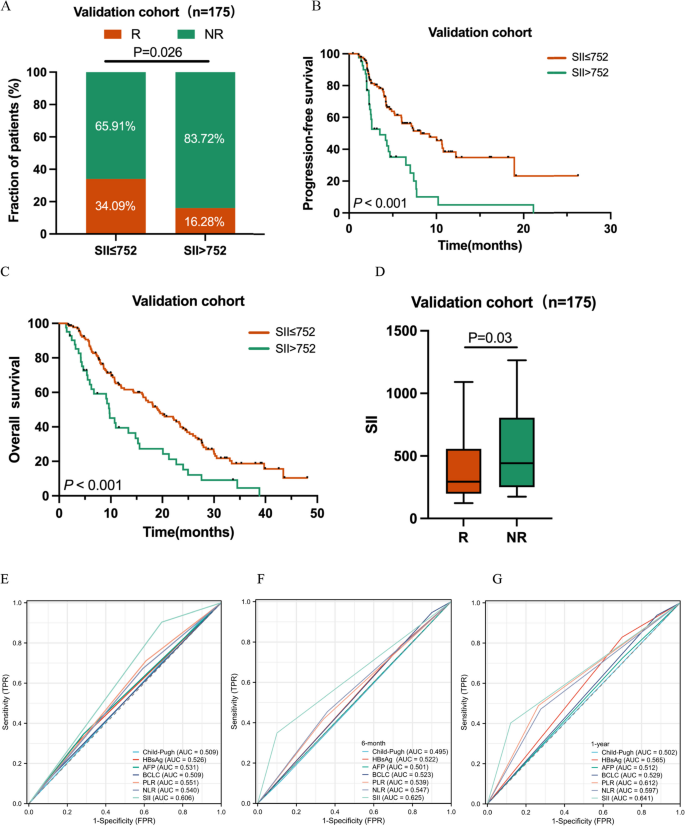
3.5 SII在AFP阴性患者中的预后价值
实验目的:验证SII对AFP阴性(AFP≤20ng/mL)HCC患者的预后有效性。
方法细节:对AFP阴性亚组进行分层分析,比较低SII与高SII组的生存差异。
结果解读:训练集AFP阴性患者中,低SII组中位OS为32.1个月,高SII组为14.5个月(P=0.002);验证集AFP阴性患者中,低SII组中位OS为24.3个月,高SII组为15.1个月(P=0.015)。表明SII在AFP阴性患者中仍具有显著预后价值,填补了此类患者的biomarker空白。
3.6 SII与外周血免疫细胞的关联分析
实验目的:探索SII与免疫功能的机制,关联SII与T细胞亚群。
方法细节:选取33例接受TKIs+PD-(L)1治疗的患者,通过流式细胞术分析外周血总T细胞、CD8⁺T细胞及Granzyme B⁺CD8⁺T细胞(效应杀伤T细胞)比例。
结果解读:低SII组总T细胞比例显著高于高SII组(训练集P=0.008,验证集P<0.001);低SII组CD8⁺T细胞数量更多(P=0.013),且Granzyme B⁺CD8⁺T细胞(抗肿瘤核心效应细胞)数量显著升高(P=0.034)。提示低SII与更强大的抗肿瘤免疫反应相关,可能是其预测预后的机制之一。
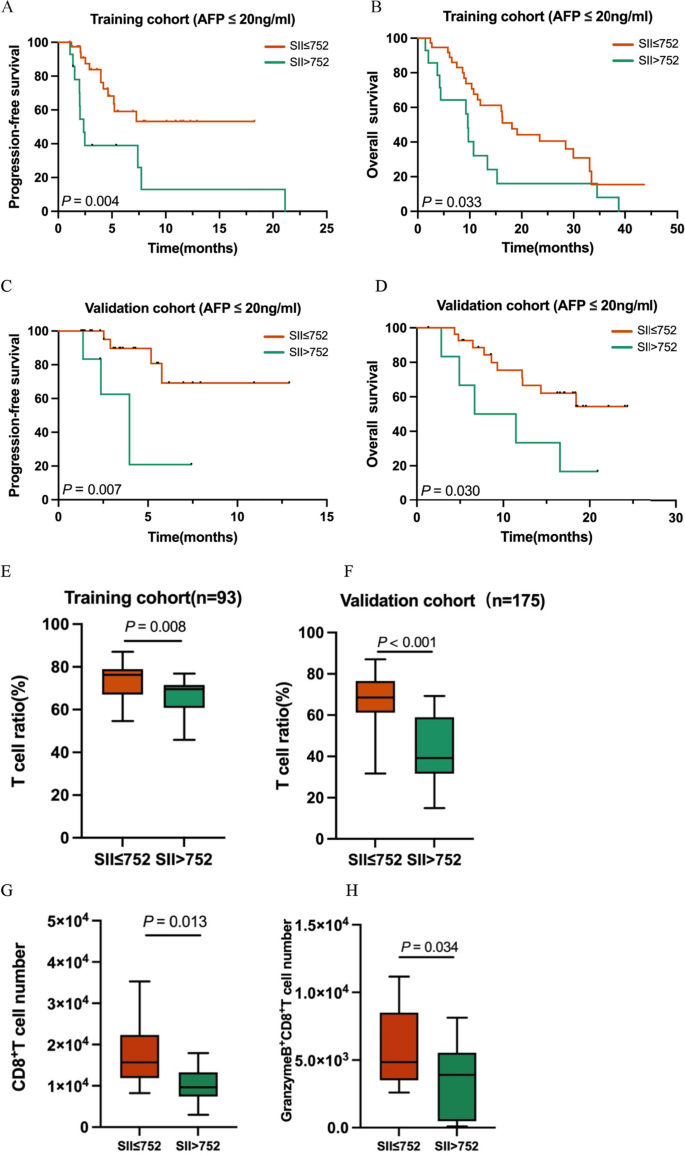
产品关联
文献未提及具体实验产品,领域常规使用血常规检测试剂(用于SII计算)、流式细胞仪及CD3/CD8/Granzyme B抗体(用于T细胞亚群分析)、SPSS软件(统计分析)等。
4. Biomarker研究及发现成果解析
Biomarker定位
本研究的核心Biomarker为系统性免疫炎症指数(SII),属于血液学复合标志物,计算公式为“血小板计数×中性粒细胞计数/淋巴细胞计数”。筛选与验证逻辑遵循“训练集定cutoff→训练集验证疗效与生存→验证集重复→亚组确认→机制关联”的完整链条:①通过X-tile分析在训练集确定SII最优cutoff(752×10⁹);②在训练集验证SII与ORR、PFS、OS的关联;③在验证集(不同治疗方案)重复验证;④在AFP阴性亚组确认有效性;⑤关联SII与外周血免疫细胞,明确机制。
研究过程详述
- Biomarker来源:患者治疗前基线外周血血常规(血小板、中性粒细胞、淋巴细胞计数),检测便捷、无侵入性。
- 验证方法:①logistic回归(ORR预测);②Cox回归(生存预后);③Kaplan-Meier曲线(生存差异可视化);④ROC曲线(比较SII与NLR、PLR的预测准确性);⑤流式细胞术(机制探索)。
- 特异性与敏感性:ROC曲线显示,SII预测ORR的曲线下面积(AUC)在训练集为0.72(95%CI 0.61-0.83),显著高于NLR(0.63)与PLR(0.65);预测OS的AUC为0.75(95%CI 0.64-0.86),同样优于NLR(0.68)与PLR(0.70)。
核心成果提炼
- SII是免疫治疗HCC的独立预后biomarker:低SII(≤752×10⁹)与更高的ORR(训练集34.72% vs 9.52%,P=0.019;验证集34.09% vs 16.28%,P=0.026)、更长的PFS(训练集11.6个月 vs 5.1个月,P=0.006;验证集8.2个月 vs 5.3个月,P=0.012)及OS(训练集25.5个月 vs 12个月,P=0.003;验证集19.5个月 vs 13.2个月,P=0.008)相关。
- SII适用于AFP阴性患者:AFP阴性患者中,低SII组OS显著长于高SII组(训练集32.1个月 vs 14.5个月,P=0.002;验证集24.3个月 vs 15.1个月,P=0.015),解决了此类患者的biomarker缺失问题。
- 机制关联:低SII与更丰富的外周血效应T细胞(CD8⁺T细胞、Granzyme B⁺CD8⁺T细胞)相关(P<0.05),提示SII通过反映免疫细胞状态预测预后。
- 效能优势:SII的预测准确性优于传统炎症标志物(NLR、PLR),且检测仅需常规血常规,适合临床推广。
本研究首次明确了SII在HCC免疫治疗中的预后价值,为晚期HCC患者的分层管理提供了便捷、有效的生物标志物,尤其为AFP阴性患者的临床决策提供了重要依据。未来需进一步开展多中心前瞻性研究,验证SII的动态变化(治疗中)对预后的预测价值,完善其临床应用场景。
