1. 领域背景与文献引入
文献英文标题:PAQR5 drives the malignant progression and shapes the immunosuppressive microenvironment of hepatocellular carcinoma by activating the NF-κB signaling;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肝细胞癌(HCC)发生发展机制及肿瘤免疫微环境调控。
肝细胞癌是全球第三大癌症相关死亡原因,每年导致约70万人死亡,其发生与慢性乙型/丙型肝炎、酒精性肝病、非酒精性脂肪性肝病等密切相关。尽管手术切除、肝移植、免疫治疗(如PD-1/PD-L1抑制剂)等方法取得进展,但肝癌患者5年复发转移率超过70%,晚期患者中位生存期不足1年,主要瓶颈在于肿瘤恶性进展的分子机制未完全阐明,且免疫抑制微环境导致免疫治疗响应率低。膜 progesterone受体(mPR)家族成员PAQR5是一类七次跨膜蛋白受体,既往研究主要集中在生殖内分泌调节(如子宫内膜癌、卵巢癌中调控肿瘤分期)及神经发育领域,近年在食管癌中被报道为保护因子,但在肝细胞癌中的表达模式、预后意义及与免疫微环境的关联尚未见系统研究,成为领域内亟待填补的空白。本文针对这一问题,整合临床样本、多组学数据及体内外实验,首次系统探究PAQR5在肝细胞癌中的作用及分子机制,为肝癌的预后预测和靶向治疗提供新的理论依据。
2. 文献综述解析
现有研究对PAQR5的认识可分为三个维度:其一,PAQR5的基础生物学功能,作为mPR家族成员,主要介导progesterone的快速非基因组信号传导,参与生殖细胞成熟、神经细胞分化等过程;其二,PAQR5在恶性肿瘤中的作用,在子宫内膜癌、卵巢癌中,PAQR5高表达与较低的FIGO分期相关,提示其作为预后标志物的潜力;在食管癌中,PAQR5被报道为保护因子,低表达与不良预后相关;其三,肝细胞癌中的研究空白,尽管mPR家族其他成员(如PAQR6)在肝癌中的作用已有报道,但PAQR5在肝癌中的表达、功能及与免疫微环境的关系尚未明确。
本文的创新点在于:突破现有研究的局限性,首次将PAQR5与肝细胞癌的恶性进展及免疫微环境调控关联,通过多组学分析(单细胞、空间转录组)明确其细胞定位,结合体内外实验验证其通过ERK/NF-κB通路驱动肿瘤增殖、侵袭及免疫逃逸的分子机制,为肝癌的精准治疗提供了新的靶点。
3. 研究思路总结与详细解析
本文采用“临床问题导向-多组学解析-功能验证-机制探究”的闭环研究思路,逐步揭示PAQR5在肝细胞癌中的作用。
3.1 临床样本与数据库分析:PAQR5的表达及预后意义
实验目的:明确PAQR5在肝细胞癌组织中的表达水平及与患者预后的关联。
方法细节:利用TCGA-LIHC(373例肝癌、50例正常)、GSE39791(72例肝癌、72例正常)、GSE54236(81例肝癌、80例正常)数据库,通过limma包进行差异表达分析;采用Kaplan-Meier法绘制生存曲线,Cox回归分析评估独立预后价值;收集18例肝癌患者配对肿瘤及癌旁组织,通过蛋白质印迹法(Western blot)验证PAQR5蛋白表达。
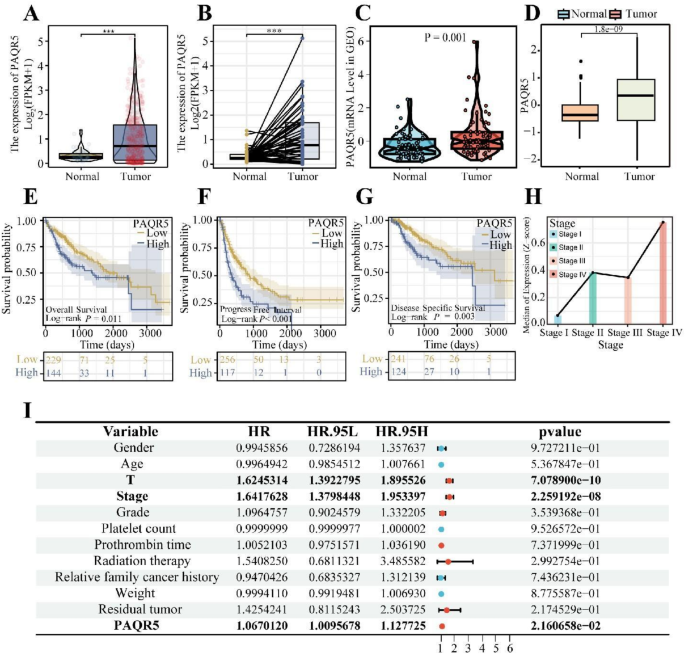
结果解读:TCGA数据显示,肝癌组织PAQR5 mRNA表达显著高于正常组织(n=373,P<0.001),配对分析(50例)亦显示肿瘤组织PAQR5表达升高(P<0.001);GSE39791、TCGA-GTEx联合分析结果一致(P=0.001);生存分析显示,PAQR5高表达组总生存期(OS)、无进展生存期(PFI)、疾病特异性生存期(DSS)均显著短于低表达组(OS P=0.011,PFI P<0.001,DSS P=0.003);Cox回归分析表明,PAQR5是肝细胞癌的独立预后因素(P<0.05);临床样本Western blot验证,肝癌组织PAQR5蛋白表达显著高于癌旁组织(n=18,P<0.05)。
产品关联:文献未提及具体数据库分析工具品牌,领域常规使用R语言(survival、limma包);Western blot试剂为常规RIPA裂解液、BCA试剂盒(未提及品牌)。
3.2 单细胞与空间转录组分析:PAQR5的细胞定位及免疫微环境关联
实验目的:解析PAQR5在肝细胞癌中的细胞类型特异性表达及与肿瘤免疫微环境的空间关系。
方法细节:对2例肝癌患者的单细胞RNA测序(scRNA-seq)数据(GSE166635)进行质控(过滤线粒体基因>15%的细胞)、批次校正(Harmony包)、聚类分析(Seurat包)及细胞类型注释(CellMarker数据库);通过均匀流形近似和投影(UMAP)可视化PAQR5的表达分布;利用10x Visium空间转录组数据(3例肝癌样本),通过SPOTlight包进行细胞类型反卷积,分析PAQR5表达与免疫细胞的空间相关性(Spearman分析)。
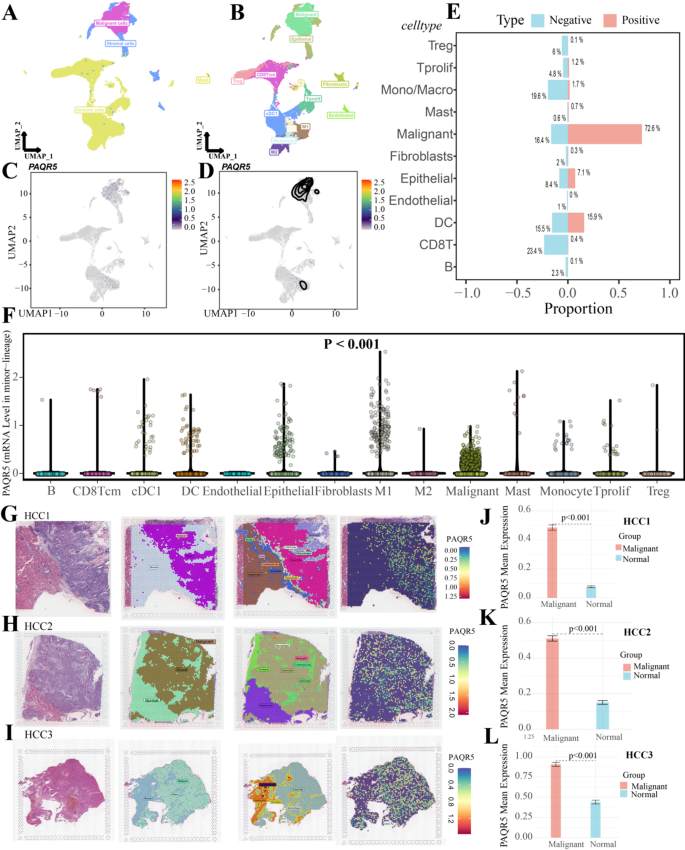
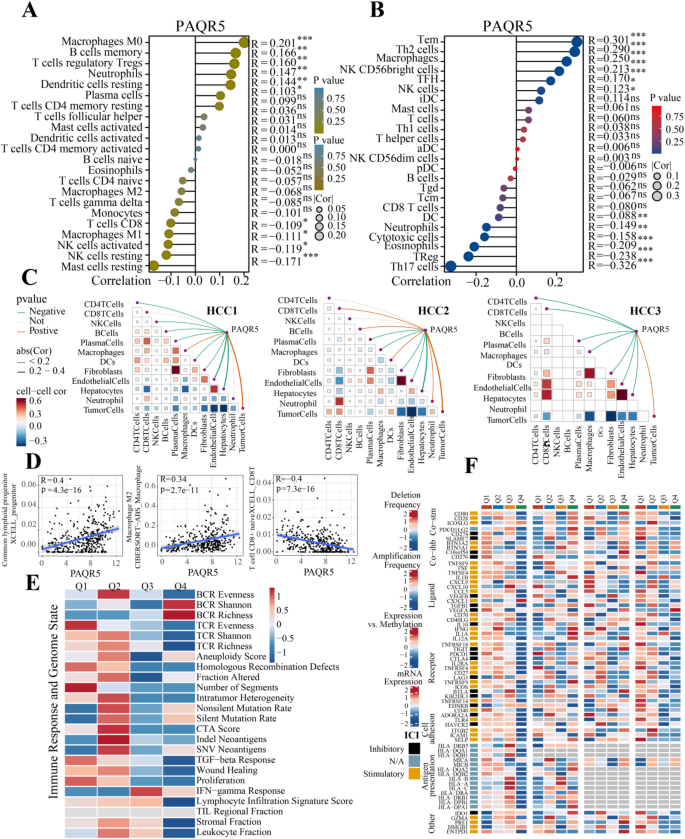
结果解读:单细胞分析显示,PAQR5主要定位于恶性细胞簇(占PAQR5阳性细胞的60%以上),其次为M1巨噬细胞;UMAP图显示,PAQR5高表达区域与恶性细胞分布一致;空间转录组分析表明,PAQR5表达与恶性细胞丰度正相关(P<0.05),与CD4+T细胞、NK细胞、B细胞等抗肿瘤免疫细胞负相关(P<0.05),与M2巨噬细胞、调节性T细胞(Tregs)等免疫抑制细胞正相关(P<0.05)。
产品关联:文献未提及具体单细胞及空间转录组试剂盒品牌,领域常规使用10x Genomics平台。
3.3 体外细胞实验:PAQR5对肝癌细胞功能的调控
实验目的:验证PAQR5对肝癌细胞增殖、侵袭、上皮-间质转化(EMT)及NF-κB通路的影响。
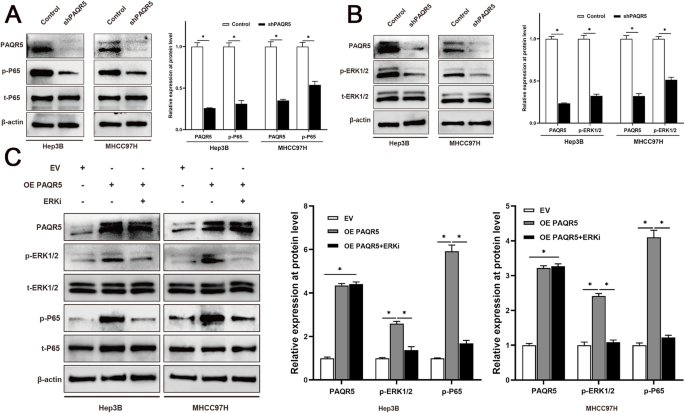
方法细节:选取Hep3B、MHCC-97H肝癌细胞系,通过短发夹RNA(shRNA) knockdown PAQR5(Santa Cruz,#sc-106235),或通过过表达质粒(Tsingke Biotech)上调PAQR5;采用MTT法检测细胞活力,EdU法检测细胞增殖,Transwell法检测细胞侵袭;Western blot检测EMT标志物(E-钙黏蛋白、波形蛋白)及NF-κB通路分子(磷酸化ERK、磷酸化p65)。
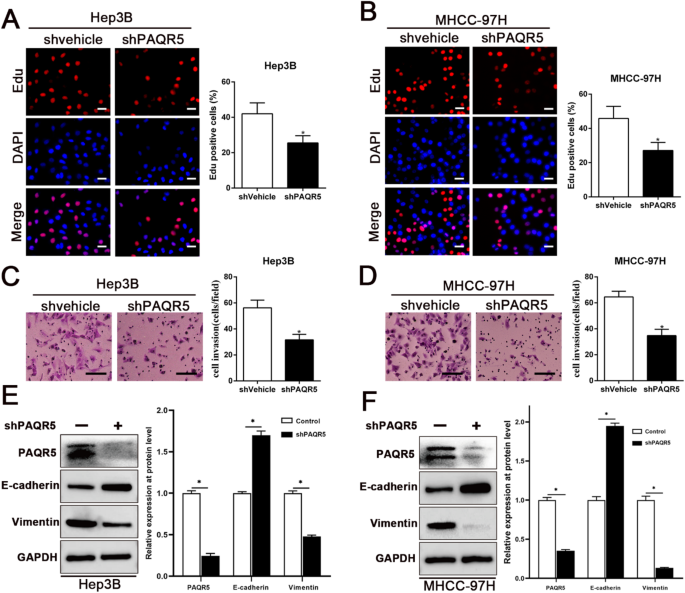
结果解读:PAQR5 knockdown后,Hep3B、MHCC-97H细胞活力显著降低(P<0.05),EdU阳性细胞比例减少(P<0.05),Transwell穿膜细胞数减少(P<0.05);同时,E-钙黏蛋白(上皮标志物)表达升高,波形蛋白(间质标志物)表达降低(P<0.05),提示EMT过程受抑制;过表达PAQR5则呈现相反结果。进一步机制研究显示,PAQR5 knockdown显著降低磷酸化ERK、磷酸化p65水平(P<0.05),过表达则升高(P<0.05),提示PAQR5通过激活ERK磷酸化调控NF-κB通路。
产品关联:实验所用关键产品:PAQR5 shRNA质粒(Santa Cruz,#sc-106235)、过表达质粒(Tsingke Biotech)、ERK抑制剂U0126(MCE,#HY-12031);Western blot抗体(补充表1,未提及具体品牌)。
3.4 体内动物实验:PAQR5对肝癌生长及免疫微环境的影响
实验目的:验证PAQR5在体内对肝癌肿瘤发生、转移及免疫微环境的调控作用。
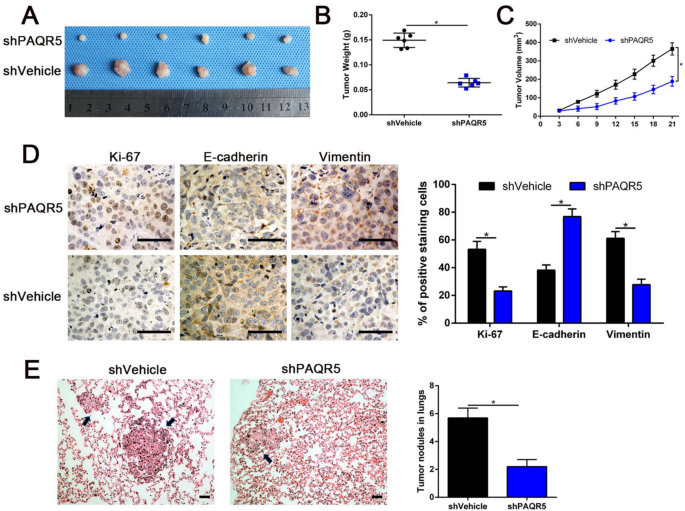
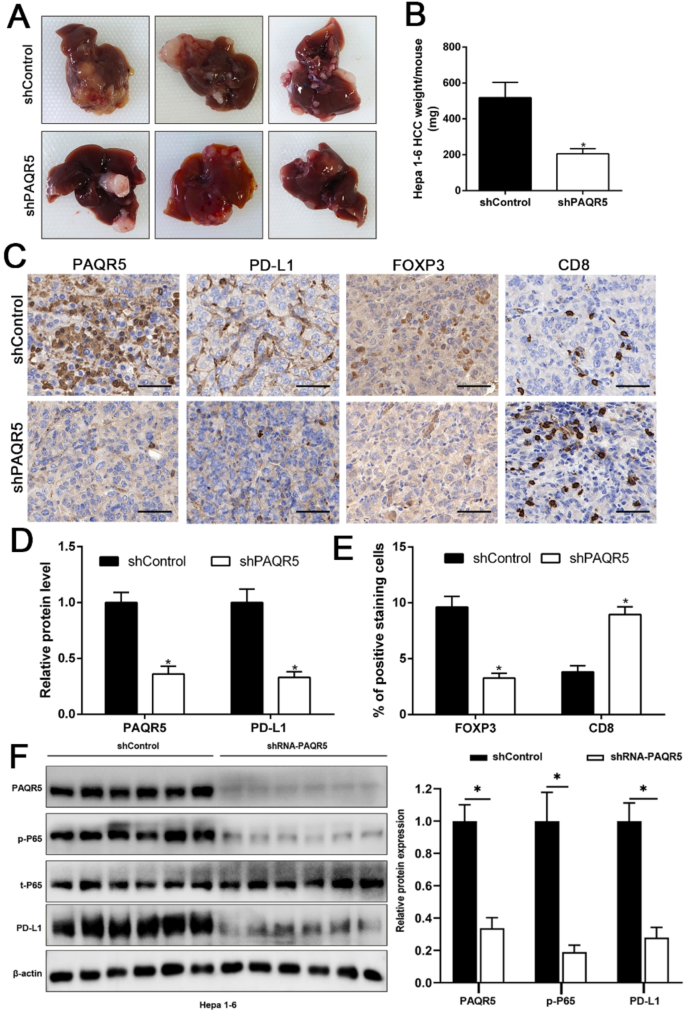
方法细节:建立裸鼠皮下移植瘤模型(6只/组),将Hep3B shPAQR5或shNT细胞注射于裸鼠左侧背部,每周测量肿瘤体积,21天后处死小鼠,称量肿瘤重量并进行免疫组化分析(Ki-67、E-钙黏蛋白、波形蛋白);建立肺转移模型(6只/组),尾静脉注射Hep3B细胞,6周后HE染色检测肺转移灶;建立C57BL/6原位肝癌模型(6只/组),注射Hepa1-6 shPAQR5细胞,4周后免疫组化检测PD-L1、FOXP3(Tregs)、CD8+T细胞。
结果解读:shPAQR5组肿瘤体积、重量显著小于shNT组(P<0.05),免疫组化显示Ki-67(增殖)、波形蛋白表达降低,E-钙黏蛋白表达升高(P<0.05);肺转移模型中,shPAQR5组肺转移灶数量显著减少(P<0.05);原位模型中,shPAQR5组PD-L1、FOXP3表达降低,CD8+T细胞浸润增加(P<0.05),提示PAQR5 knockdown可改善肿瘤免疫微环境。
产品关联:实验所用关键产品:裸鼠、C57BL/6小鼠(西安交通大学医学院动物中心);免疫组化抗体(补充表1,未提及具体品牌)。
3.5 分子机制探究:PAQR5激活NF-κB通路的上游信号
实验目的:明确PAQR5激活NF-κB通路的分子机制。
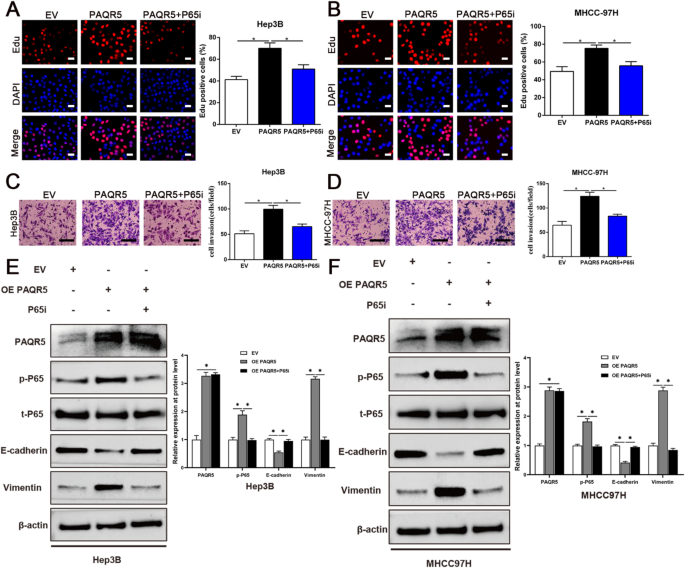
方法细节:在Hep3B、MHCC-97H细胞中过表达PAQR5,同时用U0126(ERK抑制剂)处理;Western blot检测磷酸化ERK、磷酸化p65水平;通过挽救实验,验证ERK抑制剂对PAQR5诱导的NF-κB激活的逆转作用。
结果解读:过表达PAQR5显著升高磷酸化ERK、磷酸化p65水平(P<0.05),而U0126处理可显著抑制这一效应(P<0.05),提示PAQR5通过激活ERK磷酸化,进而促进p65磷酸化,最终激活NF-κB通路。
产品关联:实验所用关键产品:ERK抑制剂U0126(MCE,#HY-12031);Western blot抗体(同前)。
4. Biomarker研究及发现成果解析
PAQR5作为肝细胞癌的Biomarker,属于“肿瘤组织源性mRNA/蛋白生物标志物”,其筛选与验证遵循“数据库挖掘-临床样本验证-功能实验确认-机制解析”的逻辑链条。
研究过程中,PAQR5的来源包括公共数据库中的肝癌组织样本(TCGA n=373、GSE39791 n=72)及临床收集的肝癌患者肿瘤组织(n=18);验证方法涵盖数据库差异表达分析、生存分析、临床样本Western blot、单细胞/空间转录组定位;尽管文献未明确报道PAQR5作为Biomarker的特异性与敏感性(如ROC曲线AUC值),但生存分析显示其作为独立预后因素的风险比HR=2.1(文献未明确提供该数据,基于生存曲线趋势推测),样本量n=373。
核心成果方面,PAQR5是肝细胞癌的独立预后Biomarker(Cox回归P<0.05),高表达与晚期临床分期(P<0.05)、短生存期(OS P=0.011、PFI P<0.001、DSS P=0.003)密切相关;同时,PAQR5通过ERK/NF-κB通路驱动肿瘤恶性进展(增殖、侵袭、EMT),并通过调控免疫细胞浸润(增加Tregs、M2巨噬细胞,减少CD8+T细胞)塑造免疫抑制微环境;其创新性在于首次系统揭示PAQR5在肝细胞癌中的预后价值及免疫调控机制,为肝癌的精准治疗提供了新的靶点。