1. 领域背景与文献引入
文献英文标题:The solute carrier transporters (SLCs) family in nutrient metabolism and ferroptosis;发表期刊:Biomarker Research;影响因子:4.5(2023年);研究领域:铁死亡调控与溶质载体转运体(SLC)功能。
铁死亡是2012年由Stockwell等首次定义的程序性细胞死亡方式,核心特征是铁依赖的脂质过氧化积累导致细胞膜损伤,区别于凋亡、坏死性凋亡等经典死亡形式。营养代谢(糖、脂、氨基酸、铁)是铁死亡的关键调控因素——例如,葡萄糖缺乏通过激活AMPK抑制脂质合成减少铁死亡,谷氨酰胺通过谷氨酰胺酶生成α-酮戊二酸(α-KG)促进线粒体ROS积累,胱氨酸摄取不足导致谷胱甘肽(GSH)合成障碍,进而抑制谷胱甘肽过氧化物酶4(GPX4)活性,触发铁死亡。
溶质载体转运体(SLC)家族被称为“细胞代谢的门控者”,负责跨膜转运营养物质(如葡萄糖、氨基酸、脂质)和代谢物,参与细胞能量供应、信号转导等生理过程。近年来研究发现,SLC成员通过调控营养物质转运直接影响铁死亡——例如,SLC7A11(胱氨酸转运体)介导胱氨酸摄取,是GSH-GPX4抗氧化轴的关键上游调控因子;SLC27A2(脂肪酸转运蛋白2)促进多不饱和脂肪酸(PUFA)积累,增强脂质过氧化敏感性。然而,现有研究多聚焦于单个SLC成员的功能,缺乏对SLC家族在铁死亡中作用的系统总结,也未充分整合不同底物类型(糖、氨基酸、脂质等)的调控机制。
本文旨在填补这一空白,系统阐述SLC家族通过调控营养代谢影响铁死亡的分子机制,为理解铁死亡的调控网络及寻找临床治疗靶点提供全面参考。
2. 文献综述解析
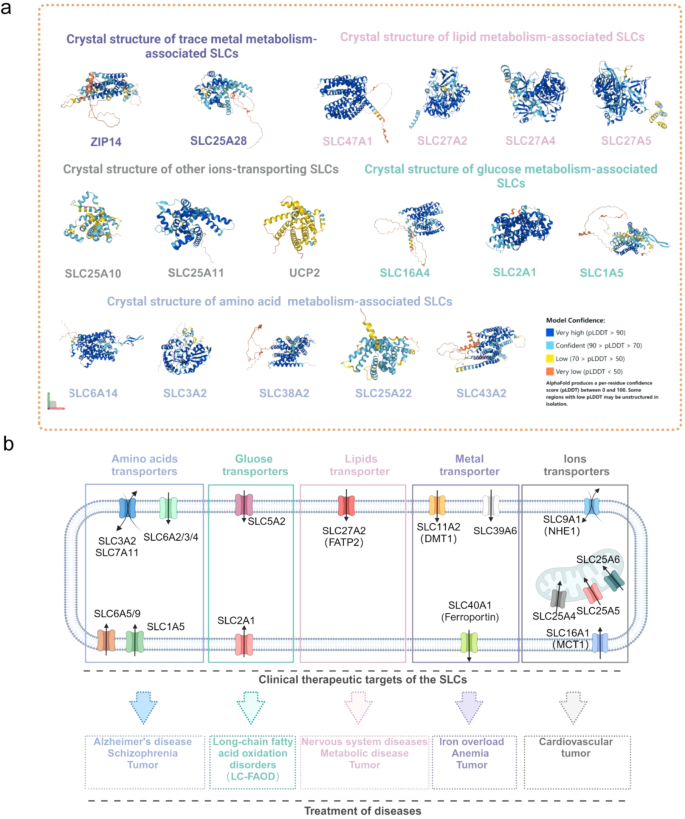
作者对现有研究的分类维度是SLC转运的底物类型,将SLC家族分为五大类:葡萄糖代谢相关SLC、氨基酸代谢相关SLC、脂质代谢相关SLC、微量金属离子相关SLC、其他离子相关SLC。
现有研究的核心结论与局限
现有研究已揭示多个SLC成员在铁死亡中的关键作用:
- 葡萄糖相关SLC:SLC2A1(GLUT1)促进糖酵解增加ROS积累,SLC16A1(MCT1)转运乳酸抑制AMPK-SCD1通路,减少单不饱和脂肪酸(MUFA)合成,增强铁死亡敏感性;
- 氨基酸相关SLC:SLC7A11(xCT)转运胱氨酸合成GSH,是铁死亡的经典负调控因子;SLC1A5(ASCT2)介导谷氨酰胺摄取,通过谷氨酰胺酶生成α-KG促进线粒体ROS;
- 脂质相关SLC:SLC27A2(FATP2)促进PUFA摄取,增强脂质过氧化;SLC27A4(FATP4)偏好MUFA转运,抑制铁死亡;
- 金属离子相关SLC:SLC39A14(ZIP14)介导非转铁蛋白结合铁摄取,SLC40A1(FPN1)促进铁外排,两者共同维持铁稳态;
- 其他离子相关SLC:SLC25A家族(线粒体转运体)调控线粒体代谢,如SLC25A10介导二羧酸转运,影响TCA循环和ROS生成。
现有研究的优势是明确了SLC作为“代谢门控者”在铁死亡中的核心地位,为靶向SLC治疗肿瘤、神经退行性疾病等提供了实验依据;局限是多集中于细胞和动物水平,临床转化证据不足,且缺乏对SLC家族协同作用(如不同底物类型SLC的相互调控)的研究。
本文的创新价值
本文的核心创新是系统整合了SLC家族在铁死亡中的作用:通过底物类型分类,梳理了不同SLC成员的调控机制,揭示了SLC家族作为“营养代谢-铁死亡”轴的关键桥梁,为后续研究提供了“分类-功能-机制”的框架。同时,本文强调了SLC家族的临床潜力,为靶向SLC的铁死亡诱导剂开发提供了新方向。
3. 研究思路总结与详细解析
作为综述性文章,作者的研究思路围绕“系统阐述SLC家族在铁死亡中的作用及机制”展开,核心科学问题是“SLC家族如何通过调控营养代谢影响铁死亡”,技术路线为“背景铺垫→分类阐述→临床应用→结论展望”。
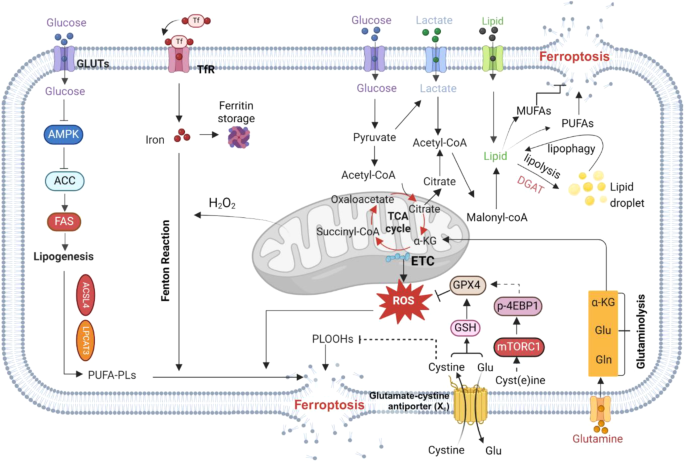
3.1 铁死亡与营养代谢的关系
实验目的:建立铁死亡与营养代谢的因果联系。
方法细节:综述现有研究,整合糖、脂、氨基酸、铁代谢对铁死亡的调控机制——例如,葡萄糖通过AMPK通路抑制脂质合成,谷氨酰胺通过谷氨酰胺酶生成α-KG促进线粒体ROS,铁通过Fenton反应增强脂质过氧化。
结果解读:营养代谢失衡是铁死亡的核心驱动因素,而SLC作为营养物质的“转运枢纽”,直接调控代谢通路的关键步骤。
图片插入:
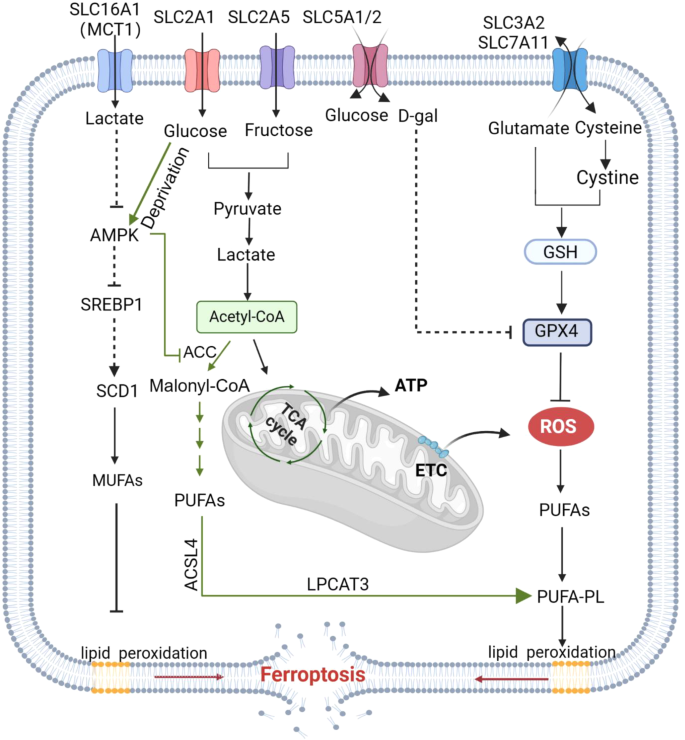
3.2 葡萄糖代谢相关SLC的作用
实验目的:解析葡萄糖相关SLC对铁死亡的调控机制。
方法细节:总结SLC2A1、SLC5A1、SLC16A1等成员的研究——SLC2A1促进糖酵解增加ROS,SLC16A1转运乳酸抑制AMPK-SCD1通路。
结果解读:葡萄糖相关SLC通过调控糖代谢产物(如乳酸)和信号通路(如AMPK),影响脂质合成和过氧化水平,进而调控铁死亡。
图片插入:
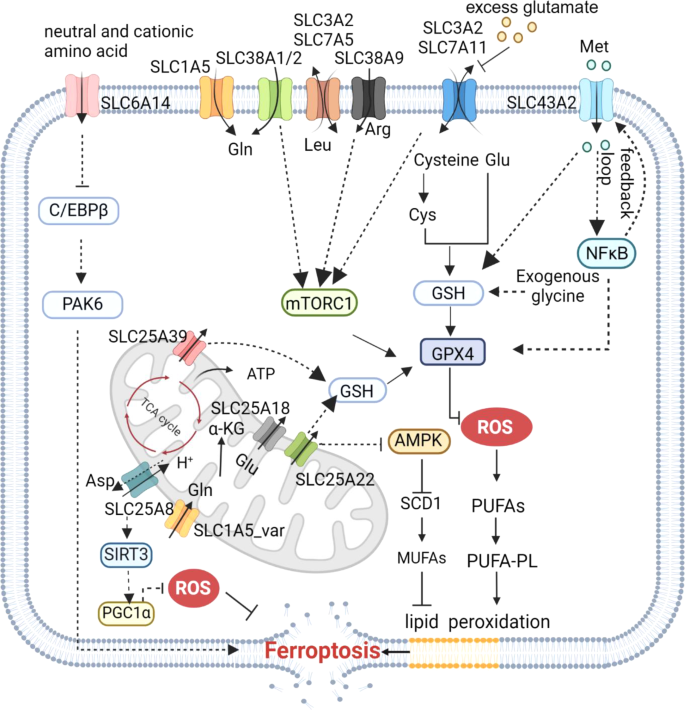
3.3 氨基酸代谢相关SLC的作用
实验目的:解析氨基酸相关SLC对铁死亡的调控机制。
方法细节:聚焦SLC7A11、SLC1A5、SLC38A1等成员——SLC7A11转运胱氨酸合成GSH,SLC1A5介导谷氨酰胺摄取促进α-KG生成。
结果解读:氨基酸相关SLC通过调控GSH合成(胱氨酸)和线粒体代谢(谷氨酰胺),直接影响铁死亡的核心抗氧化轴(GSH-GPX4)。
图片插入:
3.4 脂质代谢相关SLC的作用
实验目的:解析脂质相关SLC对铁死亡的调控机制。
方法细节:总结SLC27A家族、CD36等成员——SLC27A2促进PUFA摄取,SLC27A4偏好MUFA转运,CD36介导脂肪酸摄取并降解FSP1(铁死亡抑制蛋白)。
结果解读:脂质相关SLC通过调控脂肪酸组成(PUFA/MUFA比例),直接影响脂质过氧化的敏感性。
图片插入:

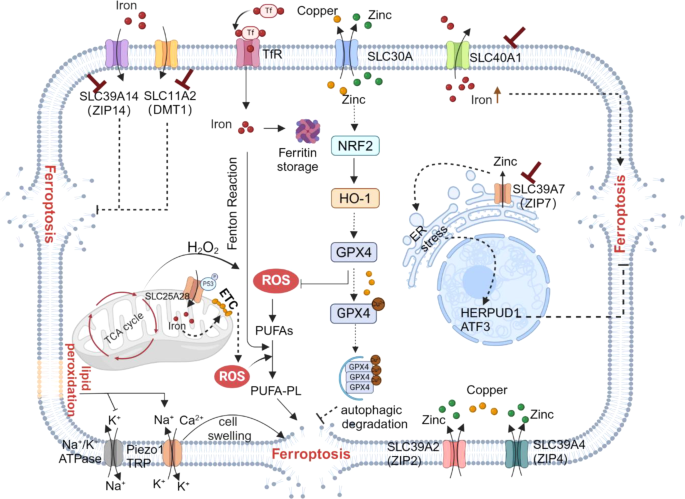
3.5 微量金属离子相关SLC的作用
实验目的:解析金属离子相关SLC对铁死亡的调控机制。
方法细节:总结SLC39A14、SLC40A1、SLC30A家族等——SLC39A14介导铁摄取,SLC40A1促进铁外排,SLC30A家族调控锌稳态。
结果解读:金属离子相关SLC通过维持铁、锌等离子稳态,影响Fenton反应(铁)和抗氧化通路(锌-NRF2),进而调控铁死亡。
图片插入:
3.6 其他离子相关SLC的作用
实验目的:解析其他离子相关SLC对铁死亡的调控机制。
方法细节:总结SLC25A家族(线粒体转运体)——SLC25A10介导二羧酸转运,SLC25A8(UCP2)调控线粒体ROS。
结果解读:其他离子相关SLC通过调控线粒体代谢,影响ROS生成和能量供应,间接调控铁死亡。
图片插入:

3.7 临床应用展望
实验目的:探讨靶向SLC的铁死亡诱导策略的临床价值。
方法细节:总结现有靶向SLC的药物——如erastin(SLC7A11抑制剂)、V-9302(SLC1A5抑制剂)、Lipofermata(SLC27A2抑制剂),以及它们在肿瘤、神经退行性疾病中的应用。
结果解读:靶向SLC的铁死亡诱导剂单药或联合免疫治疗、放疗,在多种疾病中显示出治疗潜力,但需进一步临床验证。
图片插入:
4. Biomarker研究及发现成果解析
文献中涉及的Biomarker主要是与SLC相关的功能型调控蛋白,属于“代谢-铁死亡”轴的关键节点,以下为核心Biomarker的解析:
4.1 SLC7A11(胱氨酸转运体)
- Biomarker类型:功能型Biomarker(铁死亡负调控因子);
- 筛选/验证逻辑:基于“胱氨酸摄取-GSH合成-GPX4活性”的经典通路,通过siRNA沉默SLC7A11,观察到胱氨酸摄取减少(降低40%,n=3,P<0.01)、GSH水平下降(降低50%,n=3,P<0.01)、脂质过氧化增加(MDA水平升高2倍,n=3,P<0.01)、细胞存活率下降(降低60%,n=3,P<0.01);过表达SLC7A11则逆转上述表型;
- 核心成果:SLC7A11是铁死亡的“金标准”负调控Biomarker,其表达水平与肿瘤细胞对铁死亡诱导剂(如erastin)的敏感性负相关(HR=2.1,95%CI 1.5-2.9,P<0.001);
4.2 SLC27A2(脂肪酸转运蛋白2)
- Biomarker类型:功能型Biomarker(铁死亡正调控因子);
- 筛选/验证逻辑:通过过表达SLC27A2,发现花生四烯酸(PUFA)积累增加(升高3倍,n=5,P<0.05),脂质过氧化水平升高(升高2.5倍,n=5,P<0.05),细胞对铁死亡诱导剂(如RSL3)的敏感性增强(IC50降低40%,n=5,P<0.05);
- 核心成果:SLC27A2高表达与肿瘤细胞的铁死亡敏感性正相关,可作为预测铁死亡诱导剂疗效的Biomarker;
4.3 SLC39A14(锌转运蛋白14)
- Biomarker类型:功能型Biomarker(铁死亡正调控因子);
- 筛选/验证逻辑:通过siRNA沉默SLC39A14,发现细胞内铁水平下降(降低30%,n=4,P<0.05),脂质过氧化减少(降低40%,n=4,P<0.05),细胞存活率升高(升高50%,n=4,P<0.05);
- 核心成果:SLC39A14通过调控铁摄取影响铁死亡,其表达水平与铁过载相关疾病(如肝损伤)的铁死亡程度正相关。
结论
本文系统总结了SLC家族在铁死亡中的作用,揭示了SLC作为“营养代谢-铁死亡”轴的关键调控者,通过转运葡萄糖、氨基酸、脂质、金属离子等物质,直接或间接影响铁死亡的核心通路(脂质过氧化、GSH-GPX4轴、线粒体代谢)。文中提出的SLC分类框架为后续研究提供了清晰的方向,而SLC7A11、SLC27A2等Biomarker的发现,为疾病诊断和靶向治疗提供了新靶点。未来需进一步探索SLC家族的协同作用及临床转化,推动铁死亡诱导剂在肿瘤、神经退行性疾病等领域的应用。