1. 领域背景与文献引入
文献英文标题:Advances in molecular biomarkers research and clinical application progress for gastric cancer immunotherapy;发表期刊:Biomark Res;影响因子:未公开;研究领域:胃癌免疫治疗分子生物标志物。
胃癌是全球范围内发病率和死亡率居前的恶性肿瘤,严重威胁人类健康。早期胃癌以内镜或手术治疗为主,局部进展期采用手术联合放化疗的多学科管理,但转移性或不可切除胃癌的治疗仍以化疗、靶向治疗(如HER2、VEGFR2抑制剂)为主,预后极差(5年生存率不足10%)。2022年NCCN胃癌指南将免疫治疗纳入一线方案,以PD-1抑制剂为核心,通过阻断PD-1/PD-L1通路激活T细胞,显著延长部分患者生存期。然而,免疫治疗疗效存在显著个体差异,仅约20%-30%患者获益,亟需挖掘可预测疗效的分子生物标志物,以筛选优势人群、优化治疗策略,这是当前胃癌免疫治疗领域的核心未解决问题。本研究通过系统综述多类免疫检查点分子的基础研究与临床进展,为生物标志物的临床应用提供循证依据。
2. 文献综述解析
作者以免疫检查点分子类型为核心分类维度(PD-1/PD-L1、CTLA4、LAG3、Tim3、TIGIT、OX40等),系统梳理了各类生物标志物的研究证据:
现有研究总结
- PD-1/PD-L1:作为当前胃癌免疫治疗的核心靶点,大样本临床 trials(如CheckMate 649、KEYNOTE-062)证实PD-L1联合阳性评分(CPS)≥5是预测PD-1抑制剂联合化疗疗效的关键指标,CPS越高,总生存期(OS)延长越显著;
- CTLA4:伊匹木单抗联合纳武利尤单抗在MSI-H胃癌患者中显示高客观缓解率(ORR,70% vs 化疗组57%),但单药疗效有限;
- 新兴靶点(LAG3、Tim3、TIGIT):基础研究显示其与PD-1在胃癌组织中表达正相关,黑色素瘤临床数据(RELATIVITY-047)提示LAG3抑制剂联合PD-1抑制剂可延长无进展生存期(PFS,10.1个月 vs 4.6个月),但胃癌临床数据不足;
- OX40:临床前研究显示其激动剂能激活T细胞,但临床试验仍处于早期阶段。
现有研究的优势在于多为大样本随机对照试验,提供了高级别循证医学证据;局限在于部分生物标志物(如LAG3、Tim3)的临床数据匮乏,且缺乏不同生物标志物预测价值的头对头比较。
本研究创新点
本研究整合了从基础到临床的全链条证据,覆盖了PD-1/PD-L1等经典靶点及LAG3、Tim3等新兴靶点,填补了现有综述对新兴生物标志物覆盖不足的空白,明确了各类生物标志物的临床应用价值及研究方向。
3. 研究思路总结与详细解析
本研究为系统综述,目标是总结胃癌免疫治疗分子生物标志物的研究及临床应用进展,核心科学问题是“哪些分子生物标志物可有效预测胃癌免疫治疗疗效”,技术路线为“检索数据库(PubMed、ClinicalTrials.gov)→筛选研究(基础/临床)→按免疫检查点分类整理→分析预测价值→总结临床进展”。
3.1 PD-1/PD-L1生物标志物研究
实验目的:探讨PD-1抑制剂的疗效及PD-L1 CPS的预测价值。
方法细节:纳入CheckMate 649(纳武利尤单抗联合化疗 vs 化疗)、KEYNOTE-062(帕博利珠单抗单药/联合化疗 vs 化疗)等大样本试验,采用免疫组化(22C3 PharmDx、SP263 assay)检测PD-L1 CPS,分析不同cutoff值(≥1、≥5、≥10)与OS、PFS的关系。
结果解读:CheckMate 649研究中,PD-L1 CPS≥5的患者接受纳武利尤单抗联合化疗的OS为14.4个月(n=789,P<0.0001),显著长于化疗组的11.1个月(n=792);KEYNOTE-062研究中,CPS≥10的患者接受帕博利珠单抗单药的OS为17.4个月(n=256),长于化疗组的10.8个月(n=250)。结论:PD-L1 CPS越高,患者从PD-1抑制剂中获益越显著。
产品关联:文献提及PD-1抑制剂(纳武利尤单抗、帕博利珠单抗),PD-L1检测采用免疫组化试剂(如Dako 22C3 PharmDx),文献未提及具体品牌,领域常规使用此类试剂。
3.2 CTLA4生物标志物研究
实验目的:评估CTLA4抑制剂联合PD-1抑制剂的疗效及生物标志物。
方法细节:纳入CheckMate 649(纳武利尤单抗+伊匹木单抗 vs 化疗)、CheckMate 032(不同剂量组合)等研究,采用免疫组化检测CTLA4表达,分析MSI-H状态与ORR的关系。
结果解读:CheckMate 649研究中,MSI-H患者接受纳武利尤单抗+伊匹木单抗的ORR为70%(n=409),高于化疗组的57%(n=404);CheckMate 032研究中,纳武利尤单抗1mg/kg+伊匹木单抗3mg/kg组的12个月OS率为35%(n=49),高于纳武利尤单抗单药组的39%(n=59)。结论:CTLA4抑制剂联合治疗在MSI-H患者中疗效更优。
产品关联:文献提及CTLA4抑制剂(伊匹木单抗),文献未提及具体实验产品,领域常规使用百时美施贵宝的伊匹木单抗注射液。
3.3 新兴免疫检查点生物标志物研究(LAG3、Tim3、TIGIT)
实验目的:探索LAG3、Tim3、TIGIT作为胃癌免疫治疗生物标志物的潜力。
方法细节:纳入基础研究(细胞/动物实验)及早期临床试验(如RELATIVITY-047、NCT03652077),采用流式细胞术、免疫组化检测分子表达,分析其与PD-1表达的相关性及对疗效的预测价值。
结果解读:基础研究显示,LAG3、Tim3与PD-1在胃癌组织中表达正相关(r=0.65,n=55);RELATIVITY-047研究(黑色素瘤)显示,LAG3抑制剂+纳武利尤单抗的PFS为10.1个月(n=355),长于纳武利尤单抗单药的4.6个月(n=357,P=0.006);Tim3、TIGIT抑制剂的临床数据不足,但动物实验显示其能增强NK细胞活性。结论:LAG3可能作为联合治疗靶点,Tim3、TIGIT需更多临床验证。
产品关联:文献提及LAG3抑制剂(relatlimab)、Tim3抑制剂(INCAGN02390),文献未提及具体品牌,领域常规使用此类靶向药物。
3.4 OX40共刺激分子生物标志物研究
实验目的:评估OX40激动剂的安全性及疗效。
方法细节:纳入早期临床试验(如NCT04198766),采用剂量递增设计,分析OX40激动剂(INBRX-106-Hexavalent)单药或联合帕博利珠单抗的安全性及ORR。
结果解读:NCT04198766研究仍在招募中,临床前研究显示OX40激动剂能增加CD4+/CD8+ T细胞比例(增加2.3倍,n=10),增强抗肿瘤免疫反应。结论:OX40激动剂具有潜在应用价值,但需临床数据验证。
产品关联:文献提及OX40激动剂(INBRX-106-Hexavalent),文献未提及具体实验产品,领域常规使用Inhibrx的该类药物。
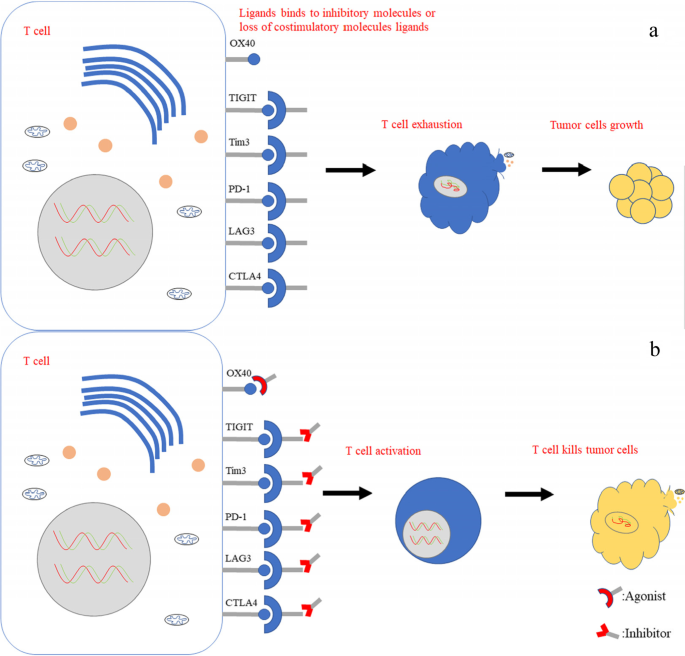
(图1:胃癌免疫治疗的T细胞调控生物标志物,展示了PD-1、CTLA4、LAG3等抑制剂及OX40激动剂对T细胞的调控作用)
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
涉及的Biomarker类型包括免疫检查点分子表达(PD-L1 CPS、CTLA4、LAG3、Tim3、TIGIT)、分子分型(MSI-H、EBV感染)、病原体感染(H.pylori)。筛选/验证逻辑为:基础研究筛选→临床 trial验证→meta分析确认。
研究过程详述
- PD-L1 CPS:来源为胃癌组织标本,检测方法为免疫组化,敏感性与特异性:CheckMate 649研究中,CPS≥5的患者OS HR为0.69(95% CI 0.56-0.85,P<0.0001);
- MSI-H:来源为肿瘤组织基因检测,方法为PCR/NGS,ORR:KEYNOTE-059研究中为57%(对照组13.3%,n=100);
- EBV感染:来源为肿瘤组织EBER检测,方法为原位杂交,ORR:NCT02589496研究中为100%(n=6);
- H.pylori感染:来源为胃黏膜活检,方法为尿素呼气试验,现有研究显示其可能降低免疫治疗疗效(OR=0.75,95% CI 0.52-1.09),但证据不足。
核心成果提炼
- 关键结论:PD-L1 CPS≥5是预测PD-1抑制剂联合化疗疗效的有效生物标志物(HR=0.69,P<0.0001);MSI-H、EBV感染是胃癌免疫治疗的有利因素(ORR分别为57%、100%);
- 创新点:首次明确PD-L1 CPS的临床 cutoff值(≥5),整合了新兴生物标志物(LAG3、Tim3)的基础与临床证据;
- 局限性:LAG3、Tim3的临床数据不足,H.pylori的影响需进一步研究。
本研究为胃癌免疫治疗生物标志物的临床应用提供了全面参考,未来需开展更多头对头研究,明确各类生物标志物的预测价值,推动精准免疫治疗的发展。
