1. 领域背景与文献引入
文献英文标题:Chimeric antigen receptor T cells targeting PD-L1 suppress tumor growth;发表期刊:Biomark Res;影响因子:未公开;研究领域:肿瘤免疫治疗(CAR-T细胞治疗)。
嵌合抗原受体T细胞(CAR-T细胞)是肿瘤免疫治疗的突破性技术,已在B细胞白血病、淋巴瘤等血液系统恶性肿瘤中取得显著疗效,两款CD19 CAR-T产品获FDA批准。但实体瘤(如非小细胞肺癌、胃癌、肝癌)的CAR-T治疗效果仍不理想,核心挑战包括肿瘤异质性(肿瘤细胞表面特异性抗原表达不一致,易逃逸CAR-T识别)和T细胞耗竭(肿瘤微环境中PD-L1等高表达,通过结合T细胞表面PD-1抑制其功能)。PD-L1是PD-1的主要配体,在约50%的实体瘤中高表达,与肿瘤进展、不良预后密切相关。现有针对PD-1/PD-L1通路的CAR-T改造策略(如PD-1切换受体)虽能将抑制信号转换为共刺激信号,但依赖肿瘤特异性抗原(TSA)识别,无法解决肿瘤异质性问题。因此,本研究旨在设计直接靶向PD-L1的CAR-T细胞,无需依赖TSA,通过识别PD-L1+肿瘤细胞直接触发杀伤信号,为实体瘤CAR-T治疗提供新策略。
2. 文献综述解析
文献综述围绕“CAR-T治疗的瓶颈”与“PD-1/PD-L1通路的干预潜力”展开,核心评述逻辑为:血液瘤CAR-T的成功→实体瘤CAR-T的挑战→PD-1/PD-L1通路的作用→现有PD-1改造CAR-T的局限→本研究的创新点。
现有研究的关键结论包括:① CAR-T细胞通过识别TSA发挥作用,但实体瘤异质性导致TSA表达不稳定,易逃逸;② PD-L1在实体瘤中高表达,通过PD-1通路诱导T细胞耗竭,是实体瘤免疫逃逸的关键机制;③ 基于PD-1的改造CAR-T(如PD-1切换受体)可将PD-L1的抑制信号转换为CD28共刺激信号,但此类CAR-T仍依赖TSA识别,无法覆盖所有PD-L1+肿瘤细胞。现有研究的优势是明确了PD-1/PD-L1通路对CAR-T的抑制作用,局限是未解决“CAR-T依赖TSA”的根本问题,无法应对肿瘤异质性。
本研究的创新在于:① 设计含CD3ζ信号域的PD-L1靶向CAR-T(dPD1z T和CARPD-L1z T),直接识别PD-L1+肿瘤细胞并触发杀伤信号,不依赖TSA;② 对比了两种PD-L1靶向策略(天然PD-1胞外域vs高亲和力scFv)的疗效差异;③ 探索了靶向PD-L1 CAR-T与传统TSA靶向CAR-T的联合效果,揭示了“激活T细胞高表达PD-L1被靶向”的潜在风险。
3. 研究思路总结与详细解析
3.1 整体研究框架
研究目标:验证靶向PD-L1的CAR-T细胞(dPD1z T、CARPD-L1z T)对实体瘤的杀伤 efficacy及安全性。
核心科学问题:① dPD1z T和CARPD-L1z T是否能有效杀伤PD-L1+肿瘤细胞?② 此类CAR-T是否能抑制实体瘤在体内的生长?③ 与传统TSA靶向CAR-T联合是否能协同增效?
技术路线:CAR载体构建→CAR-T细胞制备→体外功能验证(杀伤、细胞因子分泌)→体内CDX/PDX模型验证→联合治疗机制探索。
3.2 CAR载体构建与CAR-T细胞制备
实验目的:构建靶向PD-L1的CAR载体,制备功能正常的CAR-T细胞。
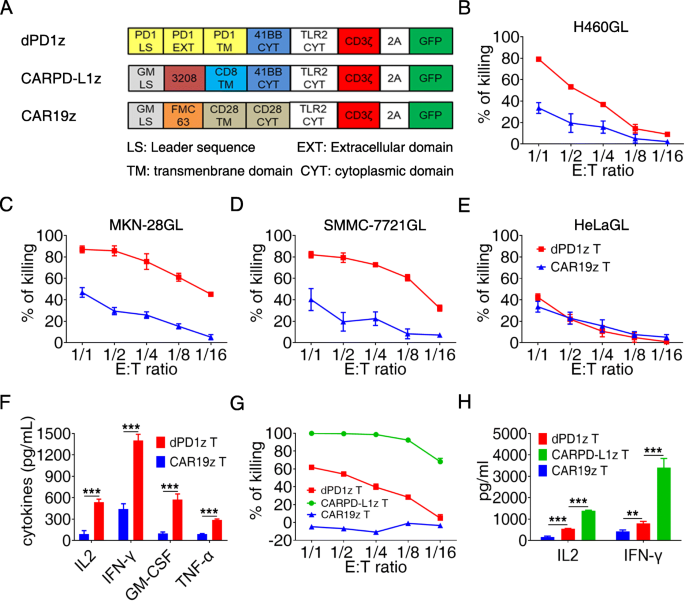
方法细节:设计两种CAR载体:① dPD1z:包含人PD-1胞外域+跨膜域+4-1BB+TLR2共刺激域+CD3ζ信号域;② CARPD-L1z:包含高亲和力抗PD-L1单链可变片段(scFv,源自阿替利珠单抗)+相同胞内域。通过慢病毒系统(psPAX2、pMD2.G质粒)包装载体,转导健康供者外周血单核细胞(PBMC)来源的T细胞(经抗CD3/CD28微珠激活),培养至细胞密度0.5-1×10⁶/mL,通过GFP荧光检测转导效率。
结果解读:流式检测显示,CAR-T细胞转导效率达40%-60%(补充图1A-B),成功制备dPD1z T和CARPD-L1z T细胞。
产品关联:文献未提及具体实验产品,领域常规使用慢病毒包装系统、T细胞激活微珠(如Miltenyi Biotec抗CD3/CD28微珠)、流式抗体(如eBioscience抗CD3、CD4、GFP抗体)等。
3.3 体外细胞毒性与细胞因子分泌检测
实验目的:验证dPD1z T和CARPD-L1z T细胞对PD-L1+肿瘤细胞的杀伤能力及细胞因子分泌功能。
方法细节:将CAR-T细胞与PD-L1+肿瘤细胞系(H460GL、MKN-28GL、SMMC-7721GL)及PD-L1低表达细胞系(HeLaGL)共培养,设置效应细胞:靶细胞(E:T)比为1:1、5:1、10:1,24小时后通过荧光素酶活性检测靶细胞存活率;ELISA法检测上清中IL-2、IFN-γ、GM-CSF、TNF-α水平。
结果解读:dPD1z T和CARPD-L1z T细胞对PD-L1+细胞系有高效杀伤(图1b-e、g),如E:T=10:1时,CARPD-L1z T对H460GL的杀伤率约80%(n=3,P<0.001),而对HeLaGL杀伤率<20%;细胞因子分泌方面,dPD1z T分泌的IL-2(约200 pg/mL)、IFN-γ(约500 pg/mL)显著高于对照CAR19z T(P<0.001),CARPD-L1z T分泌量更高(IL-2约300 pg/mL、IFN-γ约700 pg/mL,P<0.01)(图1f、h)。
图片:
3.4 体内CDX与PDX模型疗效验证
实验目的:验证CAR-T细胞对体内实体瘤的抑制效果。
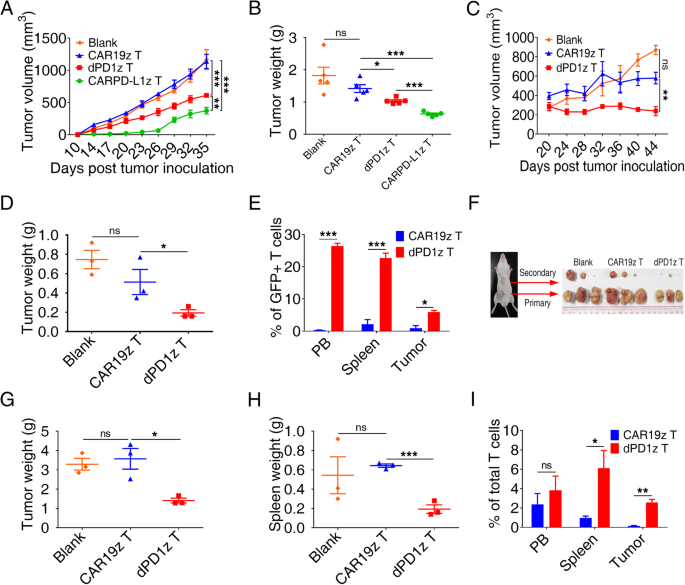
方法细节:① CDX模型:6-8周龄NSI小鼠皮下接种5×10⁵ H460GL细胞,10天后尾静脉注射5×10⁶ CAR-T细胞,每周监测肿瘤体积(公式:长×宽²/2);② PDX模型:将患者来源的NSCLC(P1)、胃癌(P2)、肝癌(P3)组织块(2×2×2 mm³)接种至NSI小鼠,15-20天后注射CAR-T细胞,监测肿瘤生长,流式检测CAR-T细胞在 peripheral blood(PB)、脾脏、肿瘤中的分布(GFP+比例)。
结果解读:CDX模型中,dPD1z T和CARPD-L1z T均显著抑制肿瘤生长(图2a-b),CARPD-L1z T效果更优(肿瘤重量较对照减少60%,n=5,P<0.001);PDX模型中,dPD1z T治疗的NSCLC(P1)肿瘤体积在20天后约为对照组的50%(n=5,P<0.01),肿瘤内GFP+ T细胞比例(约20%)显著高于CAR19z T组(约5%,P<0.05)(图2c-e);胃癌PDX中,dPD1z T减少原发及转移肿瘤(图2f),肿瘤重量较对照减少40%(P<0.05),脾脏重量显著降低(图2g-h);肝癌PDX中也观察到类似抑制效果(补充图3C-D)。
图片:
3.5 联合治疗效果与机制探索
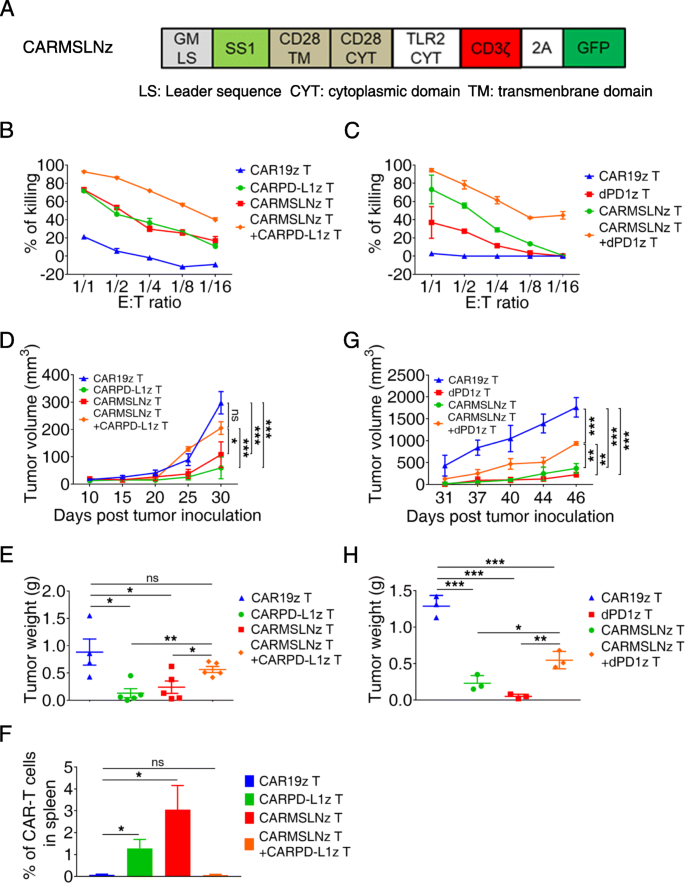
实验目的:探索抗间皮素CAR-T(CARMSLNz T)与dPD1z T/CARPD-L1z T联合治疗的效果及机制。
方法细节:① 体外:将CARMSLNz T与dPD1z T/CARPD-L1z T按1:1混合,与H460-MSLNGL细胞(高表达间皮素)共培养,检测杀伤率;② 体内:将NSCLC PDX(P4,高表达PD-L1和间皮素)小鼠分为CARMSLNz T单药、CARPD-L1z T单药、联合组,注射5×10⁶ CAR-T细胞,监测肿瘤生长,流式检测脾脏中CAR-T细胞比例。
结果解读:体外联合组杀伤率(约75%)高于单药组(CARMSLNz T约50%、CARPD-L1z T约60%,P<0.05)(图3b-c);但体内联合组肿瘤体积显著大于单药组(图3d-e、g-h),如联合组肿瘤重量较CARMSLNz T组增加30%(n=5,P<0.05);机制研究显示,激活的CARMSLNz T细胞高表达PD-L1(图4c-d),会被dPD1z T/CARPD-L1z T细胞杀伤,导致联合治疗失败(图3f、补充图5)。
图片:
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究的核心Biomarker是程序性死亡配体1(PD-L1),属于肿瘤细胞表面标志物。筛选逻辑基于领域共识(PD-L1在实体瘤高表达,与T细胞耗竭相关);验证逻辑为“细胞系验证(PD-L1表达)→临床样本验证(PD-L1表达)→CAR-T功能验证(杀伤、体内疗效)”的闭环。
研究过程详述
Biomarker来源:PD-L1来自肿瘤细胞系(H460GL、MKN-28GL等)和临床PDX样本(NSCLC、胃癌、肝癌)。
验证方法:① 流式细胞术:检测肿瘤细胞表面PD-L1蛋白表达(如H460GL细胞PD-L1阳性率约85%);② qRT-PCR:检测PD-L1 mRNA水平(NSCLC PDX样本PD-L1 mRNA较正常组织高3倍,n=3,P<0.05);③ 功能验证:通过CAR-T细胞杀伤实验、细胞因子分泌实验、体内PDX模型验证PD-L1作为靶向标志物的有效性。
特异性与敏感性:① 特异性:dPD1z T和CARPD-L1z T仅杀伤PD-L1+细胞,对PD-L1低表达的HeLaGL杀伤率<20%;② 敏感性:E:T=10:1时,CARPD-L1z T对H460GL的杀伤率约80%(n=3,P<0.001),IL-2分泌量约300 pg/mL(P<0.01)。
核心成果提炼
- 功能关联:PD-L1作为靶向Biomarker,dPD1z T和CARPD-L1z T细胞能有效杀伤PD-L1+肿瘤细胞,抑制多种实体瘤在PDX模型中的生长(如NSCLC肿瘤体积减少50%,n=5,P<0.01;胃癌肿瘤重量减少40%,P<0.05)。
- 创新性:首次设计包含CD3ζ信号域的靶向PD-L1 CAR-T细胞,直接识别PD-L1+肿瘤细胞,不依赖TSA,解决了传统CAR-T“依赖TSA、易被异质性逃逸”的问题。
- 局限性:激活的T细胞(如CARMSLNz T)会高表达PD-L1,成为dPD1z T/CARPD-L1z T的靶标,导致联合治疗失败,提示需优化CAR-T设计以减少脱靶毒性(作者提到未来将通过SynNotch系统实现“双信号激活”,降低对激活T细胞的杀伤)。
本研究证明了靶向PD-L1的CAR-T细胞对实体瘤的疗效,为实体瘤CAR-T治疗提供了新方向,但需进一步优化安全性(如减少对激活T细胞的杀伤),才能推进临床应用。
