1. 领域背景与文献引入
文献英文标题:HER2-targeted advanced metastatic gastric/gastroesophageal junction adenocarcinoma: treatment landscape and future perspectives;发表期刊:Biomarker Research;影响因子:未公开;研究领域:胃/胃食管结合部腺癌的HER2靶向治疗。
胃/胃食管结合部(G/GEJ)癌是全球第五大常见癌症(2020年约100万新发病例),也是第四大癌症死亡原因(约76万死亡病例)。中国是胃癌高发国,病例数占全球40%,且超过90%的GEJ癌为腺癌类型。早期患者术后5年生存率可达60%以上,但晚期转移性G/GEJ腺癌患者以系统药物治疗(氟尿嘧啶+铂类±紫杉醇)为主,中位总生存(mOS)仅约11个月,长期生存仍不乐观。生物标志物的发现推动了靶向治疗的突破:人表皮生长因子受体2(HER2)作为关键靶点,其过表达/扩增见于7.3-20.2%的G/GEJ腺癌患者(中国人群约12-13%)。2010年ToGA试验首次将曲妥珠单抗(抗HER2单克隆抗体)加入标准化疗,结果显示HER2阳性患者的mOS从11.1个月延长至13.8个月(P=0.046),开启了G/GEJ腺癌的HER2靶向治疗时代。然而,多数患者在治疗后会出现耐药或疾病进展,且HER2检测的异质性、低表达患者的治疗空白等问题尚未解决。因此,系统总结现有HER2靶向药物的临床疗效、探索耐药机制及未来优化策略,成为领域内的关键需求——本综述正是基于这一背景,通过分类梳理各类HER2靶向药物的临床数据,整合耐药机制研究,为HER2阳性晚期G/GEJ腺癌的治疗提供全面参考。
2. 文献综述解析
作者以“HER2靶向药物的类型”为核心分类维度(单克隆抗体、双特异性抗体、抗体药物偶联物(ADC)、酪氨酸激酶抑制剂(TKI)、免疫联合治疗),系统总结了现有研究的关键结论、优势及局限性。
现有研究的关键结论包括:(1)单克隆抗体中,曲妥珠单抗联合化疗是HER2阳性晚期G/GEJ腺癌的一线标准治疗,但帕妥珠单抗的联合治疗(JACOB试验)未显著改善生存(mOS 17.5 vs 14.2个月,P=0.056);(2)ADC类药物(如DS-8201、维迪西妥单抗)在经治患者中显示出优效性:DESTINY-Gastric01试验中,DS-8201三线及后线治疗的ORR达51.3%(vs 标准治疗14.3%),mOS延长至12.5个月(vs 8.4个月,P=0.0097);(3)TKI类药物(如拉帕替尼)仅在HER2 IHC3+亚组显示疗效(TyTAN试验中PFS 5.6 vs 4.2个月,P=0.0101),但总人群OS未改善;(4)免疫联合HER2靶向治疗(如帕博利珠单抗联合曲妥珠单抗)显示协同效应:KEYNOTE-811试验中,联合治疗的ORR从51.9%提升至74.4%(P<0.001)。
现有研究的优势在于多线治疗策略的探索(覆盖一线至后线),但局限性仍显著:部分药物临床试验未达主要终点(如帕妥珠单抗的JACOB试验)、耐药机制未完全阐明、HER2检测的异质性(45-79%的HER2阳性患者存在表达异质性)影响疗效评估。
本综述的创新价值在于:通过系统分类整合各类药物的临床数据,明确了不同药物的适用场景(如ADC针对经治及HER2低表达患者);并结合耐药机制的最新研究(如HER2异质性、信号通路激活),为未来治疗优化(如ADC联合免疫治疗、HER2低表达患者的精准治疗)提供了依据。
3. 研究思路总结与详细解析
本综述的研究目标是“系统总结HER2阳性晚期G/GEJ腺癌的HER2靶向治疗现状、耐药机制及未来方向”;核心科学问题包括“各类HER2靶向药物的临床疗效如何?”“HER2靶向治疗的耐药机制是什么?”“如何优化未来治疗策略?”;技术路线为“回顾临床研究(按药物类型分类)→ 分析耐药机制→ 探讨未来策略”。
3.1 单克隆抗体类HER2靶向药物研究
实验目的:总结曲妥珠单抗、帕妥珠单抗等单克隆抗体在HER2阳性晚期G/GEJ腺癌中的疗效。
方法细节:回顾ToGA试验(曲妥珠单抗+化疗 vs 化疗,一线治疗)、JACOB试验(帕妥珠单抗+曲妥珠单抗+化疗 vs 曲妥珠单抗+化疗,一线治疗)、CPMGAH22-05试验(玛格妥昔单抗+帕博利珠单抗,二线及后线治疗)。
结果解读:ToGA试验显示曲妥珠单抗联合化疗显著延长mOS(13.8 vs 11.1个月,P=0.046),成为一线标准;JACOB试验未显示帕妥珠单抗的生存优势(P=0.056),但病理完全缓解率(pCR)更高;玛格妥昔单抗联合帕博利珠单抗的二线治疗显示出“meaningful outcomes”(文献未明确具体数据)。
产品关联:实验所用关键产品包括曲妥珠单抗(Herceptin)、帕妥珠单抗(Perjeta);文献未提及具体货号,领域常规使用此类HER2单克隆抗体。
3.2 双特异性抗体类HER2靶向药物研究
实验目的:评估ZW25、KN026等双特异性抗体的疗效。
方法细节:回顾ZW25的I期试验(单药治疗经治患者)、II期试验(联合化疗一线治疗),以及KN026的II期试验(单药治疗)。
结果解读:ZW25单药治疗经治患者显示出抗肿瘤活性;II期试验中,ZW25联合化疗的疾病控制率(DCR)达100%(部分患者仍在治疗);KN026的II期试验显示客观缓解率(ORR)为55.6%,常见不良反应为肝功能异常和皮疹。
产品关联:文献未提及具体实验产品,领域常规使用双特异性抗体如ZW25、KN026。
3.3 抗体药物偶联物(ADC)类HER2靶向药物研究
实验目的:探索ADC对经治及HER2低表达患者的疗效。
方法细节:回顾GATSBY试验(T-DM1 vs 紫杉醇,二线治疗)、DESTINY-Gastric01试验(DS-8201 vs 标准治疗,三线及后线)、RC48-C008试验(维迪西妥单抗,三线及后线)。
结果解读:GATSBY试验未显示T-DM1的优势(mOS 7.9 vs 8.6个月,P=0.86),可能因未重新评估HER2状态;DESTINY-Gastric01试验中,DS-8201的ORR达51.3%(vs 14.3%),mOS延长至12.5个月(P=0.0097);维迪西妥单抗的ORR为24.8%,mPFS为4.1个月。
产品关联:实验所用关键产品包括DS-8201(Enhertu)、维迪西妥单抗(爱地希);文献未提及具体货号,领域常规使用此类ADC药物。
3.4 酪氨酸激酶抑制剂(TKI)类HER2靶向药物研究
实验目的:评估拉帕替尼、图卡替尼等TKI的疗效。
方法细节:回顾TyTAN试验(拉帕替尼+紫杉醇 vs 紫杉醇,二线治疗)、TRIO-013/LOGiC试验(拉帕替尼+卡培他滨+奥沙利铂 vs 卡培他滨+奥沙利铂,一线治疗)。
结果解读:TyTAN试验中,拉帕替尼在HER2 IHC3+亚组的PFS更长(5.6 vs 4.2个月,P=0.0101),但总人群OS未改善(11.0 vs 8.9个月,P=0.104);TRIO-013/LOGiC试验未显示拉帕替尼的OS优势(P=0.349)。
产品关联:文献未提及具体实验产品,领域常规使用TKI类药物如拉帕替尼。
3.5 免疫联合HER2靶向治疗研究
实验目的:探索免疫检查点抑制剂(ICIs)与HER2靶向药物的协同效应。
方法细节:回顾KEYNOTE-811试验(帕博利珠单抗+曲妥珠单抗+化疗 vs 曲妥珠单抗+化疗,一线治疗)、CPMGAH22-05试验(玛格妥昔单抗+帕博利珠单抗,二线治疗)。
结果解读:KEYNOTE-811试验中,联合治疗的ORR从51.9%提升至74.4%(P<0.001),DCR达96.2%(vs 89.3%);玛格妥昔单抗联合帕博利珠单抗显示出协同效应。
产品关联:实验所用关键产品包括帕博利珠单抗(Keytruda)、曲妥珠单抗(Herceptin);文献未提及具体货号,领域常规使用此类联合方案。
3.6 HER2靶向治疗的耐药机制研究
实验目的:分析HER2靶向治疗的耐药机制。
方法细节:整合临床研究(如GATHER3试验中HER2阳性状态丢失)、基础研究(如基因测序、免疫组化)的结果。
结果解读:耐药机制包括:(1)HER2异质性(45-79%的患者存在表达异质性);(2)HER2阳性状态丢失(29-69%的患者治疗后丢失);(3)信号通路激活(如SRC介导的MAPK-ERK通路激活);(4)ADC-specific机制(如内吞异常)。
产品关联:文献未提及具体实验产品,领域常规通过基因测序研究耐药机制。
4. Biomarker研究及发现成果解析
本综述的核心Biomarker是HER2(人表皮生长因子受体2),类型为“HER2过表达/扩增”,筛选/验证逻辑为“免疫组化(IHC)检测蛋白表达,联合荧光原位杂交(FISH)检测基因扩增;IHC 3+或IHC 2+/FISH+定义为HER2阳性”。
Biomarker定位
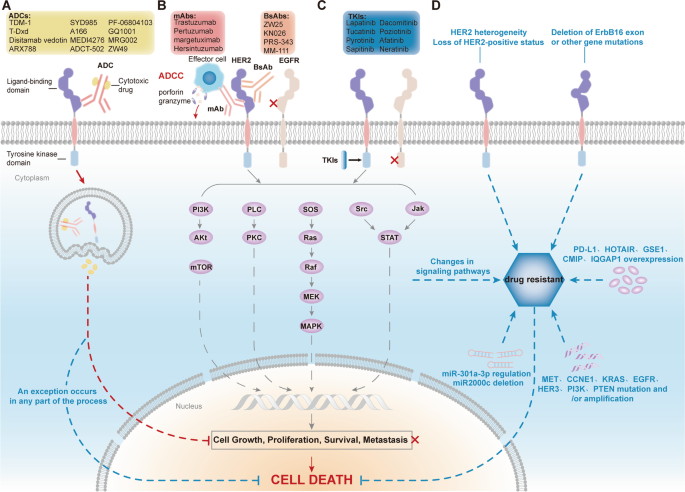
HER2是G/GEJ腺癌的关键靶向治疗Biomarker:其基因扩增导致蛋白过表达,进而激活下游Ras-Raf-Mek-MAPK、PI3K-Akt-mTOR通路,促进细胞增殖并抑制凋亡。HER2阳性患者约占G/GEJ腺癌的7.3-20.2%(中国人群12-13%),且更常见于胃食管结合部癌(32.2%)及肠型腺癌(31.8%)。
研究过程详述
HER2的来源为肿瘤组织样本(手术或活检标本),验证方法为IHC联合FISH:
- IHC检测蛋白表达:0/1+为阴性,2+需FISH确认,3+为阳性;
- FISH检测基因扩增:HER2/CEP17比值≥2.0定义为扩增。
临床验证包括ToGA试验(纳入594例HER2阳性患者,曲妥珠单抗联合化疗的mOS为13.8个月,vs 化疗组11.1个月,P=0.046)、DESTINY-Gastric01试验(纳入187例经治HER2阳性患者,DS-8201的ORR为51.3%,vs 标准治疗14.3%,P<0.001)。
核心成果提炼
- 疗效关联:HER2阳性是曲妥珠单抗联合化疗的一线治疗指征,显著改善生存(ToGA试验HR=0.74,95%CI 0.59-0.92);
- 耐药机制:HER2异质性(45-79%的患者存在表达异质性)、阳性状态丢失(29-69%的患者治疗后丢失)、信号通路激活(如SRC介导的通路激活)是主要耐药原因;
- 创新价值:明确了HER2低表达患者(IHC 1+或IHC 2+/FISH-)的治疗潜力——ADC类药物(如DS-8201、维迪西妥单抗)通过“旁观者效应”(payload释放后杀伤邻近HER2阴性细胞),可改善此类患者的生存;
- 统计学结果:ToGA试验的mOS差异有统计学意义(P=0.046);DESTINY-Gastric01试验的ORR差异显著(P<0.001)。
综上,本综述通过系统梳理HER2靶向药物的临床数据及耐药机制,明确了HER2作为G/GEJ腺癌关键Biomarker的价值,并为未来治疗优化(如ADC联合免疫治疗、HER2低表达患者的精准治疗)提供了重要参考。
