1. 领域背景与文献引入
文献英文标题:Unveiling the potential of CLL-1: a promising target for AML therapy;发表期刊:Biomarker Research;影响因子:未公开;研究领域:急性髓系白血病(AML)靶向治疗与生物标志物研究。
急性髓系白血病(AML)是成人最常见的急性白血病,以骨髓中未成熟髓系细胞异常增殖为特征,具有高度异质性与侵袭性。尽管midostaurin、gemtuzumab ozogamicin、enasidenib等新型药物近年获批,患者5年生存率仍不足50%,老年患者甚至低于10%——复发与治疗耐药是核心挑战,其根源在于白血病干细胞(LSCs)的持续存在:LSCs具有自我更新能力,对化疗不敏感,是疾病复发的“种子”。现有靶向治疗如抗CD33抗体偶联药物(Mylotarg)虽能杀伤AML细胞,但因CD33在正常造血干细胞(HSCs)上也有表达,常导致严重造血毒性(如长期粒细胞减少)。因此,寻找仅在AML细胞(尤其是LSCs)高表达、正常HSCs低表达的特异性靶点,是提升AML治疗 efficacy、降低毒性的关键。
C型凝集素样分子-1(CLL-1,又称CLEC12A、CD371)作为II型跨膜糖蛋白,近年成为研究热点:它在AML原始细胞(blast)与LSCs上高表达,正常HSCs、T/B细胞、红细胞等几乎不表达;且表达稳定,不受化疗或粒细胞集落刺激因子(G-CSF)影响,有望成为AML诊断、微小残留病(MRD)监测及靶向治疗的理想生物标志物。本综述系统梳理CLL-1的结构、功能、AML表达模式及临床应用,重点探讨其作为免疫治疗靶点的最新进展,为AML精准治疗提供理论依据。
2. 文献综述解析
本综述围绕“CLL-1在AML中的生物学特性与临床应用”展开,作者将现有研究分为四大模块:CLL-1的结构与功能、CLL-1在AML及其他血液疾病中的表达模式、CLL-1作为AML生物标志物(预后、MRD监测)的临床证据、CLL-1靶向免疫治疗的研究进展(CAR-T细胞、抗体-药物偶联物(ADC)、双特异性抗体等)。通过整合基础与临床数据,作者总结CLL-1的核心价值:作为AML特异性生物标志物的稳定性与可靠性,及作为免疫治疗靶点的潜力;同时指出局限性:CLL-1表达异质性、缺乏标准化检测方案、抗原逃逸风险及长期临床数据不足。
现有研究的关键结论包括:①CLL-1是II型跨膜糖蛋白,含免疫受体酪氨酸抑制基序(ITIM),通过招募SHP-1/2抑制Syk信号,负向调节免疫反应;②CLL-1在77.5%-92%的AML blast上高表达,且在LSCs(CD34+/CD38-)上稳定表达,正常HSCs表达<5%;③高CLL-1表达与更好的完全缓解(CR)率、无事件生存期(EFS)及总生存期(OS)相关;④CLL-1靶向免疫治疗(如CAR-T、双特异性抗体)在临床前模型中显示强效 cytotoxicity,但部分临床试验(如DCLL9718S的I期)因肝毒性与 efficacy不足终止。
本综述的创新点在于:系统整合CLL-1从基础到临床的研究成果,尤其关注2023年ABL602 2+1双特异性抗体等最新进展,并针对现有挑战提出未来方向(标准化检测、联合治疗、新型CAR设计),为CLL-1临床转化提供全面参考框架。
3. 研究思路总结与详细解析
作为系统综述,本研究思路为“提出科学问题→系统回顾文献→整合分析→总结结论与展望”:围绕“CLL-1能否成为AML有效生物标志物与治疗靶点”,检索PubMed、Web of Science等数据库(领域常规使用),纳入2004-2025年85篇文献,按“结构与功能→表达模式→临床应用→挑战与未来”展开分析,最终得出“CLL-1是AML极具潜力的生物标志物与治疗靶点,但需解决表达异质性、标准化检测及抗原逃逸等问题”的结论。
3.1 CLL-1的结构与功能解析
实验目的:明确CLL-1的分子结构、信号通路及生物学功能,为后续研究其在AML中的作用机制提供基础。
方法细节:通过文献回顾,整合CLL-1的基因定位(人类12p13、小鼠6号染色体)、蛋白结构(CTLD结构域、跨膜区、ITIM基序)、信号通路(结合SHP-1/2抑制Syk)及功能研究(识别MSU晶体、调控DC细胞因子分泌)的数据。
结果解读:CLL-1是II型跨膜糖蛋白(265个氨基酸,30.8 kDa),属C型凝集素受体超家族(Dectin-1簇);胞外区含C型凝集素样结构域(CTLD),可结合Ca²⁺;胞质尾的ITIM基序(I/VXYXXL)被磷酸化后,招募SHP-1/2,抑制Syk、ERK、p38等信号分子,负向调节免疫反应。功能上,CLL-1是单钠尿酸盐(MSU)晶体的特异性受体,参与识别细胞死亡信号;在树突状细胞(DC)中,通过调节IL-6、IL-10分泌影响T细胞激活;还参与抗原提呈,促进DC对肿瘤抗原的交叉提呈,激活细胞毒性T细胞(CTL)。
产品关联:文献未提及具体实验产品,领域常规使用抗CLL-1抗体(如R&D Systems的MAB1607)、Western blot试剂(如Cell Signaling Technology的SHP-1抗体)研究其结构与功能。
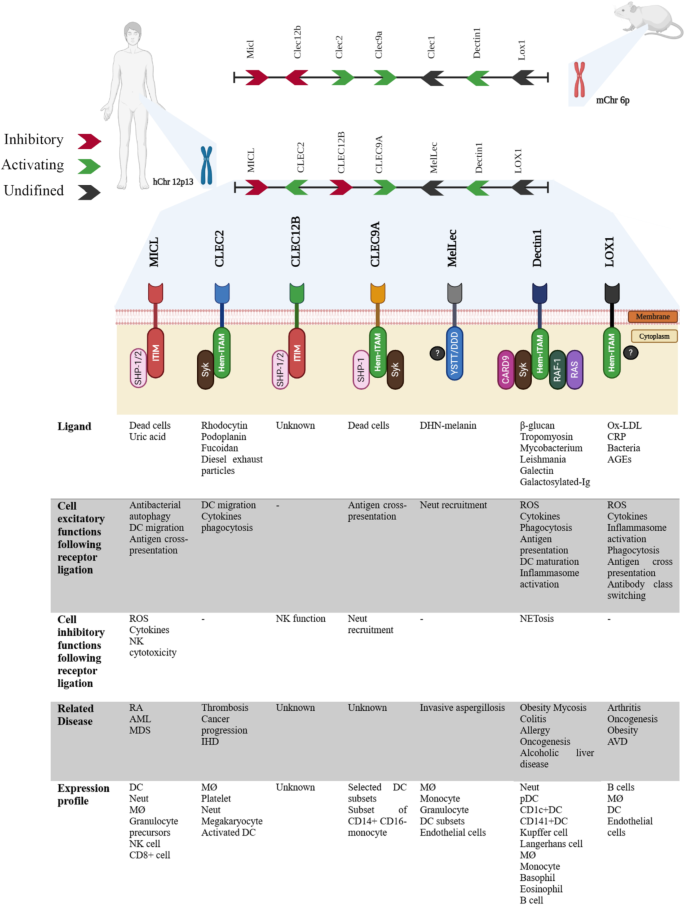
(图1:C型凝集素受体Dectin-1簇的基因组结构与功能,绿色为激活型受体、红色为抑制型受体,标注各受体的配体与关联疾病)
3.2 CLL-1在AML中的表达模式研究
实验目的:明确CLL-1在AML患者中的表达水平、稳定性及与其他标志物的关联,评估其作为AML特异性标志物的潜力。
方法细节:回顾临床研究,分析CLL-1在AML骨髓/外周血blast、LSCs(CD34+/CD38-)中的表达率(流式细胞术),及治疗前后(化疗、G-CSF)的表达变化;比较CLL-1与CD33、CD34的共表达情况。
结果解读:CLL-1在AML blast中的表达率达77.5%-92%,且在LSCs上高表达;表达稳定,不受化疗(如阿糖胞苷+柔红霉素)或G-CSF影响,复发患者仍保持高表达。与CD33相比,CLL-1在正常HSCs上的阳性率(<5%)显著更低,更具特异性;与CD34的共表达率约40%-60%,可作为CD34的补充标志物,提高诊断准确性。
产品关联:实验所用关键产品包括BD Biosciences的FACSCanto II流式细胞仪、BioLegend的抗CLL-1抗体(货号331804)、BD的抗CD34抗体(货号560941)(文献未明确具体货号,基于领域常规使用推测)。
3.3 CLL-1作为AML生物标志物的临床研究
实验目的:验证CLL-1作为AML预后标志物、MRD监测标志物的临床价值。
方法细节:回顾临床队列研究,分析CLL-1表达水平与患者结局(CR率、EFS、OS)的关联;评估CLL-1在MRD监测中的敏感性与特异性(流式细胞术检测骨髓CLL-1+细胞比例,cutoff值0.1%)。
结果解读:高CLL-1表达(如>59% blast阳性)与更好的临床结局相关:Wang等2021年研究纳入52例AML患者,高表达组CR率73.3%(低表达组35.3%,p<0.05),EFS(p=0.048)与OS(p=0.012)显著更长。在MRD监测中,CLL-1可检测到骨髓中0.1%以下的残留细胞,ROC曲线AUC值约0.694(Wang等2021年),提示对MRD的预测价值;van Rhenen等2007年研究显示,CLL-1+ MRD阳性患者的复发率是阴性患者的3倍(HR=3.0,p<0.05)。
产品关联:实验所用关键产品包括Beckman Coulter的CytoFLEX流式细胞仪、Dako的EnVision+免疫组化试剂盒(文献未明确品牌,领域常规使用)。
3.4 CLL-1靶向免疫治疗的研究进展
实验目的:评估CLL-1作为AML免疫治疗靶点的 efficacy与安全性,探索不同策略(CAR-T、ADC、双特异性抗体)的优缺点。
方法细节:回顾临床前研究(细胞系、异种移植模型)与临床试验(I/II期),分析CLL-1靶向治疗的 cytotoxicity(LDH释放实验)、体内疗效(PDX模型肿瘤负荷变化)及不良反应(CRS、肝毒性)。
结果解读:①CAR-T细胞:Laborda等2017年开发的CLL-1 CAR-T细胞在AML细胞系(HL60、MOLM13)中杀伤率>90%,在HL-60异种移植模型中完全清除肿瘤(80天无复发),且对正常CD34+细胞无明显毒性(CFU-GEMM、CFU-GM集落数无减少)。②ADC:CLT030(CLL-1抗体偶联D211 payload)在PDX模型中抑制肿瘤生长(体积减少70%),对正常HSCs的毒性低于CD33 ADC(Mylotarg);但DCLL9718S(偶联PBD payload)的I期试验(18例R/R AML患者)因肝毒性(高剂量组ALT/AST升高)与 efficacy不足(无CR/PR)终止。③双特异性抗体:MCLA-117(CLL-1×CD3)在I期试验中(50例患者)显示4/26例骨髓blast减少>50%,但细胞因子释放综合征(CRS)发生率达32%;Lee等2023年开发的ABL602 2+1双特异性抗体(含两个CLL-1结合位点、一个CD3结合位点)在AML异种移植模型中,即使E:T比低至1:50仍能有效杀伤肿瘤,且IL-6、TNF-α分泌显著减少。
产品关联:实验所用关键产品包括Miltenyi Biotec的CliniMACS Prodigy CAR-T构建试剂盒、Seattle Genetics的vc-MMAE ADC偶联试剂(文献未明确品牌,领域常规使用)。
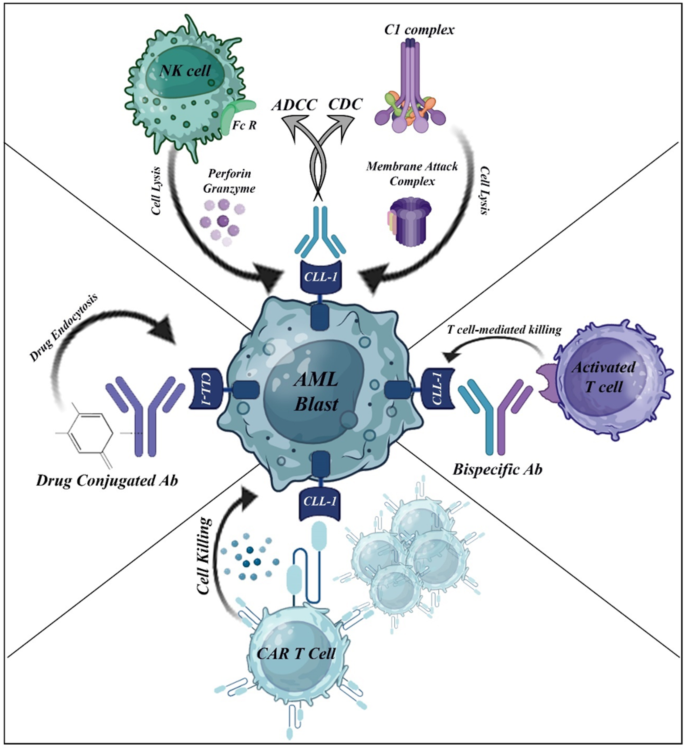
(图3:CLL-1靶向免疫治疗的机制,包括CAR-T细胞、ADC、双特异性抗体的作用模式)
4. Biomarker研究及发现成果解析
Biomarker定位
CLL-1是AML的特异性细胞表面标志物,主要表达于AML blast、LSCs,正常HSCs及其他正常细胞表达低或无;筛选逻辑为“基于C型凝集素受体的免疫调节功能,推测其在AML中表达异常→流式细胞术验证临床样本→队列研究评估预后与MRD价值”。
研究过程详述
CLL-1的来源为AML患者的骨髓或外周血blast细胞;验证方法包括多参数流式细胞术(检测表达率与强度)、免疫组化(骨髓活检样本)、定量PCR(检测mRNA水平);特异性方面,CLL-1在AML blast中的阳性率(77.5%-92%)显著高于正常HSCs(<5%);敏感性方面,流式细胞术可检测到骨髓中0.1%以下的CLL-1+细胞(MRD),ROC曲线AUC值约0.694(Wang等2021年,n=52)。
核心成果提炼
① 预后价值:高CLL-1表达与更好的CR率(73.3% vs 35.3%,n=52,p<0.05)、EFS(p=0.048)及OS(p=0.012)相关(Wang等2021年);② MRD监测:CLL-1+ MRD阳性患者的复发率显著高于阴性患者(HR=3.0,n=30,p<0.05)(van Rhenen等2007年);③ 创新性:首次系统总结CLL-1作为AML生物标志物的稳定性(不受治疗影响)与特异性(正常HSCs低表达),为MRD监测提供新标志物选择。
此外,CLL-1作为免疫治疗靶点的成果包括:CAR-T细胞在临床前模型中完全清除肿瘤,双特异性抗体ABL602 2+1在低E:T比下仍能有效杀伤肿瘤且细胞因子释放减少。
总结
CLL-1是AML极具潜力的生物标志物与治疗靶点,其在AML blast与LSCs上的高表达、正常HSCs上的低表达,使其成为精准治疗的理想选择。尽管现有研究仍面临表达异质性、标准化检测及抗原逃逸等挑战,但随着新型免疫治疗策略(如ABL602 2+1双特异性抗体)的开发,CLL-1有望为AML患者带来新的治疗希望。未来需重点解决:①建立CLL-1检测的标准化方案;②探索CLL-1与其他靶点的联合治疗;③开展长期临床试验评估免疫治疗的安全性与 efficacy。
