1. 领域背景与文献引入
文献英文标题:Organ specific responses to first-line lenvatinib plus anti-PD-1 antibodies in patients with unresectable hepatocellular carcinoma: a retrospective analysis;发表期刊:Biomarker Research;影响因子:3.496(2021年);研究领域:肝细胞癌系统治疗。
肝细胞癌(HCC)是全球第四大癌症相关死亡原因,超过50%的患者确诊时已处于晚期,失去手术或局部治疗机会,预后极差。2008年索拉非尼获批为首个晚期HCC系统治疗药物,但客观缓解率(ORR)仅约20%;2018年仑伐替尼因非劣于索拉非尼的疗效获批,ORR提升至24.1%,但仍未满足临床需求。免疫检查点抑制剂(如抗PD-1抗体)的出现为晚期HCC带来新希望,但单药ORR仅15%-20%,疗效有限。
近年研究发现,抗血管生成药物(如仑伐替尼)与免疫治疗具有协同作用:抗血管生成药物可通过抑制VEGF通路改善肿瘤微环境,增强免疫细胞浸润;免疫治疗则可清除肿瘤细胞,两者联合有望提高疗效。2020年阿替利珠单抗联合贝伐珠单抗获批为晚期HCC一线治疗,ORR达36%,中位总生存期(OS)延长至19.2个月;仑伐替尼联合抗PD-1抗体的Ib期研究也显示ORR达36%,中位OS 22个月,优于单药治疗。
然而,现有研究多关注整体疗效,缺乏对不同器官病变的反应差异分析——HCC常伴随大血管癌栓(MVTT)或肝外转移,不同部位的肿瘤微环境异质性可能导致治疗反应差异,而MVTT作为晚期HCC的常见特征,其对联合治疗的反应直接影响患者预后,但相关研究尚未见报道。因此,本研究旨在探讨一线仑伐替尼联合抗PD-1抗体对HCC不同器官病变的器官特异性反应率(OSRR),尤其是MVTT的反应,为个性化治疗策略提供依据。
2. 文献综述解析
作者围绕“晚期HCC系统治疗”的研究脉络,按治疗类型(单药酪氨酸激酶抑制剂(TKI)、免疫单药、联合治疗)梳理现有研究:
- 单药TKI:索拉非尼、仑伐替尼等通过抑制VEGF通路发挥抗瘤作用,但ORR低(20%-24%),无法有效控制进展;
- 免疫单药:nivolumab、pembrolizumab等抗PD-1抗体单药治疗晚期HCC的ORR仅15%-20%,且响应持续时间短;
- 联合治疗:抗血管生成药物与免疫治疗的协同作用已被证实,阿替利珠单抗联合贝伐珠单抗、仑伐替尼联合抗PD-1抗体的ORR均达36%以上,中位OS显著延长,但未关注不同器官病变的反应差异,尤其是MVTT这一关键预后因素。
现有研究的优势在于验证了联合治疗的协同效应,局限性在于缺乏对器官特异性反应的分析——HCC的异质性导致不同部位病变的治疗反应可能差异显著,而MVTT的控制情况直接影响患者生存,但此前无研究聚焦这一问题。
本文的创新点在于:① 首次报道一线仑伐替尼联合抗PD-1抗体的器官特异性反应率;② 首次分析MVTT对联合治疗的反应,及该反应与生存的关联;③ 为晚期HCC患者的“降期治疗”(通过联合治疗缩小MVTT,使不可切除患者获得手术机会)提供临床证据。
3. 研究思路总结与详细解析
整体框架
研究目标:探讨仑伐替尼联合抗PD-1抗体对HCC不同器官病变(肝内、MVTT、肝外转移)的反应差异,及MVTT反应与生存的关系;
核心科学问题:联合治疗对不同器官病变的反应是否存在差异?MVTT的反应是否影响患者生存?
技术路线:回顾性纳入患者→基线特征收集→联合治疗→每2个月影像学评估→统计OSRR、PFS、OS→生存分析→安全性评估。
3.1 患者入组与基线特征分析
实验目的:明确研究人群的基线特征,为后续疗效分析提供基线参考。
方法细节:回顾性纳入2018年10月至2020年5月在复旦大学附属中山医院接受治疗的60例不可切除HCC患者,纳入标准:① 病理或临床确诊HCC;② 接受一线仑伐替尼(8mg/天)联合≥3次抗PD-1抗体治疗;③ 有可测量病灶(RECIST v1.1)。收集患者性别、年龄、ECOG评分、HBsAg状态、Child-Pugh分级、BCLC分期、CNLC分期、病变部位(肝内、MVTT、肝外)等基线数据。
结果解读:患者以男性为主(55/60),平均年龄54岁;85% HBsAg阳性(提示乙肝相关性HCC);96.7%为Child-Pugh A级(肝功能储备良好);76.7%为BCLC C期(晚期);55%(33例)有MVTT,26.7%(16例)有肝外转移(肺、淋巴结、肾上腺、腹腔种植)。
产品关联:治疗药物中,仑伐替尼由Eisai Inc.提供;抗PD-1抗体包括nivolumab(Bristol-Myers Squibb)、camrelizumab(江苏恒瑞医药)、pembrolizumab(MSD)、sintilimab(信达生物)、toripalimab(君实生物);文献未提及其他实验产品(如影像学试剂)。
3.2 治疗方案与疗效评估
实验目的:评估仑伐替尼联合抗PD-1抗体的整体疗效。
方法细节:患者接受仑伐替尼(8mg/天,无论体重)联合抗PD-1抗体治疗:① nivolumab 3mg/kg每2周静脉输注;② camrelizumab 200mg每2周输注;③ pembrolizumab 200mg每3周输注;④ sintilimab 200mg每3周输注;⑤ toripalimab 240mg每3周输注。每2个月通过增强MRI(肝内病变、MVTT)和胸部CT(肝外转移)评估疗效,由研究者(INV)和独立影像评审(IIR)按RECIST v1.1标准判定最佳疗效:完全缓解(CR,病灶完全消失)、部分缓解(PR,病灶缩小≥30%)、稳定(SD,缩小<30%或增大<20%)、进展(PD,增大≥20%或新病灶)。
结果解读:60例患者中,INV与IIR评估的ORR均为33.3%(2例CR,18例PR),疾病控制率(DCR)分别为83.3%和85.0%;中位起效时间2个月,中位缓解持续时间(DOR)10.5个月,中位无进展生存期(PFS)7.0个月(95% CI 1.7-12.3),中位OS未达到(随访至2020年8月,35例仍在治疗)。
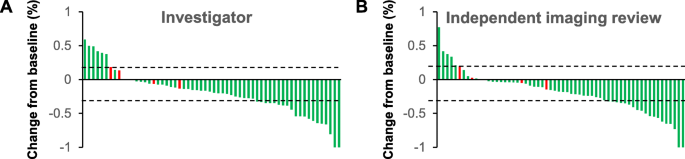
(图1:INV与IIR评估的肿瘤大小变化,红色代表因新病灶判定为PD的患者)
3.3 器官特异性反应分析
实验目的:探讨联合治疗对不同器官病变的反应差异,尤其是MVTT的反应。
方法细节:将病灶分为肝内病变、MVTT、肝外转移(肺、淋巴结、肾上腺、腹腔种植),其中MVTT的反应通过增强MRI评估:测量癌栓最大垂直直径,按RECIST v1.1标准判定疗效(CR:癌栓完全消失;PR:缩小≥30%;SD:缩小<30%或增大<20%;PD:增大≥20%)。统计各部位的OSRR(CR+PR患者比例),并分析同时有肝内病变和MVTT患者的差异反应。
结果解读:
- MVTT的OSRR(INV 54.5%、IIR 51.5%)显著高于肝内病变(32.8%)、肺转移(37.5%)、淋巴结转移(33.3%)(P=0.042);
- 33例同时有肝内病变和MVTT的患者中,18例存在差异反应,13例MVTT反应优于肝内病变;
- 18例MVTT达到CR/PR的患者中,6例接受手术切除,4例MVTT实现病理完全缓解(pCR),2例肝内病变pCR。
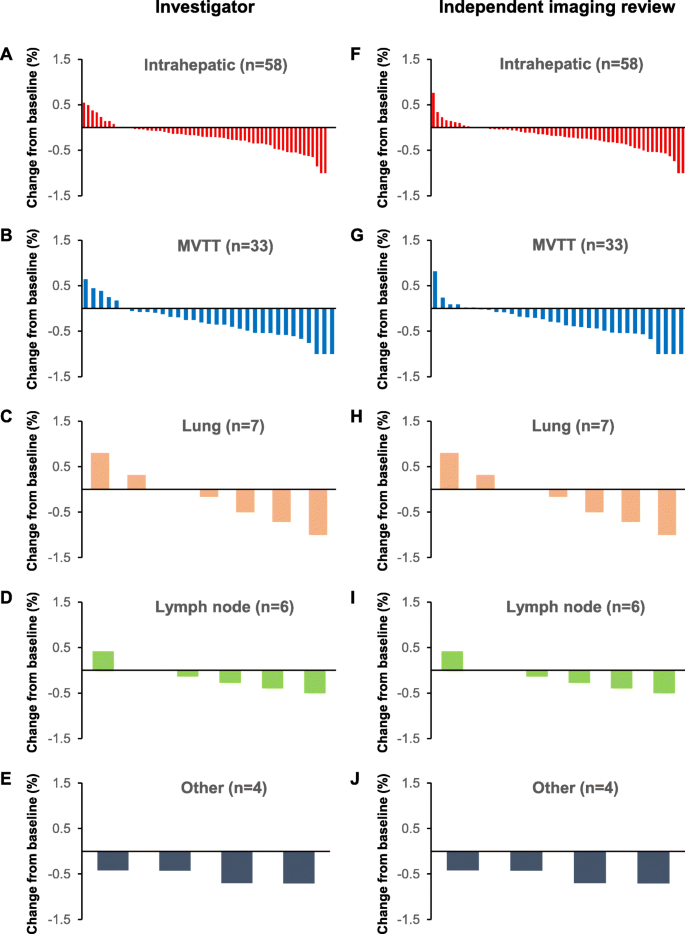
(图2:不同器官病变的肿瘤大小变化,MVTT的缩小比例更显著)
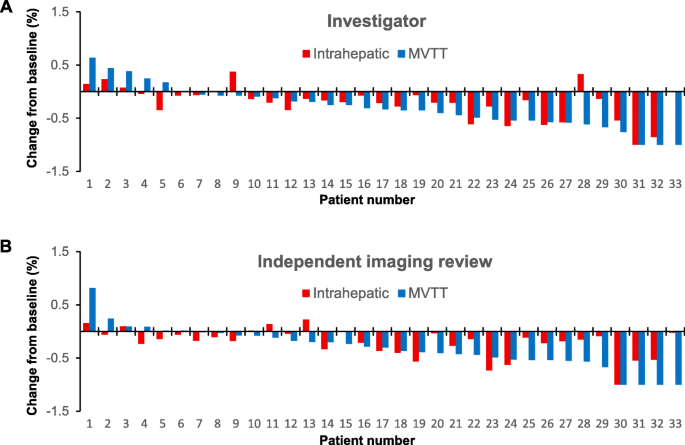
(图3:肝内病变与MVTT的差异反应,MVTT反应更优)
3.4 生存分析与安全性评估
实验目的:分析器官特异性反应与生存的关系,及治疗的安全性。
方法细节:用Kaplan-Meier法计算PFS和OS,log-rank检验比较不同反应组(如MVTT反应组vs无反应组)的生存差异;统计不良事件(AE)的发生率和严重程度(按CTCAE标准)。
结果解读:
- 生存分析:中位PFS 7.0个月(95% CI 1.7-12.3),中位OS未达到;MVTT反应组的OS显著长于无反应组(P=0.037),但肝内病变反应组与无反应组的OS无显著差异(P=0.198);
- 安全性:38.3%的患者出现3/4级AE,最常见为γ-谷氨酰转移酶升高(8.3%)、AST升高(8.3%)、消化道出血(6.7%)、白细胞减少(6.7%),未发生治疗相关死亡。

(图5:生存曲线,MVTT反应组的OS显著延长)
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本研究的核心Biomarker为“器官特异性治疗反应”,具体为:
- 观察指标:MVTT的OSRR(CR+PR患者比例);
- 筛选逻辑:通过回顾性分析联合治疗后不同器官病变的影像学反应,明确MVTT的反应是否优于其他部位,并验证其与生存的关联;
- 验证方法:每2个月用增强MRI评估MVTT的最大垂直直径变化,按RECIST v1.1标准判定疗效,结合手术病理验证pCR率。
研究过程详述
- Biomarker来源:患者治疗后的影像学评估结果(增强MRI);
- 验证方法:
- 影像学验证:每2个月通过增强MRI测量MVTT的最大垂直直径,计算缩小比例;
- 病理验证:对MVTT达到CR/PR的患者进行手术切除,通过苏木精-伊红染色(H&E染色)评估癌栓的坏死程度;
- 特异性与敏感性:MVTT的OSRR为54.5%(INV),显著高于肝内病变的32.8%(P=0.042);18例MVTT达到CR/PR的患者中,6例接受手术,4例实现pCR(敏感性66.7%)。
核心成果提炼
- 功能关联:MVTT的反应与生存显著相关——MVTT反应组的OS显著长于无反应组(P=0.037),提示MVTT的控制情况是晚期HCC的重要预后因素;
- 创新性:首次证实一线仑伐替尼联合抗PD-1抗体对MVTT的反应优于肝内病变,且部分患者可通过MVTT的完全缓解实现“降期治疗”(6例接受手术,4例pCR);
- 临床价值:MVTT的OSRR可作为预测生存的生物标志物,指导临床医生优先关注MVTT的控制,对达到CR/PR的患者可考虑手术切除,改善预后。
综上,本研究填补了晚期HCC联合治疗中“器官特异性反应”的研究空白,明确了MVTT对仑伐替尼联合抗PD-1抗体的高反应性及其预后价值,为晚期HCC的个性化治疗提供了重要依据。
