1. 领域背景与文献引入
文献英文标题:The landscape of bispecific T cell engager in cancer treatment;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗。
T细胞免疫治疗是近年来癌症治疗领域的革命性突破,主要分为两类:一类以免疫检查点抑制剂(immune checkpoint inhibitors, ICIs)为代表,通过阻断PD-1/PD-L1等免疫抑制通路,释放细胞毒性T细胞的“刹车”以清除肿瘤,但仅约20%-30%患者响应(核心原因是“冷肿瘤”缺乏肿瘤浸润T细胞);另一类以嵌合抗原受体T细胞(chimeric antigen receptor T cell, CAR-T)和双特异性T细胞衔接器(bispecific T cell engager, BiTE)为代表,通过直接激活或定向T细胞发挥抗瘤作用。其中,CAR-T通过基因修饰T细胞靶向肿瘤抗原,在血液瘤中疗效显著,但存在制备复杂、耗时(需2-4周体外扩增)、成本高的缺陷;BiTE作为双特异性抗体的重要子类,通过同时结合肿瘤细胞表面抗原与T细胞CD3分子,无需预激活即可诱导T细胞活化并裂解肿瘤,具有分子量小(约55 kDa,易扩散至肿瘤部位)、制备流程相对简单的优势。
然而,BiTE治疗仍面临诸多挑战:① 血液瘤中部分患者因抗原丢失(如CD19突变)或免疫检查点上调(如PD-L1表达增加)耐药;② 实体瘤中肿瘤微环境(tumor microenvironment, TME)的免疫抑制(如调节性T细胞(regulatory T cell, Treg)富集、髓源性抑制细胞(myeloid-derived suppressor cell, MDSC)浸润)导致响应率低;③ 治疗相关毒性(如细胞因子释放综合征(cytokine release syndrome, CRS)、神经毒性)限制剂量提升。当前研究热点聚焦于优化BiTE结构(如延长半衰期的HLE-BiTE)、开发联合疗法(如与ICIs联合逆转免疫抑制)及拓展实体瘤应用,但缺乏对BiTE临床进展、挑战及新型策略的系统总结——这正是本综述的核心目的:通过全面回顾BiTE的研究现状,为后续优化策略提供方向。
2. 文献综述解析
作者对现有研究的分类维度涵盖:① T细胞免疫治疗类型对比(ICIs、CAR-T、BiTE的机制与优劣);② BiTE临床应用场景(血液系统恶性肿瘤vs实体瘤);③ BiTE治疗的关键挑战(耐药机制、毒性);④ 新型策略开发(结构优化、联合疗法、innate免疫细胞应用)。
现有研究的关键结论:① BiTE在血液瘤中疗效显著,如全球首个获批的BiTE药物blinatumomab(CD19×CD3),在复发/难治性B细胞急性淋巴细胞白血病(relapsed/refractory B-cell acute lymphoblastic leukemia, R/R B-ALL)中,骨髓原始细胞<50%患者的完全缓解(complete remission, CR)率达65.5%,但骨髓原始细胞≥50%患者仅34.4%(P=0.039);② 实体瘤中BiTE仍处于早期探索阶段,如靶向前列腺特异性膜抗原(prostate-specific membrane antigen, PSMA)的AMG 212在转移性去势抵抗性前列腺癌(metastatic castration-resistant prostate cancer, mCRPC)中显示剂量依赖性PSA下降,靶向DLL3的AMG 757在R/R小细胞肺癌中客观缓解率(objective response rate, ORR)约15.8%(6/38例);③ 耐药机制主要包括肿瘤抗原丢失(如CD19突变、剪接变体导致表位改变)和免疫抑制(如PD-L1上调、Treg比例增加);④ 毒性以CRS和神经毒性为主,CRS与肿瘤负荷及药物剂量正相关(血液瘤中≥3级CRS发生率0-6%),神经毒性多表现为头晕、震颤(≥3级发生率5.5%-24%)。
现有研究的局限性:① 多数BiTE临床试验集中于血液瘤,实体瘤的TME复杂性(如纤维化、免疫抑制细胞浸润)未充分纳入研究;② 耐药机制的研究多基于血液瘤,实体瘤的抗原异质性与免疫逃逸机制未明确;③ 新型BiTE(如半衰期延长的HLE-BiTE、同时靶向免疫检查点的CiTE)的长期疗效与毒性尚未验证。本综述的创新价值在于:首次全面覆盖BiTE的临床进展、响应预测因子、挑战及新型策略,不仅总结了血液瘤与实体瘤的疗效差异,还系统解析了耐药机制(如CD19剪接变体的抗原逃逸),并拓展了BiTE的应用边界——包括针对innate免疫细胞(如γδ T细胞、自然杀伤(natural killer, NK)细胞)的衔接器开发,为BiTE的未来研究提供了全景式参考。
3. 研究思路总结与详细解析
本综述为系统性文献回顾,研究思路以“结构-机制-临床进展-挑战-策略”为逻辑闭环,核心环节包括BiTE结构与机制解析、临床进展总结、响应预测与毒性分析、新型策略开发。
3.1 双特异性T细胞衔接器的结构与机制解析
实验目的:明确BiTE的结构特征及其诱导T细胞抗瘤的分子机制。
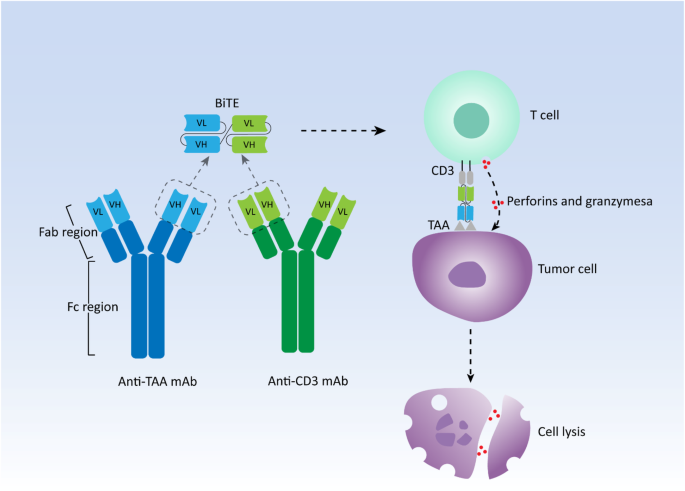
方法细节:通过回顾经典BiTE药物(如blinatumomab)的设计原理,结合基础研究文献,分析其与肿瘤细胞、T细胞的相互作用模式。BiTE的核心结构为两个串联的单链可变片段(single-chain variable fragment, scFv):一端靶向肿瘤相关抗原(tumor-associated antigen, TAA,如CD19、CD33),另一端靶向T细胞表面CD3分子(T细胞受体复合物的恒定链,确保泛T细胞激活);无Fc段(避免Fc受体介导的非特异性免疫反应),分子量约55 kDa。
结果解读:BiTE通过“桥接”肿瘤细胞与T细胞,形成“T细胞-肿瘤细胞”免疫突触,无需共刺激信号即可激活T细胞:① 激活的T细胞释放穿孔素与颗粒酶,直接裂解肿瘤细胞;② 分泌干扰素-γ(interferon-γ, IFN-γ)等细胞因子,增强局部免疫反应。与传统单克隆抗体相比,BiTE的优势在于:以低T细胞/肿瘤细胞比例(如1:10)即可发挥高效抗瘤作用(体外实验显示,BiTE诱导的肿瘤裂解效率是传统抗体的100-10000倍)。
3.2 临床进展总结(血液系统恶性肿瘤与实体瘤)
实验目的:系统总结BiTE在不同肿瘤类型中的疗效与安全性。
方法细节:检索PubMed、ClinicalTrials.gov等数据库,纳入2011-2021年发表的BiTE临床试验数据,按“血液瘤”与“实体瘤”分类分析。
结果解读:
- 血液系统恶性肿瘤:① B细胞急性淋巴细胞白血病(B-ALL):blinatumomab(CD19×CD3)在R/R B-ALL中,骨髓原始细胞<50%患者的CR率达65.5%(n=60),≥50%患者仅34.4%(n=40,P=0.039);② 急性髓系白血病(AML):AMG 330(CD33×CD3)在R/R AML中,≥120 μg/d剂量组的CR+CRi率约16.7%(3+4/42例);③ 多发性骨髓瘤(multiple myeloma, MM):AMG 420(BCMA×CD3)在R/R MM中,最大耐受剂量(maximum tolerated dose, MTD)400 μg/d队列的ORR达70%(5 CR+1 VGPR+1 PR/10例),且MRD阴性率高(5/10例)。
- 实体瘤:① 前列腺癌:AMG 212(PSMA×CD3)在mCRPC中显示剂量依赖性PSA下降(2例患者治疗超过1年);② 胶质母细胞瘤:AMG 596(EGFRvIII×CD3)在复发患者中获得1例PR(1/8例);③ 小细胞肺癌:AMG 757(DLL3×CD3,半衰期延长的HLE-BiTE)在R/R患者中ORR约15.8%(6/38例),且5例响应者的缓解持续时间超过8.8个月。
安全性:血液瘤中≥3级CRS发生率0-6%(如blinatumomab的3级CRS率6%),实体瘤中CRS多为1-2级(如AMG 757的CRS发生率43%,无≥3级事件);神经毒性是BiTE的另一主要毒性(如blinatumomab的≥3级神经毒性发生率5.5%-24%),表现为头晕、震颤,多发生于治疗第1周期。
3.3 响应预测因子与毒性机制分析
实验目的:识别BiTE治疗的响应预测生物标志物,解析毒性的分子机制。
方法细节:通过回顾blinatumomab等药物的临床试验数据,关联患者基线特征(如疾病负荷、Treg比例)与治疗响应率;结合体外实验与动物模型,解析CRS与神经毒性的发生机制。
结果解读:
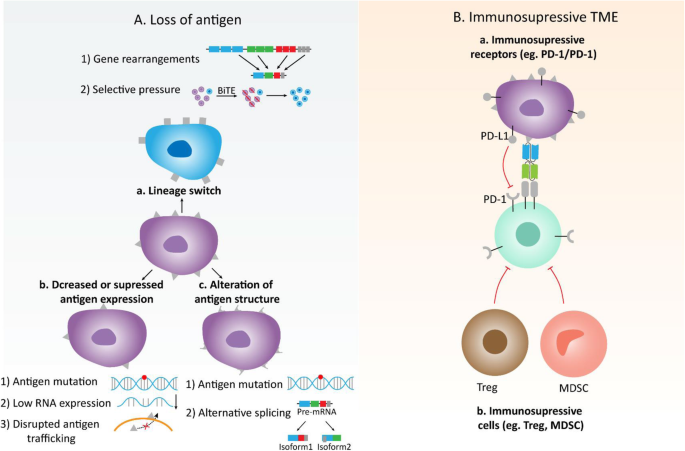
- 响应预测因子:① 疾病负荷:骨髓原始细胞≥50%的R/R B-ALL患者,blinatumomab响应率显著低于<50%患者(34.4% vs 65.5%,P=0.039);② 肿瘤抗原密度:CD19分子密度<1000个/细胞的B-ALL细胞,BiTE诱导的T细胞裂解效率下降50%(体外实验);③ Treg比例:blinatumomab响应者的外周血Treg比例为4.82%(95% CI 1.79%-8.34%,n=22),非响应者为10.25%(95% CI 3.36%-65.9%,n=20),以8.525%为 cutoff值可100%识别响应者(22/22),并排除70%非响应者(14/20);④ CD19剪接变体:预处理患者中,blinatumomab非响应者的CD19 ex2part( exon 2部分缺失的剪接体)水平显著高于响应者(P=0.025,n=15);复发患者的CD19 ex2part水平较预处理时升高(P=0.0002,n=8),提示其通过改变CD19表位、阻断BiTE结合导致耐药。
- 毒性机制:① CRS:由T细胞大量活化释放IL-6、IFN-γ等细胞因子引发,与肿瘤负荷(肿瘤细胞数越多,T细胞激活越强烈)和药物剂量正相关;② 神经毒性:可能与T细胞黏附内皮细胞并穿过血脑屏障有关(临床研究发现,BiTE治疗后患者脑脊液中T细胞比例增加,且体外实验显示T细胞与脑内皮细胞的黏附可诱导内皮活化)。
3.4 新型策略与联合疗法开发
实验目的:探索优化BiTE疗效、降低毒性的创新策略。
方法细节:回顾近年来BiTE结构优化(如HLE-BiTE、CiTE)、联合疗法(如与ICIs、化疗联合)及innate免疫细胞衔接器的研究进展。
结果解读:
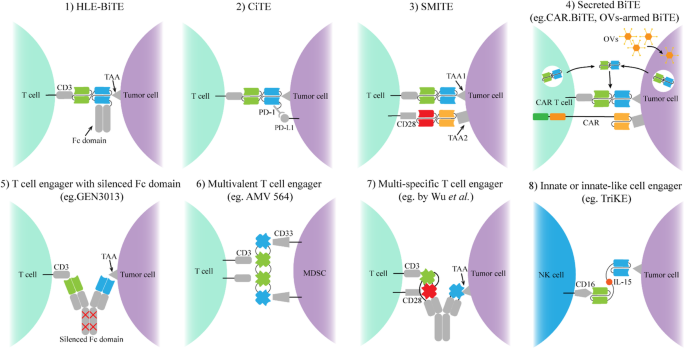
- 结构优化:① 半衰期延长的HLE-BiTE:通过添加Fc段(如AMG 673,CD33×CD3),将半衰期从数小时延长至数天,实现每周1次输注(替代传统BiTE的持续静脉输注),在R/R AML中显示初步疗效(1例CRi/30例);② checkpoint inhibitory T cell engager(CiTE):同时靶向TAA与PD-1/PD-L1(如anti-CD33×anti-PD-L1 BiTE),在AML细胞系中可逆转PD-L1介导的免疫抑制,增强T细胞裂解效率;③ simultaneous multiple interaction T-cell engaging(SMiTE):同时提供CD3激活信号与CD28共刺激信号(如anti-TAA×anti-CD3×anti-CD28三特异性抗体),可增强T细胞的长期活化与增殖。
- 联合疗法:① 与化疗联合:blinatumomab与Hyper-CVAD化疗联合用于新诊断B-ALL,CR率达100%(27/27例),且MRD阴性率96%;② 与ICIs联合:blinatumomab与nivolumab(PD-1抑制剂)联合用于R/R B-ALL,CR率达80%(4/5例),且PD-L1上调患者的响应率显著提升;③ 与靶向治疗联合:blinatumomab与酪氨酸激酶抑制剂(如dasatinib)联合用于Ph+ B-ALL,CR率达98%(62/63例),分子缓解率随blinatumomab周期增加(从29.3%升至80%)。
- innate免疫细胞衔接器:除T细胞外,研究者开始开发针对innate免疫细胞的衔接器,如靶向γδ T细胞(Vγ9Vδ2亚型,MHC非依赖的抗瘤活性)的BiTE(如anti-EGFR×anti-Vγ9Vδ2),在小鼠模型中显示强效抗瘤作用;针对NK细胞的bispecific killer cell engager(BiKE,如anti-CD16×anti-CD33)与trispecific killer engager(TriKE,添加IL-15片段增强NK细胞存活),在AML中显示协同抗瘤效应。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
本综述涉及的BiTE相关Biomarker可分为三类:① 肿瘤抗原类(CD19、CD33、BCMA、PSMA、EGFRvIII、DLL3):作为BiTE的靶标,需满足“肿瘤细胞高表达、正常组织低表达”的条件,通过临床试验验证其有效性;② 响应预测类(疾病负荷、肿瘤抗原密度、Treg比例、CD19 ex2part):通过临床试验数据关联或回顾性分析,识别与响应率相关的指标;③ 毒性相关类(IL-6水平):通过CRS患者的血清检测,验证其与毒性严重程度的相关性。筛选逻辑遵循“临床关联-基础验证-临床应用”的闭环:先通过临床试验观察指标与疗效的相关性,再通过基础实验验证其功能(如CD19 ex2part的抗原逃逸机制),最后通过回顾性分析确定 cutoff值(如Treg比例的8.525%)。
研究过程详述
- 肿瘤抗原类Biomarker:CD19在B-ALL细胞中高表达(95%以上患者),且仅局限于B细胞系(正常T细胞、髓细胞无表达),通过blinatumomab的Ⅲ期临床试验验证其作为BiTE靶标的有效性(CR率65.5%);CD33在AML原始细胞中表达(80%以上患者),通过AMG 330的Ⅰ期试验验证其靶标价值(CR+CRi率16.7%);BCMA在MM浆细胞中高表达(90%以上患者),通过AMG 420的Ⅰ期试验验证(ORR 70%)。
- 响应预测类Biomarker:① 疾病负荷:通过blinatumomab的Ⅲ期试验(n=100例R/R B-ALL),发现骨髓原始细胞≥50%患者的CR率显著低于<50%患者(34.4% vs 65.5%,P=0.039);② 肿瘤抗原密度:通过体外实验(n=5株B-ALL细胞系),发现CD19密度<1000个/细胞时,T细胞裂解效率下降50%;③ Treg比例:通过回顾性分析(n=42例R/R B-ALL患者,22例响应者、20例非响应者),发现响应者的外周血Treg比例(4.82%)显著低于非响应者(10.25%),以8.525%为 cutoff值可100%识别响应者;④ CD19 ex2part:通过测序分析(n=7例R/R B-ALL患者),发现耐药患者的CD19 ex2part水平显著高于响应者(P=0.025),且复发患者的水平较预处理时升高(P=0.0002)。
- 毒性相关Biomarker:IL-6水平通过CRS患者的血清检测(n=20例)验证,与CRS严重程度正相关(3级CRS患者的IL-6水平是1级患者的5倍以上),且tocilizumab(IL-6受体抑制剂)可快速缓解CRS症状。
核心成果提炼
- 肿瘤抗原是BiTE治疗的基础:CD19、BCMA等靶点的“肿瘤特异性”已被临床试验验证,是BiTE开发的核心依据;
- 响应预测Biomarker指导患者筛选:疾病负荷(骨髓原始细胞≥50%)、Treg比例(>8.525%)、CD19 ex2part(预处理水平高)可作为BiTE治疗的“排除指标”,降低无效治疗的风险;
- 新型Biomarker揭示耐药机制:CD19 ex2part是首次被明确的“抗原逃逸型”Biomarker(通过改变表位而非降低表达导致耐药),为开发“覆盖剪接变体”的BiTE提供了靶点;
- 毒性Biomarker指导临床干预:IL-6水平可作为CRS的早期预警指标,tocilizumab的预防性使用可降低严重CRS的发生率。
本综述全面总结了BiTE的研究现状与未来方向,为BiTE的结构优化、联合疗法开发及实体瘤应用提供了关键参考,也为肿瘤免疫治疗的“精准化”(基于Biomarker的患者分层)奠定了基础。
