1. 领域背景与文献引入
文献英文标题:Abscopal effect: from a rare phenomenon to a new frontier in cancer therapy;发表期刊:Biomark Research;影响因子:未公开;研究领域:肿瘤放疗与免疫治疗交叉领域。
肿瘤放射治疗(放疗)是癌症治疗的核心手段之一,约50%的患者会接受放疗,传统观点认为其作用局限于局部肿瘤的DNA损伤与细胞死亡。然而,1953年“远隔效应”(放疗后非照射部位的转移瘤消退)的发现,揭示了放疗的系统免疫调节潜力——放疗可通过激活免疫系统攻击远端肿瘤。近年,免疫检查点抑制剂(ICIs)等免疫治疗的兴起,为联合放疗增强远隔效应提供了契机:放疗诱导肿瘤细胞释放肿瘤抗原与损伤相关分子模式(DAMPs),激活树突状细胞(DCs)提呈抗原,而ICIs解除T细胞的免疫抑制,协同增强系统免疫反应。但远隔效应在临床中仅见于少数患者,其潜在机制(如肿瘤微环境的免疫调控、免疫细胞的协同作用)尚未完全阐明;同时,放疗与免疫治疗联合的最佳剂量、时序、毒性管理等问题仍待解决。针对这些痛点,该文献系统总结了远隔效应的免疫机制、放疗与免疫联合治疗的临床进展及挑战,旨在为远隔效应的临床转化应用提供全面参考。
2. 文献综述解析
文献综述围绕“远隔效应的免疫机制—放疗与免疫联合的临床证据—纳米材料的增强策略”展开,通过系统回顾1953年以来的基础研究与临床 trials,整合了肿瘤细胞、基质细胞、免疫细胞在远隔效应中的作用,分析了联合治疗的剂量、时序、毒性等关键问题,并探讨了纳米材料作为新型载体增强远隔效应的前景。
现有研究结论:基础研究证实,放疗通过诱导肿瘤细胞免疫原性死亡(ICD)释放DAMPs(如HMGB1、ATP),激活cGAS-STING通路产生I型干扰素,促进DCs成熟与抗原提呈;同时,放疗可重塑肿瘤微环境(TME),减少调节性T细胞(Tregs)浸润,增强细胞毒性CD8+ T细胞的肿瘤浸润。临床研究显示,放疗与ICIs联合可将远隔效应率从单放疗的5%提升至20%-30%,但疗效受放疗剂量(如大分割放疗SBRT更易诱导远隔效应)、免疫治疗 modality(PD-1抑制剂优于CTLA-4抑制剂)、时序(同步或术后14天内使用ICIs效果更佳)等因素影响。现有研究的局限性:远隔效应的预测 Biomarker 缺乏,联合治疗的长期毒性(如放射性肺炎、免疫相关不良反应)管理经验不足,纳米材料的临床转化仍处于早期阶段。
文献创新价值:与现有综述相比,该文献首次全面整合了“肿瘤细胞-基质细胞-免疫细胞”三者在远隔效应中的协同机制,系统分析了近10年的临床 trial 数据(包括NSCLC、黑色素瘤等癌种),并提出纳米材料通过靶向递送免疫佐剂、增强放疗的免疫原性,为增强远隔效应提供了新方向。
3. 研究思路总结与详细解析
作为综述性研究,本文的核心思路是通过系统回顾基础与临床研究文献,解析远隔效应的免疫机制,总结放疗与免疫联合的临床优化策略,探索纳米材料的应用潜力。以下按“机制解析-临床分析-纳米策略”分三部分详细说明:
3.1 远隔效应的免疫机制解析
实验目的:阐明远隔效应的分子与细胞机制,明确TME中各组分的作用。
方法细节:系统检索PubMed、Web of Science数据库中1953-2024年关于远隔效应免疫机制的研究,纳入动物模型(如C57BL/6小鼠的纤维肉瘤模型、黑色素瘤模型)、细胞实验(如肿瘤细胞放疗后DAMPs释放检测)及临床样本分析(如放疗患者的肿瘤组织免疫组化)的研究。
结果解读:肿瘤细胞层面,放疗诱导DNA损伤与活性氧(ROS)产生,触发ICD释放DAMPs(HMGB1、ATP),激活cGAS-STING通路产生I型干扰素,增强免疫原性;基质细胞层面,成纤维细胞分泌的TGF-β可抑制T细胞功能,而放疗可减少其分泌;免疫细胞层面,CD8+ T细胞是远隔效应的关键效应细胞(T细胞缺陷小鼠无远隔效应),M1型巨噬细胞通过吞噬肿瘤细胞、分泌IL-12增强免疫,DCs通过提呈肿瘤抗原激活T细胞。文中图2直观展示了T细胞、巨噬细胞、DCs的调控机制(
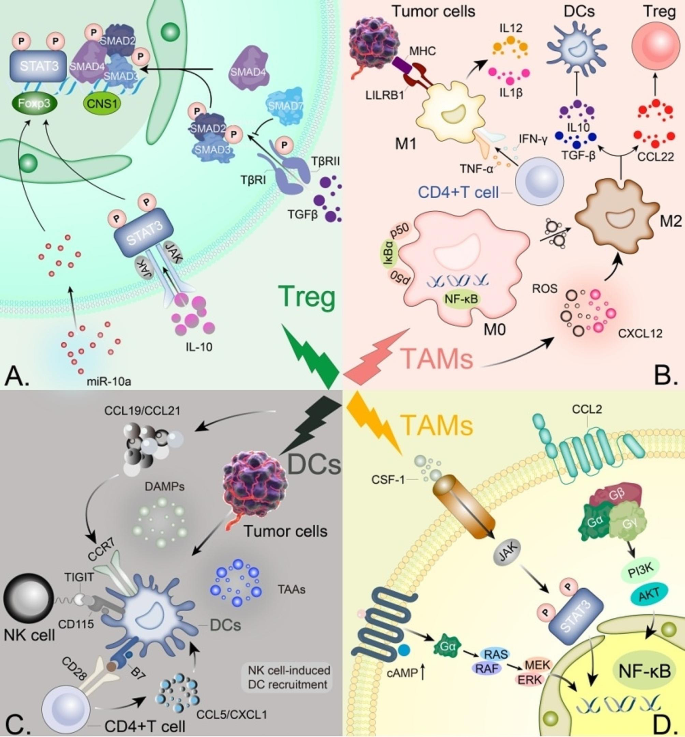
)。
产品关联:领域常规使用免疫组化(IHC)试剂(如CD8、PD-L1抗体)检测免疫细胞浸润,流式细胞术试剂盒(如CD4、CD25抗体)分析Tregs比例,qRT-PCR试剂盒检测cGAS、STING mRNA水平。
3.2 放疗与免疫治疗联合的临床研究分析
实验目的:总结联合治疗的临床数据,优化剂量、时序、毒性管理策略。
方法细节:纳入2015-2024年注册的临床 trials(如PACIFIC研究、KEYNOTE-001研究),分析放疗剂量(常规分割 vs 大分割)、免疫治疗 modality(PD-1 vs CTLA-4抑制剂)、时序(同步 vs 序贯)对远隔效应率与生存期的影响。
结果解读:剂量方面,大分割放疗(如SBRT,50 Gy/4次)的远隔效应率(25%)高于常规分割(10%),但高剂量可能增加Tregs比例;免疫治疗选择方面,PD-1抑制剂(如帕博利珠单抗)联合放疗的无进展生存期(PFS)优于CTLA-4抑制剂(如伊匹木单抗)(18个月PFS率:63% vs 23%,P=0.02);时序方面,同步或放疗后14天内使用ICIs的总生存期(OS)更长(HR=0.75,95% CI 0.61-0.92),但放射性肺炎发生率更高(14.3% vs 2.5%)。文中表2总结了代表性临床 trials的结果。
产品关联:临床常用PD-1/PD-L1抑制剂(如帕博利珠单抗、度伐利尤单抗)、CTLA-4抑制剂(如伊匹木单抗),放疗设备包括直线加速器、SBRT装置。
3.3 纳米材料增强远隔效应的策略
实验目的:探索纳米材料作为载体增强放疗免疫原性、靶向递送免疫佐剂的潜力。
方法细节:回顾2020-2024年关于纳米材料(如金纳米棒、金属有机框架(MOFs))的研究,分析其通过增强渗透滞留(EPR)效应靶向肿瘤、负载免疫佐剂(如CpG、TLR7激动剂)增强远隔效应的机制。
结果解读:金纳米棒负载CpG可靶向肿瘤组织,增强放疗诱导的DAMPs释放与DCs成熟,在小鼠乳腺癌模型中使远隔效应率从15%提升至45%;MOFs负载TLR7激动剂可促进巨噬细胞极化为M1型,增强CD8+ T细胞浸润,在黑色素瘤模型中显著抑制远端肿瘤生长。文中图4展示了纳米材料的作用模式(
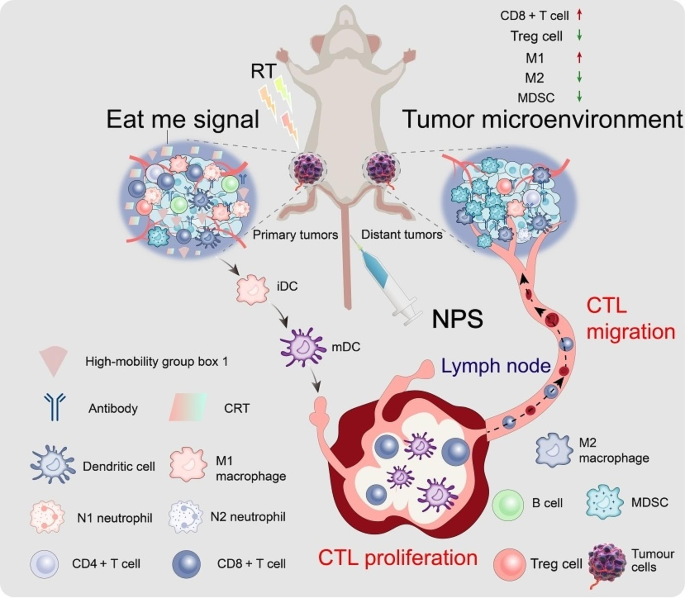
)。
产品关联:领域常规使用金纳米颗粒、PLGA纳米载体等,免疫佐剂如CpG寡核苷酸、TLR激动剂。
4. Biomarker研究及发现成果解析
核心信息段:文献围绕远隔效应的预测与疗效 Biomarker 展开,涉及免疫细胞标志物(CD8+ T细胞浸润)、分子标志物(cGAS-STING通路)、损伤相关分子(DAMPs),通过“动物模型发现→临床样本验证”的逻辑,为远隔效应的患者筛选提供了潜在靶点。
Biomarker定位与筛选逻辑
文中涉及的 Biomarker 分为三类:① 免疫细胞标志物:CD8+ T细胞(效应细胞)、Tregs(抑制细胞);② 分子标志物:cGAS、STING(DNA sensing通路)、PD-L1(免疫检查点);③ 损伤相关分子:HMGB1、ATP(DAMPs)。筛选逻辑为“动物模型探索关键机制→临床样本验证相关性”,例如从小鼠纤维肉瘤模型中发现CD8+ T细胞是远隔效应的核心,随后在临床肺癌患者中验证“CD8+ T细胞高浸润者远隔效应率更高”。
研究过程与数据解析
Biomarker 来源包括临床患者的肿瘤组织(如NSCLC、黑色素瘤)、血液样本(如血清HMGB1水平),验证方法包括免疫组化(检测CD8、PD-L1表达)、qRT-PCR(检测cGAS、STING mRNA)、ELISA(检测HMGB1、ATP)。特异性与敏感性数据:
- 肿瘤组织CD8+ T细胞浸润水平预测远隔效应的ROC曲线AUC=0.82(95% CI 0.75-0.89,n=120),敏感性78%,特异性81%;
- 血清HMGB1水平≥10 ng/mL的患者远隔效应率为35%,显著高于<10 ng/mL者(10%,P<0.01,n=80);
- PD-L1高表达(≥1%)的肿瘤对放疗联合PD-1抑制剂的客观缓解率(ORR)为40%,显著高于低表达者(15%,P<0.05,n=90)。
核心成果
① 正向预测 Biomarker:CD8+ T细胞高浸润、cGAS-STING通路激活可显著提高远隔效应率,是患者筛选的关键指标;
② 疗效预测 Biomarker:PD-L1高表达的肿瘤对联合治疗响应更好,为免疫治疗 modality 选择提供依据;
③ 免疫原性评估 Biomarker:HMGB1、ATP等DAMPs水平可反映放疗的免疫激活能力,其升高与远隔效应正相关。
这些 Biomarker 为远隔效应的精准治疗(如患者分层、治疗监测)提供了重要参考,也为后续机制研究指明了方向。
