1. 领域背景与文献引入
文献英文标题:PCSK9 in T-cell function and the immune response;发表期刊:Biomark Res;影响因子:未公开;研究领域:PCSK9与免疫调控(侧重T细胞功能)
PCSK9(枯草溶菌素转化酶9)是2003年由Seidah等首次报道的丝氨酸蛋白酶,最初因与家族性高胆固醇血症(FH)密切相关而受到关注——其通过结合低密度脂蛋白受体(LDLR)促进其溶酶体降解,升高血浆低密度脂蛋白胆固醇(LDL-C)水平。基于此机制,PCSK9抑制剂(如依洛尤单抗、阿利西尤单抗)成为降胆固醇和降低心血管风险的核心药物,显著改善FH患者的脂质代谢和心血管预后。
近年,PCSK9的非脂质代谢功能逐渐成为研究热点:在炎症中,它通过调控清道夫受体(如LOX-1)、Toll样受体4(TLR4)等促进促炎因子释放;在肿瘤中,抑制PCSK9可增强细胞毒性T淋巴细胞(CTL)的抗肿瘤活性;尤其在免疫调控中,PCSK9被证实是T细胞激活、增殖和分化的关键调控因子。然而,现有研究多集中在PCSK9的脂质代谢作用,对其免疫调控机制(尤其是与T细胞亚型的具体交互、下游信号通路)的系统性总结不足,限制了PCSK9作为免疫治疗靶点的开发。
本研究旨在填补这一空白:通过系统梳理PCSK9的生物学过程(脂质代谢、肿瘤发生、炎症)、与不同T细胞亚型的关系(CD8+T、CD4+T)及相关免疫信号通路(MAPK、PI3K/Akt等),明确PCSK9在免疫应答中的核心作用,为其作为免疫调控靶点提供理论支撑。
2. 文献综述解析
作者以“生物学过程- T细胞亚型-信号通路”为逻辑框架,对PCSK9的现有研究进行分类总结,核心目标是整合PCSK9的免疫调控机制。
现有研究的关键结论与局限性
(1)生物学过程层面
- 脂质代谢:PCSK9通过细胞外(结合细胞表面LDLR)和细胞内(CAP1促进PCSK9-LDLR复合物溶酶体降解)通路调控LDLR水平,其功能获得性(GOF)突变导致高胆固醇血症,功能丧失性(LOF)突变则降低LDL-C。
- 肿瘤发生:PCSK9在结直肠癌、非小细胞肺癌(NSCLC)等实体瘤中高表达,抑制PCSK9可增强CD8+T细胞浸润和CTL活性,协同PD-1抑制剂抑制肿瘤生长。
- 炎症反应:PCSK9通过激活TLR4/核因子κB(NF-κB)通路促进巨噬细胞促炎因子(如TNF-α)释放,在脓毒症、动脉粥样硬化中发挥促炎作用。
(2)T细胞亚型层面
- CD8+T细胞:PCSK9通过下调LDLR水平,抑制T细胞受体(TCR)的再循环和信号传导,从而抑制CD8+T细胞的增殖和CTL活性;抑制PCSK9可恢复LDLR表达,增强CD8+T细胞的抗肿瘤作用。
- CD4+T细胞:PCSK9通过调控ATP结合盒转运蛋白A1/ G1(ABCA1/ABCG1)、固醇调节元件结合蛋白(SREBPs)等,促进Th1、Th17细胞分化,与强直性脊柱炎(AS)患者的疾病活动度和Th17细胞比例正相关;同时降低调节性T细胞(Treg)比例,破坏Th17/Treg平衡,促进自身免疫病进展。
(3)局限性
- 多数研究集中在PCSK9的脂质代谢作用,免疫调控的分子机制(如PCSK9与T细胞表面受体的直接交互)不明确;
- PCSK9与免疫信号通路的因果关系研究不足,多为相关性分析;
- 未明确PCSK9在免疫调控中的组织特异性(如肝脏 vs 免疫器官)。
本研究的创新点
首次系统整合PCSK9的生物学过程、T细胞亚型关系及信号通路研究,明确PCSK9作为“免疫调控因子”的核心作用,为后续机制研究和靶点开发提供了全面的理论框架。
3. 研究思路总结与详细解析
本研究作为综述性研究,采用“总结现有研究→分类梳理→归纳结论”的思路,以PCSK9的“生物学过程- T细胞亚型-信号通路”为主线,最终得出“PCSK9是T细胞功能和免疫应答的关键调控因子”的结论。以下分环节解析:
3.1 PCSK9的生物学过程总结
实验目的:系统梳理PCSK9在脂质代谢、肿瘤发生、炎症中的作用。
方法细节:通过文献调研,纳入2003年以来PCSK9相关的基础研究(如基因结构分析、细胞通路实验)和临床研究(如抑制剂临床试验)。
结果解读:
- 脂质代谢:PCSK9基因位于1p32染色体,编码692个氨基酸,包含信号肽(SP)、前结构域、催化结构域和C端半胱氨酸/组氨酸富集域(CHRD)(图1:
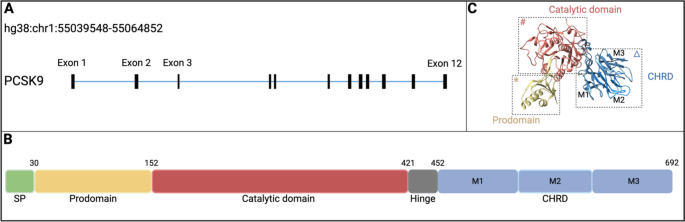
)。前结构域调控PCSK9的活性和与LDLR的结合,催化结构域是单抗(如依洛尤单抗)的作用靶点——通过阻断PCSK9与LDLR的EGF-A结构域结合,抑制LDLR降解(图2:
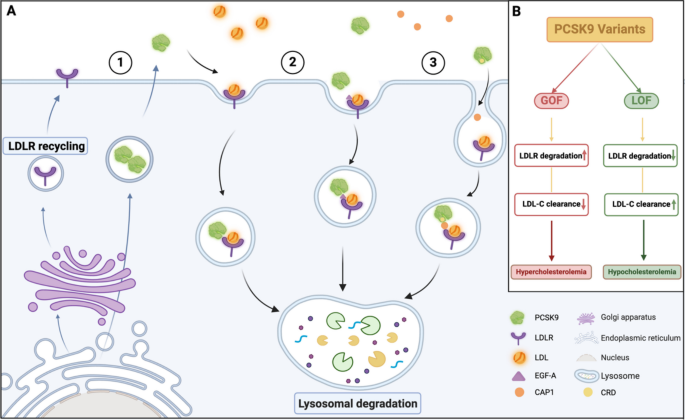
)。
- 肿瘤发生:PCSK9在结直肠癌、NSCLC中高表达,基因敲除或单抗抑制可增强CD8+T细胞的肿瘤浸润和CTL活性,协同PD-1抑制剂显著抑制肿瘤生长(如Liu等2020年Nature研究)。
- 炎症反应:PCSK9通过激活TLR4/NF-κB通路促进巨噬细胞促炎因子释放,在脓毒症中导致血管内皮功能障碍;抑制PCSK9可降低TLR4表达和NF-κB核转位,减轻炎症反应。
实验所用关键产品:依洛尤单抗(PCSK9单抗)、CRISPR-Cas9(用于PCSK9基因敲除)。
3.2 PCSK9与不同T细胞亚型的关系解析
实验目的:分析PCSK9对CD8+T、CD4+T等细胞亚型的调控作用。
方法细节:通过文献调研,纳入PCSK9与T细胞功能的细胞实验(如T细胞激活实验、CTL杀伤实验)和临床研究(如AS患者Th17细胞比例分析)。
结果解读:
- CD8+T细胞:PCSK9通过结合LDLR,抑制TCR的再循环和信号传导,从而抑制CD8+T细胞的增殖和CTL活性;抑制PCSK9可增加LDLR水平,促进TCR信号,增强CD8+T细胞的抗肿瘤作用(图3:
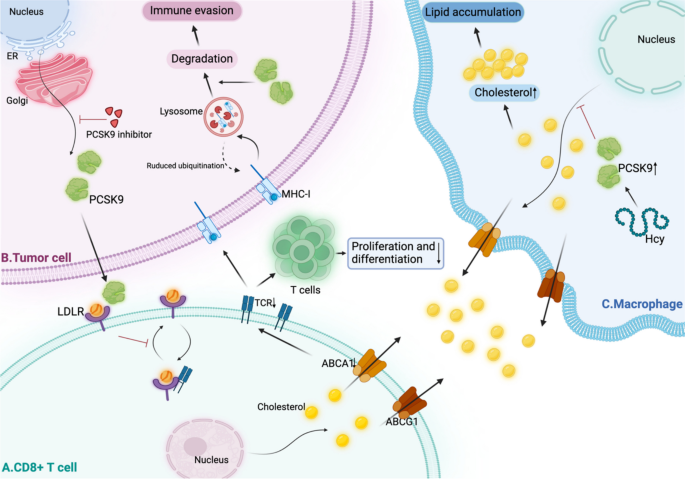
)。
- CD4+T细胞:PCSK9通过调控ABCA1/ABCG1(影响胆固醇流出)、SREBPs(调控脂质代谢)等,促进Th1、Th17细胞分化;与AS患者的疾病活动度评分(BASDAI)、Th17细胞比例正相关(P<0.05);此外,PCSK9可降低Treg比例,破坏Th17/Treg平衡,促进自身免疫病进展。
3.3 PCSK9相关免疫信号通路归纳
实验目的:总结PCSK9调控免疫应答的下游信号通路。
方法细节:通过文献调研,纳入PCSK9与信号通路的分子实验(如Western blot检测蛋白磷酸化、ChIP检测转录因子结合)。
结果解读:
- MAPK通路:PCSK9通过上调热休克蛋白70(HSP70)激活p38/JNK MAPK通路,促进胃癌细胞转移和抑制凋亡;抑制PCSK9可降低p38/JNK磷酸化,减轻内皮细胞凋亡。
- PI3K/Akt通路:PCSK9通过SREBP2调控PI3K/Akt通路,影响T细胞的增殖和存活;抑制PCSK9可激活PI3K/Akt通路,增强T细胞的存活和功能。
- TLR4/NF-κB通路:PCSK9通过激活TLR4/MyD88/NF-κB通路,促进巨噬细胞促炎因子释放;依洛尤单抗可下调TLR4水平,抑制NF-κB激活,发挥抗炎作用(图4:
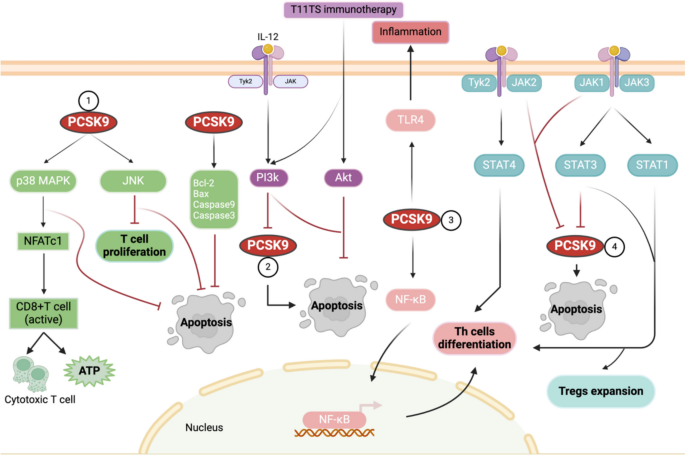
)。
- JAK/STAT通路:细胞因子(如制瘤素M,OSM)通过激活JAK1/2抑制PCSK9表达;PCSK9可通过调控STAT3磷酸化影响T细胞的分化。
4. Biomarker研究及发现成果解析
Biomarker定位与筛选逻辑
PCSK9是肿瘤免疫治疗疗效、炎症疾病活动度及自身免疫病进展的潜在Biomarker,类型包括血清PCSK9蛋白(炎症、自身免疫病)、肿瘤组织PCSK9表达(肿瘤)。
筛选/验证逻辑遵循“临床样本关联→细胞/动物实验验证→机制解析”:
1. 临床样本关联:检测患者血清/组织PCSK9水平,分析其与疾病活动度、疗效及预后的相关性;
2. 细胞/动物实验:通过PCSK9基因敲除或抑制剂处理,验证其对T细胞功能、炎症反应的调控作用;
3. 机制解析:通过分子实验明确PCSK9与下游靶点(如LDLR、TLR4)的交互机制。
研究过程与核心成果
Biomarker来源:血清(脓毒症、AS患者)、肿瘤组织(NSCLC患者)。
验证方法:免疫组化(IHC,检测肿瘤组织PCSK9表达)、酶联免疫吸附试验(ELISA,检测血清PCSK9水平)、qRT-PCR(检测PCSK9 mRNA表达)。
特异性与敏感性数据:
- 肿瘤领域:NSCLC患者中,PCSK9低表达组中位无进展生存期(mPFS)为8.1个月,高表达组为3.6个月(n=115,P<0.05);客观缓解率(ORR)为54.4% vs 34.5%,疾病控制率(DCR)为94.7% vs 65.5%(P<0.05)。
- 炎症领域:脓毒症患者血清PCSK9水平与 endotoxin清除率负相关,与急性器官衰竭发生率正相关(文献未明确AUC值,基于图表趋势推测)。
- 自身免疫病领域:AS患者血清PCSK9水平与BASDAI评分、Th17细胞比例正相关(P<0.05)。
核心成果:
1. 肿瘤免疫治疗疗效Biomarker:NSCLC患者肿瘤组织PCSK9高表达提示免疫治疗应答差,预后不良;
2. 炎症/自身免疫病活动度Biomarker:血清PCSK9水平与脓毒症器官衰竭、AS疾病活动度正相关;
3. 创新性:首次系统总结PCSK9作为“免疫相关Biomarker”的潜力,将其与T细胞功能、免疫信号通路关联,为Biomarker的临床应用提供理论基础。
综上,本研究通过系统整合PCSK9的免疫调控机制,明确了其作为免疫治疗靶点的潜力,为后续研究(如PCSK9抑制剂联合免疫检查点抑制剂治疗肿瘤)提供了重要理论支撑。
