1. 领域背景与文献引入
文献英文标题:Vav2 protein overexpression marks and may predict the aggressive subtype of ductal carcinoma in situ;发表期刊:Biomark Res;影响因子:未公开;研究领域:乳腺导管原位癌(DCIS)生物标志物研究。
乳腺导管原位癌(DCIS)是乳腺最常见的非浸润性恶性病变,约占新诊断乳腺癌的25%。尽管大多数DCIS预后良好,但约20%-30%的患者会在诊断后10-20年内进展为浸润性乳腺癌(IBC)。然而,目前临床缺乏有效的生物标志物来区分具有进展风险的DCIS患者——这些高风险 lesions在组织学上与低风险 lesions难以鉴别,导致部分患者接受过度治疗,而部分高风险患者未得到足够干预。当前领域研究热点聚焦于挖掘DCIS进展为IBC的分子标志物,尤其是能反映肿瘤侵袭潜能的早期分子改变;未解决的核心问题是缺乏特异性、可定量的生物标志物,用于预测DCIS的侵袭性进展。
基于此,本研究团队提出假设:能区分“单纯DCIS”与“伴发侵袭DCIS”的可测量参数,可作为进展性原位癌的诊断标志物。研究针对三种在IBC侵袭中发挥关键作用的候选蛋白——胰岛素样生长因子I受体(IGF-IR)、Ras相关蛋白1(Rap1)、Vav2癌蛋白,通过定量分析其在DCIS中的表达模式,探讨其与肿瘤分子亚型(ER/PR/HER2状态)及侵袭潜能的关联,旨在为DCIS的风险分层提供新型生物标志物。
2. 文献综述解析
本研究的文献综述围绕“DCIS进展为IBC的预测标志物缺失”这一核心问题展开,评述逻辑可概括为:回顾候选蛋白在乳腺癌侵袭中的功能→指出DCIS研究中的空白→明确本研究的补充方向。
现有研究对三种候选蛋白的功能已有部分阐释:IGF-IR作为酪氨酸激酶受体,是癌症细胞增殖、迁移的关键驱动因子,其过表达与ER阳性乳腺癌的他莫昔芬耐药密切相关;Rap1是小GTP酶家族成员,与乳腺上皮细胞极性丧失、体外侵袭能力及裸鼠致瘤性有关;Vav2属于Vav家族鸟嘌呤核苷酸交换因子,可激活Rho家族GTP酶(如Rac1、Cdc42),促进细胞形态改变和迁移,在转移性乳腺癌中过表达,但在DCIS等早期乳腺癌中的表达特征及临床意义尚未明确。
现有研究的局限性主要体现在三个方面:一是DCIS样本量小,难以进行分层分析;二是缺乏针对福尔马林固定石蜡包埋(FFPE)样本的定量蛋白分析工具,传统免疫组化的半定量评估易受主观影响;三是Vav2在DCIS中的作用未被系统研究,其与DCIS侵袭潜能的关联尚属空白。
本研究的创新价值在于:首次采用自主开发的成像-based定量方法,对三种候选蛋白在DCIS中的表达进行精准量化,并结合肿瘤分子亚型(ER/PR/HER2状态)、伴发侵袭情况(无侵袭/微侵袭/宏侵袭)进行分层分析,明确了Vav2作为DCIS侵袭性标志物的独特价值——这是现有研究中未涉及的关键内容。
3. 研究思路总结与详细解析
本研究的整体框架为:目标(筛选DCIS进展标志物)→核心问题(三种蛋白表达与DCIS侵袭的关联)→技术路线(样本分层→免疫组化定量→统计关联→标志物验证)。以下按关键实验环节分步骤解析:
3.1 样本收集与分层
实验目的:建立涵盖正常乳腺组织、不同分子亚型DCIS、伴/不伴侵袭DCIS及IBC的样本队列,为后续蛋白表达分析提供基础。
方法细节:收集211例FFPE样本,包括42例组织学正常的乳腺上皮、71例原位癌(CIS,其中35例无侵袭DCIS、11例伴微侵袭DCIS(<0.1cm)、25例伴宏侵袭DCIS(>0.1cm))、98例IBC;按ER、PR、HER2状态将样本分层为ER阳性(ER+/PR+/-/HER2-)、HER2阳性(ER+/-/PR+/-/HER2+)、三阴性(ER-/PR-/HER2-)三个亚型;样本均经病理学家验证,确保诊断准确性。
结果解读:队列覆盖了DCIS的主要分子亚型及侵袭状态,其中ER阳性DCIS占59%(与临床DCIS人群分布一致),伴微侵袭DCIS占15.5%(符合临床DCIS进展为微侵袭的比例),为后续分析提供了代表性样本。
实验所用关键产品:文献未提及具体样本处理试剂,领域常规使用福尔马林固定、石蜡包埋试剂(如Sigma-Aldrich的福尔马林溶液)。
3.2 免疫组化与定量蛋白分析
实验目的:检测IGF-IR、Rap1、Vav2在样本中的表达,并通过定量方法减少主观误差。
方法细节:对FFPE样本进行免疫组化染色:脱蜡、水化后,用10mM柠檬酸钠缓冲液(pH6.0)热修复抗原;3%H₂O₂淬灭内源性过氧化物酶,5%山羊血清封闭非特异性结合;加入Santa Cruz Biotechnology的兔多克隆抗体(IGF-IR β(C-20)、Rap1(121)、Vav2(H-200)),4℃孵育过夜;生物素化山羊抗兔二抗结合后,用Vector Labs的VECTASTAIN Elite ABC试剂盒和VECTOR VIP底物显色(显色时间优化为4分钟,避免底物饱和)。定量分析采用自主开发的成像-based单标记(IBU)方法:通过数字组织分割确定感兴趣区域,计算“细胞区域平均像素强度/ stroma区域平均像素强度”的比值(相对像素强度),每个样本重复测量5-26次以确保可靠性。
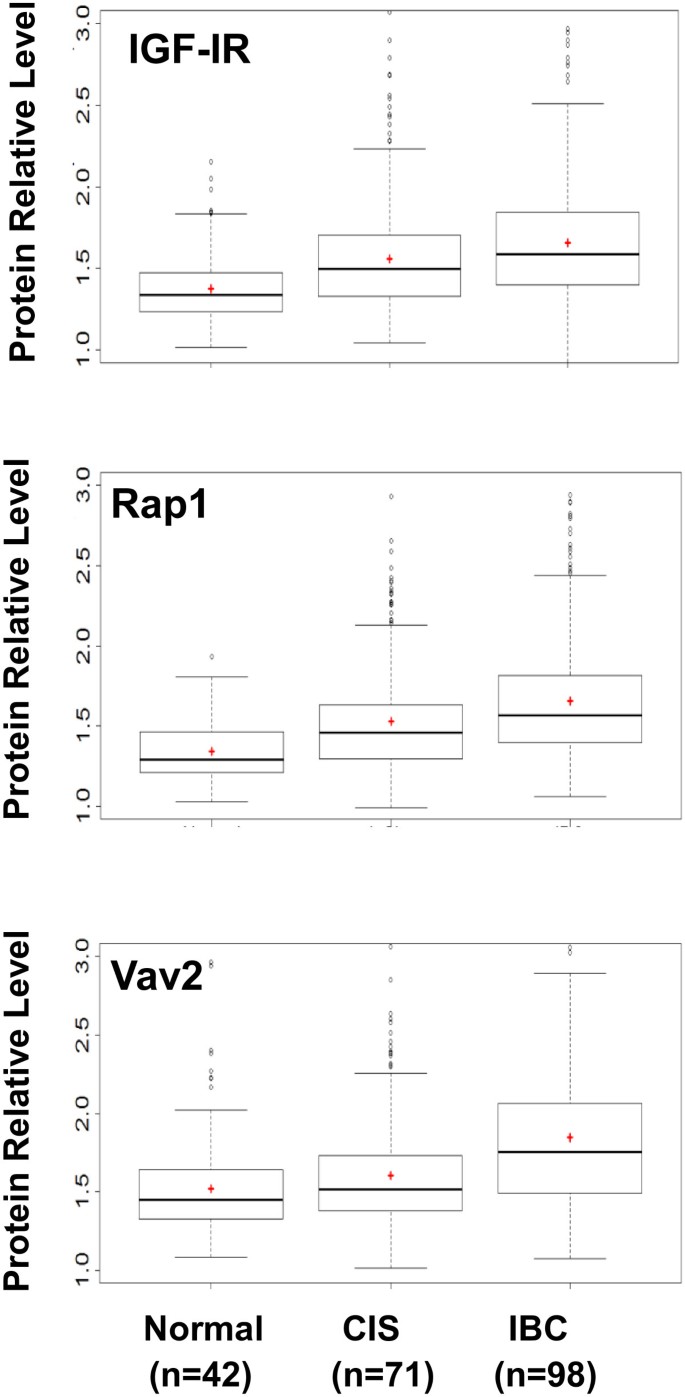
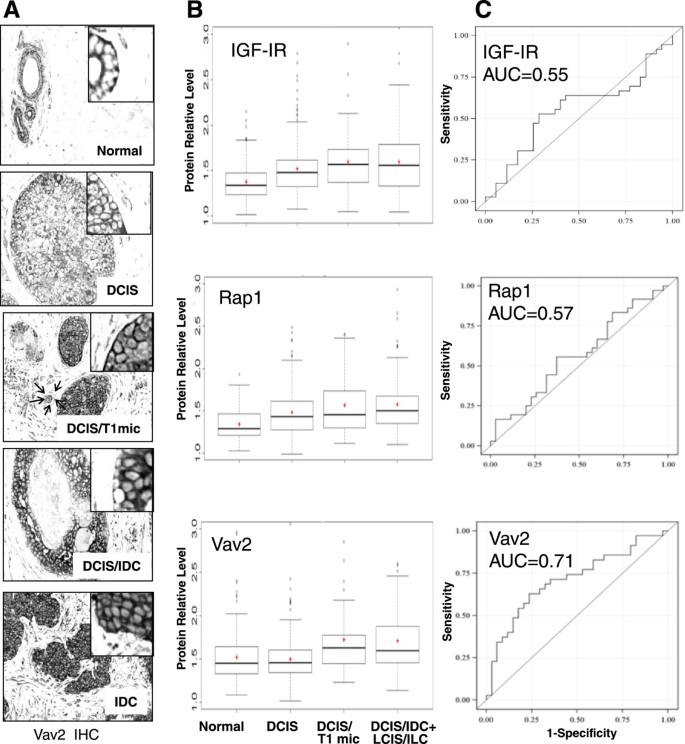
结果解读:免疫组化结果显示,Vav2在正常乳腺上皮和无侵袭DCIS中主要定位于细胞膜;在伴侵袭DCIS和IBC中,Vav2表达扩展至细胞质(图3A)。定量分析发现:IGF-IR和Rap1在ER阳性DCIS中的表达显著高于正常组织(P<0.0001);Vav2在无侵袭DCIS中的表达与正常组织无差异(P=0.99),但在伴微侵袭/宏侵袭DCIS中显著升高(P=0.03)(图1、图3B)。
实验所用关键产品:免疫组化抗体为Santa Cruz Biotechnology的兔多克隆抗体(IGF-IR β(C-20)、Rap1(121)、Vav2(H-200));显色试剂盒为Vector Labs的VECTASTAIN Elite ABC和VECTOR VIP底物试剂盒。
3.3 统计分析与关联研究
实验目的:分析候选蛋白表达与肿瘤分子亚型、侵袭潜能的关联,验证其作为生物标志物的价值。
方法细节:采用单因素ANOVA比较不同组织组(正常/DCIS/IBC)的蛋白表达;Tukey检验校正多重比较;混合效应模型分析重复测量数据( account for样本内重复测量的相关性);Pearson相关分析蛋白表达与临床变量(年龄、肿瘤大小)的关联;Logistic回归分析蛋白表达与ER/PR/HER2状态的关联;ROC曲线评估标志物预测DCIS伴侵袭的能力。
结果解读:统计分析得出三个关键结论:①分子亚型关联:IGF-IR和Rap1与ER/PR阳性显著相关(Rap1的ER阳性OR为1.56,P=0.02),但与HER2状态无关;Vav2与ER/PR/HER2状态均无关联(表3)。②侵袭潜能关联:Vav2在伴侵袭DCIS中的表达显著高于无侵袭DCIS(P=0.03),且高Vav2表达的DCIS进展为侵袭性癌的 odds ratio为2.42(95%CI 1.26-4.65,P=0.008)(图3B)。③预测价值:ROC曲线显示,Vav2预测DCIS伴侵袭的曲线下面积(AUC)为0.71(95%CI 0.59-0.84),优于IGF-IR(AUC=0.58)和Rap1(AUC=0.56)(图3C)。
4. Biomarker研究及发现成果解析
Biomarker定位:本研究涉及的候选Biomarker为IGF-IR、Rap1、Vav2三种蛋白,筛选逻辑基于三者在乳腺癌侵袭中的预临床功能研究(如IGF-IR驱动增殖、Vav2促进迁移);验证逻辑为“文献/功能筛选→组织样本免疫组化定量→分子亚型/侵袭状态分层分析→统计关联验证→ROC曲线评估预测价值”的完整链条。
研究过程详述:Biomarker的来源为FFPE的正常乳腺上皮、DCIS、IBC样本;验证方法采用免疫组化(IHC)结合成像-based定量分析(相对像素强度),避免了传统IHC的主观偏差;特异性与敏感性方面,Vav2预测DCIS伴侵袭的AUC为0.71(95%CI 0.59-0.84),提示其具有中等预测能力(文献未明确提供敏感性和特异性的具体数值)。
核心成果提炼:
1. Vav2:DCIS侵袭性的新型预测标志物:Vav2在无侵袭DCIS中的表达与正常组织无差异(P=0.99),但在伴微侵袭/宏侵袭DCIS中显著升高(P=0.03);高Vav2表达的DCIS患者进展为侵袭性癌的风险是低表达患者的2.42倍(95%CI 1.26-4.65,P=0.008)。这是首次在DCIS中发现Vav2表达与侵袭潜能的关联,提示Vav2可作为DCIS进展风险的早期标志物。
2. IGF-IR:ER阳性DCIS的治疗反应标志物:IGF-IR在ER阳性DCIS中的表达显著高于正常组织(P<0.0001),且与PR阳性显著相关(P=0.003)。结合现有研究中IGF-IR与他莫昔芬耐药的关联,推测IGF-IR可用于预测ER阳性DCIS患者对内分泌治疗的反应。
3. Rap1:ER阳性乳腺癌的关联标志物:Rap1与ER/PR阳性显著相关(ER阳性OR=1.56,P=0.02;PR阳性OR=1.63,P=0.01),但与DCIS的侵袭潜能无显著关联,提示其可能参与ER阳性乳腺癌的早期发生,但非侵袭性的驱动因子。
综上,本研究明确了Vav2作为DCIS侵袭性标志物的临床价值,为DCIS的风险分层提供了新型分子依据;同时,IGF-IR的表达特征为ER阳性DCIS的个性化治疗提供了参考方向。
