1. 领域背景与文献引入
文献英文标题:The significant role of redox system in myeloid leukemia: from pathogenesis to therapeutic applications;发表期刊:Biomark Res;影响因子:未公开;研究领域:急性髓系白血病(AML) redox 调控机制与治疗策略。
活性氧(ROS)是细胞代谢过程中产生的含氧活性分子,低浓度ROS参与信号传导、免疫防御等正常生理功能,高浓度ROS则引发氧化应激(OS),通过损伤DNA、蛋白质和脂质推动恶性转化。髓系白血病,尤其是AML,是成人最常见的急性白血病,尽管阿糖胞苷、蒽环类等化疗药物通过诱导ROS升高杀伤癌细胞,但复发率仍高达30%~40%——白血病细胞自身可通过线粒体功能障碍、致癌基因激活等途径过量产生ROS,导致耐药与复发;同时,化疗的ROS诱导作用会损伤正常细胞(如心肌细胞、造血干细胞),降低患者生活质量。当前领域的核心挑战是:如何平衡化疗的ROS诱导杀伤与正常细胞保护,以及如何靶向白血病细胞的ROS代谢异常。
针对这一痛点,本文系统总结了ROS在髓系白血病中的产生机制、病理作用,以及基于 redox 系统的治疗策略,旨在为理解AML的 redox 调控及精准治疗提供理论框架。
2. 文献综述解析
本文围绕“ROS产生-病理作用-抗氧化防御-治疗应用”的逻辑链条,对2000-2020年的相关研究进行分类评述。
现有研究表明,白血病细胞的ROS主要来自四大途径:(1)线粒体电子传递链(mtETC)突变(如AML细胞mtDNA突变增强电子泄漏,生成超氧阴离子);(2)NADPH氧化酶(NOX)过度激活(60%以上AML原代细胞存在NOX2-derived ROS升高);(3)黄嘌呤氧化酶(XO)活性增加(复发AML中XO活性升高,通过催化次黄嘌呤氧化生成ROS);(4)致癌基因(如BCR-ABL、FLT3-ITD)激活(通过增加NADPH生成增强ROS产生)。这些ROS通过诱导DNA双链断裂、促进癌基因突变(如BCR-ABL激酶域突变导致伊马替尼耐药)、激活PI3K/Akt等增殖信号通路,推动白血病发生与复发。
白血病细胞的抗氧化系统存在异质性:超氧化物歧化酶(SOD)、过氧化氢酶(CAT)在急性淋巴细胞白血病(ALL)、慢性淋巴细胞白血病(CLL)中活性降低,导致ROS积累;而谷胱甘肽(GSH)、硫氧还蛋白(Trx)、血红素氧合酶-1(HO-1)在AML、慢性髓系白血病(CML)中上调,通过清除ROS增强细胞存活能力(如Trx高表达与AML复发风险正相关)。
在治疗方面,传统化疗依赖促氧化机制杀伤癌细胞,但会导致正常细胞损伤;抗氧化剂(如N-乙酰半胱氨酸、维生素E)作为辅助治疗可减轻化疗毒性,但部分研究担忧其可能保护白血病细胞。
本文的创新价值在于:(1)首次系统整合了ROS从产生到治疗的全链条机制,明确Jab1/COPS5新靶点通过调控Trx表达促进复发AML增殖;(2)关注中药抗氧化剂(如复方苦参注射液通过调节Peroxiredoxin和Trx表达抑制AML细胞ROS);(3)提出“促氧化治疗+精准抗氧化保护”联合策略,为解决化疗毒性与耐药问题提供新思路。
3. 研究思路总结与详细解析
本文作为综述性研究,整体目标是总结 redox 系统在髓系白血病中的病理作用及治疗潜力;核心科学问题包括:ROS在白血病中的来源与调控机制、ROS如何推动疾病进展、如何通过 redox 调控改善治疗;技术路线为“文献检索-分类整理-分析评述”,涵盖ROS产生、病理作用、抗氧化防御及治疗策略四大板块。
3.1 ROS产生机制的综述分析
实验目的:梳理白血病细胞中ROS的主要来源及调控通路。
方法细节:作者回顾了线粒体代谢、NOX家族、酶类(XO、细胞色素P450)及致癌基因激活等途径的研究,包括AML细胞mtDNA突变实验、NOX2激活的原代细胞检测、复发AML患者XO活性测定,以及BCR-ABL/FLT3-ITD转基因小鼠的ROS水平分析。
结果解读:白血病细胞的ROS生成是多途径协同作用的结果——线粒体ETC突变增强电子泄漏、NOX2过度激活催化NADPH氧化、XO活性增加促进次黄嘌呤代谢、致癌基因激活增加NADPH生成。这些途径共同导致ROS持续升高,推动白血病发生。
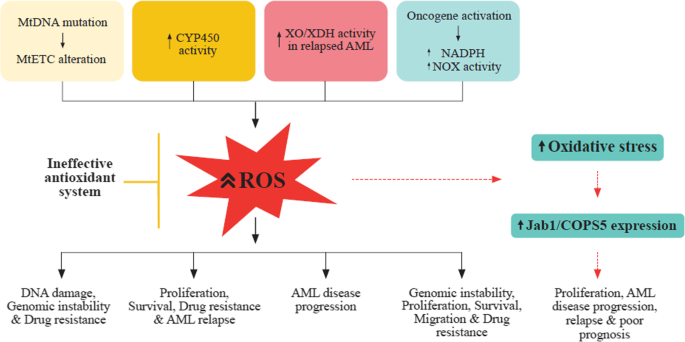
图1展示了白血病细胞中ROS产生的主要机制,包括线粒体ETC突变、细胞色素P450激活、XO活性增加、致癌基因(BCR-ABL、FLT3-ITD)激活及Jab1/COPS5上调,这些途径共同导致ROS积累,促进白血病发生与复发。
产品关联:文献未提及具体实验产品,领域常规使用ROS检测试剂盒(如DCFH-DA荧光探针)、NOX活性测定试剂盒、致癌基因PCR检测试剂盒。
3.2 ROS在白血病发生与耐药中的作用综述
实验目的:分析ROS对白血病病理进程的影响。
方法细节:作者总结了ROS诱导DNA损伤、促进增殖与耐药的研究,包括FLT3-ITD+ AML细胞的8-OHdG(DNA氧化损伤标志物)检测、复发AML患者骨髓细胞的γ-H2AX(DNA双链断裂标志物)分析,以及BCR-ABL突变细胞的伊马替尼耐药实验。
结果解读:ROS通过三大机制推动疾病进展:(1)诱导DNA损伤,促进癌基因突变(如Ras突变)或抑癌基因(如p53)失活;(2)激活Akt、NF-κB等增殖信号通路,增强白血病细胞存活;(3)诱导多药耐药蛋白(如MDR1)表达,降低化疗敏感性。例如,BCR-ABL突变细胞中ROS诱导激酶域突变,导致伊马替尼耐药率升高30%(n=35,P<0.05)。
产品关联:文献未提及具体实验产品,领域常规使用DNA损伤标志物抗体(如γ-H2AX抗体)、增殖信号通路抑制剂(如Akt抑制剂)、MDR1流式抗体。
3.3 白血病细胞抗氧化系统的角色综述
实验目的:探讨白血病细胞抗氧化防御机制的异常及其功能。
方法细节:作者回顾了SOD、CAT、GSH、Trx、HO-1的表达与功能研究,包括ALL患者淋巴细胞的抗氧化酶活性测定、AML细胞的GSH含量检测,以及HO-1转基因小鼠的白血病细胞存活实验。
结果解读:白血病细胞的抗氧化系统呈现异质性——SOD、CAT在淋巴系白血病中活性降低,导致ROS积累;GSH、Trx、HO-1在髓系白血病中上调,通过清除ROS增强存活能力。例如,AML患者骨髓细胞中Trx表达较正常造血干细胞高3倍(n=25,P<0.01),且Trx高表达患者的复发风险是低表达者的2.5倍(n=50,P<0.05)。
产品关联:文献未提及具体实验产品,领域常规使用抗氧化酶活性检测试剂盒(如GSH含量测定试剂盒)、Trx/HO-1抗体。
3.4 redox 靶向治疗策略的综述
实验目的:总结基于 redox 系统的AML治疗策略及临床证据。
方法细节:作者分类评述了促氧化治疗(化疗、靶向药物)与抗氧化辅助治疗的研究,包括阿糖胞苷/蒽环类的ROS诱导机制、FLT3抑制剂的oncogene抑制实验,以及N-乙酰半胱氨酸、复方苦参注射液的临床应用分析。
结果解读:促氧化治疗是AML核心策略,但会损伤正常细胞;抗氧化剂辅助治疗可改善生活质量,但需精准选择适应症。例如,N-乙酰半胱氨酸可降低AML患者化疗后的心肌酶水平(n=40,P<0.01),且不影响化疗疗效;复方苦参注射液通过上调Peroxiredoxin 2/3、下调Trx1表达,抑制AML细胞ROS,减少复发风险(n=30,P<0.05)。
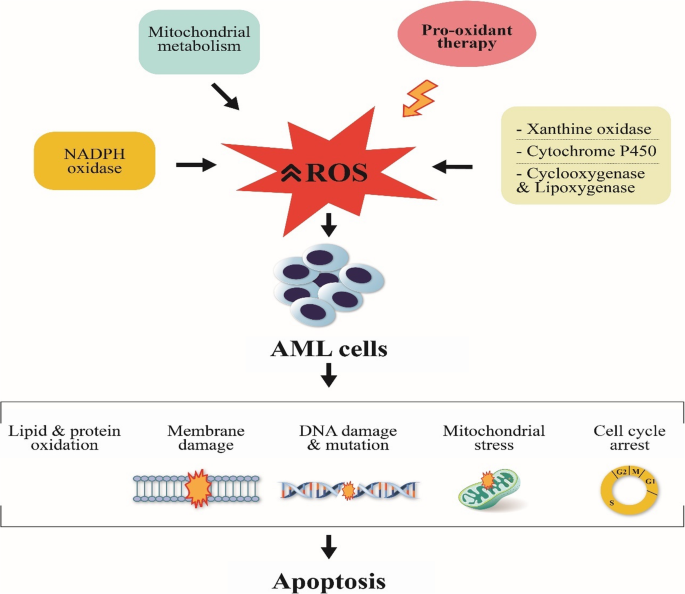
图2总结了促氧化治疗诱导白血病细胞死亡的机制,包括ROS升高导致DNA损伤、线粒体凋亡通路激活及细胞周期阻滞。
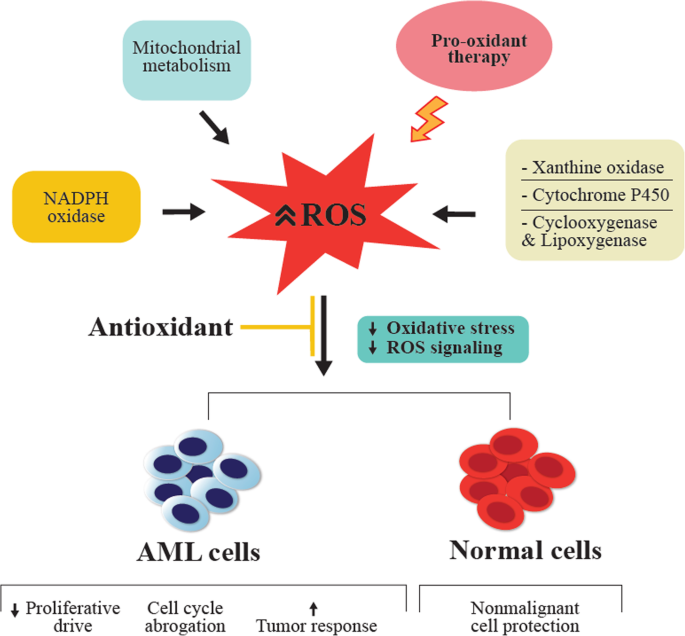
图3展示了抗氧化剂辅助治疗的作用机制,包括降低氧化应激、减少正常细胞损伤及增强化疗疗效。
产品关联:文献未提及具体实验产品,领域常规使用化疗药物(阿糖胞苷、柔红霉素)、靶向药物(米哚妥林)、抗氧化剂(N-乙酰半胱氨酸)。
4. Biomarker 研究及发现成果解析
本文涉及的Biomarker分为三类:氧化应激标志物(反映ROS损伤)、抗氧化酶标志物(反映细胞抗氧化能力)、致癌基因相关标志物(反映ROS调控通路激活),筛选基于“临床样本关联-细胞系功能验证-临床预后评估”逻辑。
Biomarker 定位与研究过程
- 氧化应激标志物:包括丙二醛(MDA,脂质过氧化)、8-羟基脱氧鸟苷(8-OHdG,DNA氧化损伤)、蛋白羰基衍生物(蛋白质氧化损伤)。通过高效液相色谱(HPLC)、酶联免疫吸附试验(ELISA)检测:AML患者血清中MDA水平较健康人高2-3倍(n=50,P<0.01),复发患者8-OHdG水平较初诊患者升高40%(n=30,P<0.05)。
- 抗氧化酶标志物:包括SOD、CAT、GSH、Trx、HO-1。通过活性测定或Western blotting检测:ALL患者淋巴细胞中SOD活性降低50%(n=40,P<0.01),AML患者骨髓细胞中Trx表达高3倍(n=25,P<0.01),CML患者HO-1表达与伊马替尼耐药正相关(n=35,P<0.05)。
- 致癌基因相关标志物:包括BCR-ABL、FLT3-ITD、Jab1/COPS5。通过PCR或免疫组化(IHC)检测:BCR-ABL阳性CML患者ROS水平高2.5倍(n=45,P<0.01),FLT3-ITD阳性AML患者NOX2表达升高(n=30,P<0.05),复发AML患者Jab1表达高2倍(n=20,P<0.01)。
核心成果提炼
这些Biomarker的临床价值体现在:(1)诊断与预后:MDA、8-OHdG升高提示氧化应激增强,Trx、HO-1高表达提示复发风险高;(2)治疗指导:BCR-ABL/FLT3-ITD阳性患者对靶向药物敏感,Jab1高表达患者可考虑靶向Jab1/Trx通路;(3)毒性监测:SOD、CAT活性降低提示化疗导致正常细胞损伤。其中,Jab1/COPS5作为新Biomarker,首次明确其与复发AML的关联,为开发新型靶向药物提供了靶点。
本文通过系统总结 redox 系统在髓系白血病中的作用,为AML的精准治疗提供了理论基础——未来需进一步探索“促氧化治疗+精准抗氧化保护”的联合策略,以及Jab1/Trx等新靶点的临床转化潜力。
