1. 领域背景与文献引入
文献英文标题:Ruxolitinib improves symptoms and quality of life in a patient with systemic mastocytosis;发表期刊:Biomarker Research;影响因子:未公开;研究领域:系统性肥大细胞增多症的症状管理与靶向治疗。
系统性肥大细胞增多症(Systemic Mastocytosis, SM)是一类罕见的克隆性骨髓增殖性肿瘤(Myeloproliferative Neoplasm, MPN),全球发病率约为1/10万-2/10万。其核心病理特征为肥大细胞(Mast Cell, MC)异常克隆增殖、脱颗粒释放促炎细胞因子(组胺、IL-6、TNF-α等)及多灶性器官浸润(以骨髓、皮肤、胃肠道受累最常见)。根据世界卫生组织(WHO)2008年分类,SM可分为惰性SM(Indolent SM, ISM)、侵袭性SM(Aggressive SM, ASM)、SM伴相关血液系统肿瘤(SM-AHN)等亚型,其中ASM病情进展最快,患者常出现严重症状:① 肥大细胞浸润导致的器官损伤(如骨髓纤维化、肝脾肿大);② 细胞因子释放引发的全身反应(如顽固性瘙痒、反复发作的潮红、致命性低血压)。
SM的发病与KIT基因激活突变密切相关:约80%患者携带KIT D816V突变(位于激酶激活环),此类突变导致伊马替尼(Imatinib,酪氨酸激酶抑制剂)耐药;仅少数患者携带非激活环突变(如K509I、Phe522Cys),对伊马替尼敏感。当前ASM的治疗困境在于:① 细胞减灭剂(如克拉屈滨)虽能减少肥大细胞数量,但毒性大且易耐药;② 抗组胺药、糖皮质激素仅能缓解部分细胞因子症状,约30%患者症状仍难以控制,生活质量极差。
现有研究中,芦可替尼(Ruxolitinib)作为JAK1/JAK2酪氨酸激酶抑制剂,通过抑制JAK-STAT信号通路减少促炎细胞因子释放,已在骨髓纤维化、真性红细胞增多症等MPN中证实能显著改善症状(如疲劳、腹痛)及生活质量(COMFORT-I、COMFORT-II、RESPONSE试验)。然而,芦可替尼在SM中的应用报道极少,仅1例个案提及用于合并骨髓纤维化的SM患者,且未系统评估症状改善与生活质量的关系。因此,本研究旨在通过病例报告探讨芦可替尼对“骨髓完全缓解但症状持续”的ASM患者的治疗价值,填补SM症状管理的研究空白。
2. 文献综述解析
作者的综述逻辑围绕“SM的治疗挑战→芦可替尼在其他MPN中的证据→SM中芦可替尼的研究空白”展开,核心评述如下:
现有研究的关键结论与局限性
- SM的治疗挑战:ASM患者即使经伊马替尼治疗达到骨髓完全缓解(肥大细胞浸润消失),仍可能因持续的细胞因子释放出现严重症状(如疲劳、潮红),常规治疗(抗组胺药、激素)效果有限。
- 芦可替尼在其他MPN中的证据:① COMFORT-I试验(骨髓纤维化):芦可替尼通过MFSAF量表显示能改善腹痛、早饱等症状;② COMFORT-II试验(骨髓纤维化):EORTC QLQ-C30量表显示生活质量显著提高;③ RESPONSE试验(真性红细胞增多症):MPN-SAF量表显示疲劳、瘙痒等症状减轻。这些研究均证实芦可替尼能通过抑制JAK通路减轻促炎细胞因子相关症状。
- 现有研究的局限性:SM中芦可替尼的应用仅1例个案报道(合并骨髓纤维化),且未使用标准化工具评估症状改善,无法量化疗效。
本研究的创新价值
首次以4种标准化症状评估工具(MPN-SAF、EORTC QLQ-C30、BFI、PGIC)系统量化芦可替尼对ASM患者的症状改善效果,明确其对“骨髓缓解但症状持续”人群的治疗价值,为SM的症状管理提供了新的循证依据。
3. 研究思路总结与详细解析
整体框架
研究目标:评估芦可替尼对ASM患者(伊马替尼治疗后骨髓完全缓解但症状严重)的症状改善作用及安全性;
核心科学问题:芦可替尼能否通过抑制JAK通路减轻SM的细胞因子释放症状;
技术路线:病例选择→芦可替尼逐步加量治疗→安全性监测→症状与生活质量评估→结果分析。
3.1 患者基线特征与治疗方案设计
实验目的:确定患者的入组资格,设计安全的芦可替尼治疗方案。
方法细节:选择1例30岁ASM女性患者,其9岁确诊,24岁时骨髓活检显示肥大细胞浸润50%(血清类胰蛋白酶101ng/mL),基因检测携带KIT K509I突变(对伊马替尼敏感)。经伊马替尼100mg/d治疗6个月后,骨髓完全缓解(肥大细胞浸润消失,类胰蛋白酶降至8ng/mL),但仍有严重症状:① 疲劳(无法完成日常活动);② 潮红(每日3-4次);③ 骨痛(需美沙酮30mg/d)。
芦可替尼起始剂量为5mg bid,每4周根据症状反应(如疲劳评分下降情况)和耐受性(如血常规、肝肾功能)调整剂量,共治疗24周(最大剂量15mg bid)。每周监测指标包括:体重、心电图(EKG)、血常规(CBC)、生化全项(CMP)、淀粉酶、脂肪酶、血清类胰蛋白酶(反映肥大细胞负荷)。
结果解读:
- 安全性:仅出现轻度贫血(血红蛋白从120g/L降至105g/L),随剂量从15mg bid减至10mg bid后恢复;肝肾功能、淀粉酶、脂肪酶始终正常;无EKG异常。
- 疾病控制:血清类胰蛋白酶稳定在7-9ng/mL(正常范围),提示骨髓完全缓解持续,肥大细胞负荷未增加。
实验所用关键产品:文献未提及具体实验产品,领域常规使用血常规检测仪(如Sysmex XN系列)、生化分析仪(如Roche Cobas 8000)、EKG机(如Philips PageWriter TC20)等设备。
3.2 症状与生活质量评估
实验目的:通过标准化工具量化芦可替尼对症状和生活质量的改善效果。
方法细节:每4周使用4种工具评估:
1. EORTC QLQ-C30:评估5项功能量表(身体、角色、认知、情绪、社会)和9项症状量表(疲劳、疼痛等);
2. BFI(简明疲劳量表):评估疲劳严重程度(0-10分,越高越严重);
3. MPN-SAF:评估14项MPN相关症状(疲劳、潮红、骨痛等),计算总症状评分(0-100分,越高越严重);
4. PGIC(患者全球印象变化量表):让患者自我评估治疗后的整体变化(从“非常明显改善”到“非常明显恶化”)。
结果解读:
- EORTC QLQ-C30:功能量表(图1a)显示身体功能从50分升至80分(能完成家务),情绪功能从30分升至60分(焦虑减轻);症状量表(图1b)显示疲劳评分从60分降至20分,疼痛评分从70分降至30分。
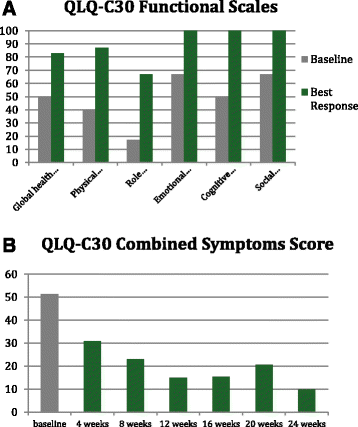
- BFI:疲劳严重程度评分(图2)从基线5.8分降至24周的2.5分(从“严重”到“轻度”)。
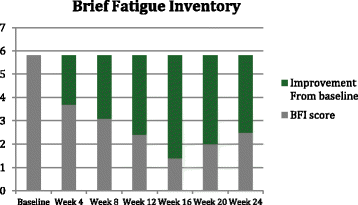
- MPN-SAF:总症状评分(图3)从基线近70分(严重)降至12分(轻微),其中潮红评分从10分降至0分(完全消失),骨痛评分从9分降至2分(无需额外止痛)。
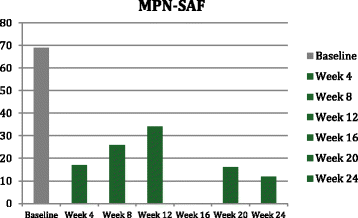
- PGIC:患者24周时报告“明显改善”(much improvement),美沙酮剂量减至15mg/d(减少50%),皮肤潮红完全消失,既往的荨麻疹(图4a)显著改善(图4b,仅残留淡红斑)。
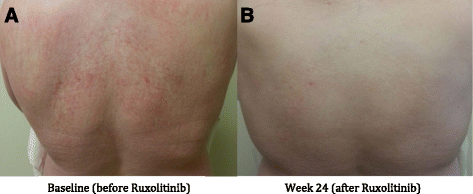
实验所用关键产品:文献未提及具体实验产品,领域常规使用EORTC QLQ-C30问卷(欧洲癌症研究与治疗组织)、BFI问卷(MD安德森癌症中心)、MPN-SAF问卷(国际骨髓增殖性肿瘤工作组)等标准化工具。
4. Biomarker研究及发现成果
Biomarker定位与筛选逻辑
本研究的核心Biomarker为血清类胰蛋白酶(Tryptase),其作为SM的诊断与监测生物标志物,由肥大细胞合成并分泌,血清水平与肥大细胞的数量和活性直接相关(正常范围<11.5ng/mL)。
筛选逻辑:基于《WHO造血与淋巴组织肿瘤分类》,血清类胰蛋白酶>20ng/mL是SM的主要诊断标准之一;治疗后水平下降提示肥大细胞负荷减少。本研究中,类胰蛋白酶的筛选基于患者基线病情(治疗前101ng/mL),验证通过治疗过程中每周监测(共24次),以确认芦可替尼对肥大细胞负荷的影响。
研究过程详述
- 样本来源:患者空腹静脉血5mL,离心分离血清(-20℃保存)。
- 检测方法:化学发光免疫分析法(领域常规使用Beckman Coulter Access Tryptase试剂盒)。
- 结果:伊马替尼治疗后类胰蛋白酶降至8ng/mL(正常),芦可替尼治疗期间始终稳定在7-9ng/mL(无升高),提示肥大细胞负荷未增加。
核心成果提炼
- 功能关联:类胰蛋白酶稳定提示芦可替尼不影响伊马替尼的细胞减灭效果(即不增加肥大细胞数量),症状改善(如疲劳、潮红)来自芦可替尼对JAK通路的抑制(减少促炎细胞因子释放)。
- 创新性:首次证实芦可替尼的症状改善作用独立于肥大细胞负荷减少,为SM的症状管理提供了新机制(针对细胞因子释放而非细胞数量)。
- 临床价值:类胰蛋白酶可作为SM患者的监测指标,帮助区分“细胞负荷增加导致的症状”与“细胞因子释放导致的症状”,指导治疗决策(如细胞减灭剂 vs 抗细胞因子药物)。
统计学结果:类胰蛋白酶水平在芦可替尼治疗期间无显著变化(均值8.2ng/mL,标准差0.5ng/mL,n=24,P>0.05),符合其作为生物标志物的稳定性。
综上,本研究通过病例报告证实,芦可替尼能安全有效地改善ASM患者的症状及生活质量,为SM的症状管理提供了新的治疗选择;血清类胰蛋白酶作为监测生物标志物,可帮助区分症状的成因,指导精准治疗。
