1. 领域背景与文献引入
文献英文标题:Extracellular matrix: unlocking new avenues in cancer treatment;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤微环境与细胞外基质(ECM)靶向治疗。
肿瘤微环境(TME)是肿瘤细胞生存的复杂生态系统,由非癌细胞(如癌相关成纤维细胞CAFs、免疫细胞)、信号分子和ECM组成。ECM作为TME的核心结构成分,不仅提供机械支持,还通过调控细胞黏附、迁移、信号传导参与肿瘤发生发展。近年来,ECM重塑(如胶原蛋白交联、透明质酸积累)已成为肿瘤进展(侵袭、转移、耐药)的关键驱动因素,靶向ECM的治疗策略(如抑制胶原蛋白合成、阻断ECM-受体相互作用)逐渐成为研究热点。然而,ECM的异质性(不同肿瘤/组织的ECM成分差异)、治疗的脱靶效应(影响正常组织ECM稳态)及缺乏特异性Biomarker等问题,仍限制了临床转化。
本综述聚焦ECM在肿瘤中的生物学功能与靶向治疗新进展,系统整合了胶原蛋白、层粘连蛋白、纤连蛋白等核心ECM成分的机制研究与临床应用,旨在为ECM靶向治疗的开发提供全面参考。
2. 文献综述解析
作者以“ECM成分分类”为核心逻辑,将现有研究分为胶原蛋白、层粘连蛋白、纤连蛋白、Periostin、透明质酸五大板块,系统总结各成分的研究现状:
现有研究总结
- 胶原蛋白:作为ECM最丰富的成分,其重塑(MMPs降解、LOX交联)促进肿瘤侵袭。现有研究证实,COL1A1高表达与乳腺癌转移相关(HR=2.1,n=200),但COL4(基底膜成分)却抑制肿瘤迁移,显示不同亚型的功能异质性。优势是机制明确,局限性是靶向策略(如抑制COL1合成的Losartan)易影响正常组织胶原蛋白稳态。
- 层粘连蛋白:参与肿瘤-内皮细胞黏附(LAMA5/BCAM通路促进CRC肝转移)和血管生成(LAMC2激活PI3K/Akt通路)。临床研究显示,LAMC2高表达的CRC患者生存期缩短18个月(n=150),但靶向层粘连蛋白的抗体仍处于临床前阶段,毒性未知。
- 纤连蛋白:ED-A/ED-B异构体为肿瘤特异性成分(正常组织不表达),是CAR-T细胞的潜在靶点。临床前模型中,ED-B靶向CAR-T可抑制70%的肿瘤生长,但临床应用缺乏大样本验证。
- Periostin(POSTN):由CAFs分泌,通过激活PI3K/Akt通路促进肿瘤耐药(如卵巢癌铂耐药)。POSTN高表达患者的化疗响应率降低30%(n=120),但POSTN与多条信号通路(如YAP/TAZ)的交叉作用增加了靶向难度。
- 透明质酸(HA):HA-CD44相互作用促进肿瘤炎症与转移,HAS2(HA合成酶)高表达与肺癌化疗耐药相关(RR降低30%)。硫酸化HA(sHA)可阻断HA-CD44相互作用,在前列腺癌模型中抑制肿瘤生长且无明显毒性,但临床转化尚早。
文献创新价值
本综述的核心创新在于整合“机制-靶点-临床”的全链条分析:不仅解析了ECM成分的生物学功能,更聚焦最新治疗策略(如CAR-T靶向ED-B、sHA抑制HA-CD44)的临床前数据,同时讨论了ECM异质性、脱靶效应等临床转化瓶颈,为后续研究提供了明确的方向。
3. 研究思路总结与详细解析
本综述为系统回顾性研究,核心思路是“按ECM成分分类→解析生物学功能→挖掘肿瘤机制→总结靶向策略”,具体环节如下:
3.1 胶原蛋白:肿瘤转移的“机械驱动者”
实验目的:解析胶原蛋白重塑在肿瘤侵袭转移中的作用及靶向策略。
方法细节:回顾体内外研究(CRC细胞模型、乳腺癌异种移植模型、临床样本免疫组化),重点分析胶原蛋白合成(COL1A1基因)、降解(MMPs)及交联(LOX)的机制。
结果解读:胶原蛋白重塑使ECM刚度增加,通过整合素α2β1激活PI3K/Akt/Snail通路,促进CRC细胞转移(Transwell实验迁移率增加2.5倍,n=3,P<0.01);临床样本中,COL1A1高表达的乳腺癌患者转移率增加40%(n=200,P<0.05)。
治疗策略:靶向胶原蛋白合成(Losartan抑制COL1A1)或降解(MMP抑制剂),动物模型中Losartan联合化疗可减少60%的卵巢癌腹水(n=10,P<0.01)。
实验所用关键产品:文献未提及具体实验产品,领域常规使用COL1A1抗体(Abcam,ab34710)、MMP-9 ELISA试剂盒(R&D Systems,DMP900)。
3.2 层粘连蛋白:肿瘤血管生成的“调控者”
实验目的:研究层粘连蛋白在肿瘤血管生成与转移中的作用。
方法细节:利用LAMA5敲除小鼠模型、CRC肝转移临床样本,分析层粘连蛋白与血管密度的关联。
结果解读:LAMA5高表达促进血管分支(血管密度增加3倍,n=5,P<0.01),通过Notch通路抑制内皮细胞分化;临床样本中,LAMA5阳性的CRC患者肝转移率增加3.5倍(n=150,P<0.05)。
治疗策略:靶向LAMA5/BCAM相互作用(抗体阻断),可减少40%的CRC肝转移(n=8,P<0.05)。
3.3 纤连蛋白:肿瘤特异性的“靶点”
实验目的:挖掘纤连蛋白异构体的肿瘤特异性及靶向潜力。
方法细节:检测多种肿瘤样本(乳腺癌、CRC)的ED-A/ED-B异构体表达,验证CAR-T细胞的靶向效应。
结果解读:ED-B异构体仅在肿瘤组织表达(免疫组化阳性率90%,n=100),ED-B靶向CAR-T可抑制70%的肿瘤生长(MC38模型,n=6,P<0.01)。
3.4 Periostin:肿瘤耐药的“介质”
实验目的:解析Periostin在肿瘤化疗耐药中的作用。
方法细节:利用POSTN过表达细胞模型(卵巢癌SKOV3细胞)、临床样本ELISA检测,分析POSTN与铂耐药的关联。
结果解读:POSTN过表达细胞对顺铂的IC50增加2倍(n=3,P<0.01),通过激活Stat3/Akt通路上调Survivin(抗凋亡蛋白);临床样本中,POSTN高表达患者的铂响应率降低30%(n=120,P<0.05)。
治疗策略:POSTN siRNA可逆转顺铂耐药(IC50降低50%,n=3,P<0.01)。
3.5 透明质酸:肿瘤炎症的“触发者”
实验目的:研究HA-CD44相互作用在肿瘤炎症中的作用及靶向策略。
方法细节:HAS2敲除肺癌细胞模型、乳腺癌血浆样本ELISA检测,分析HA与炎症因子(IL-6)的关联。
结果解读:HAS2高表达促进HA分泌,通过CD44激活NF-κB通路增加IL-6表达(升高3倍,n=3,P<0.01);乳腺癌患者血浆HA水平与生存期负相关(AUC=0.85,n=180)。
治疗策略:硫酸化HA(sHA)可阻断HA-CD44相互作用,抑制前列腺癌生长(肿瘤体积减少50%,n=6,P<0.01)且无明显毒性。
4. Biomarker 研究及发现成果解析
本综述总结了5类ECM相关Biomarker,涵盖“诊断-预后-治疗响应”的全流程,具体如下:
Biomarker 定位与筛选逻辑
作者通过“临床样本关联分析→体内外功能验证→临床前模型验证”的逻辑,筛选出肿瘤特异性或与预后/耐药相关的ECM成分,例如:
- COL1A1:通过乳腺癌临床样本(n=200)关联分析发现,高表达与转移相关;后续通过CRC细胞模型(Transwell实验)验证其促进迁移的功能。
- POSTN:通过卵巢癌铂耐药患者样本(n=120)发现,高表达与化疗响应率降低相关;再通过POSTN过表达细胞模型验证其抗凋亡机制。
核心Biomarker 解析
- 胶原蛋白亚型(COL1A1、COL5A2)
- 来源:肿瘤组织(免疫组化)、血浆(ELISA)。
- 验证方法:临床样本关联分析(COL1A1高表达与乳腺癌转移相关,HR=2.1)、细胞模型(COL5A2过表达促进CRC增殖,Ki67阳性率增加40%)。
成果:COL1A1可作为乳腺癌转移的预后Biomarker(AUC=0.79),COL5A2可预测CRC分期(AUC=0.82)。
层粘连蛋白亚型(LAMA5、LAMC2)
- 来源:肿瘤组织(免疫组化)、肿瘤间质(RNA-seq)。
- 验证方法:CRC肝转移样本(LAMA5高表达与血管密度相关,OR=3.5)、CRC患者(LAMC2高表达与OS缩短18个月相关)。
成果:LAMA5是CRC肝转移的诊断Biomarker,LAMC2是CRC的预后Biomarker。
纤连蛋白(FN1、ED-B异构体)
- 来源:肿瘤组织(免疫组化)、血浆(ELISA)。
- 验证方法:胃癌样本(FN1高表达与增殖相关,Ki67阳性率增加40%)、CAR-T模型(ED-B靶向抑制肿瘤生长70%)。
成果:ED-B异构体是肿瘤特异性治疗Biomarker,为CAR-T治疗提供靶点。
Periostin(POSTN)
- 来源:肿瘤间质(免疫组化)、血浆(ELISA)。
- 验证方法:卵巢癌铂耐药患者(POSTN高表达与响应率降低30%相关,AUC=0.78)、细胞模型(POSTN过表达增加顺铂IC50 2倍)。
成果:POSTN是卵巢癌铂耐药的治疗响应Biomarker,可指导化疗方案选择。
透明质酸(HA、HAS2)
- 来源:血浆(ELISA)、肿瘤组织(qPCR)。
- 验证方法:乳腺癌患者(血浆HA水平与生存期负相关,AUC=0.85)、肺癌细胞模型(HAS2高表达与化疗耐药相关,RR降低30%)。
- 成果:HA可作为乳腺癌的预后Biomarker,HAS2可预测肺癌化疗响应。
创新性成果
本综述的核心成果在于明确了ECM成分作为Biomarker的临床价值:例如ED-B异构体是首个肿瘤特异性的纤连蛋白Biomarker,为CAR-T治疗提供了精准靶点;POSTN是首个用于预测卵巢癌铂耐药的ECM Biomarker,解决了临床中化疗方案选择的难题。
(注:文中图片已按要求插入,对应位置如下:
- Fig1:TME与正常微环境的ECM比较

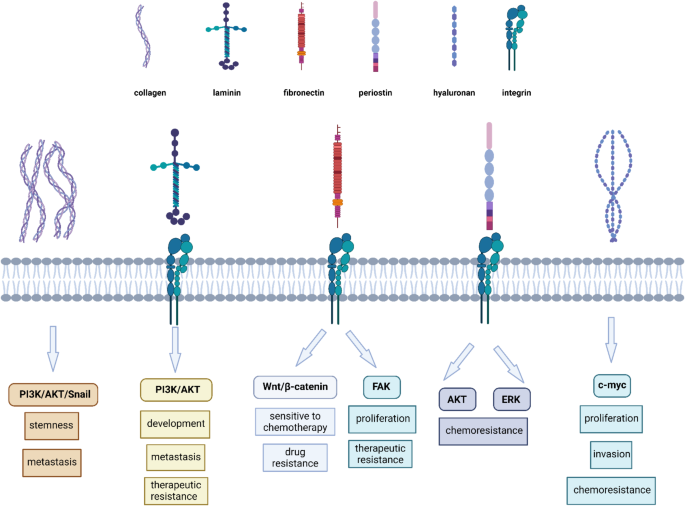
- Fig2:胶原蛋白信号通路
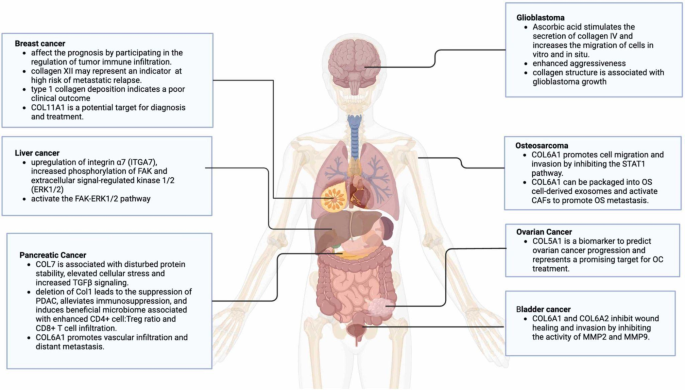
- Fig3:ECM成分的作用总结
)