1. 领域背景与文献引入
文献英文标题:The clinical and genomic distinctions of Class1/2/3 BRAF-mutant colorectal cancer and differential prognoses;发表期刊:Biomarker Research;影响因子:未公开;研究领域:结直肠癌精准医学/分子分型。
结直肠癌(CRC)是全球发病率第三、死亡率第二的恶性肿瘤,BRAF基因是其重要致癌驱动基因。BRAF突变根据功能可分为三类:1类为V600位点突变(如V600E),编码RAS非依赖的活性单体,是最常见的突变类型(约占BRAF突变的70%-80%);2类为非V600突变(如G469),编码RAS非依赖的活性二聚体;3类为非V600突变(如D594),编码RAS依赖的激酶活性受损蛋白。当前研究热点集中于不同BRAF亚型的分子特征与治疗策略——1类患者对BRAF抑制剂(如恩考芬尼)敏感,但2/3类患者因突变类型特殊,现有BRAF抑制剂无法有效靶向,且其基因组特征、预后差异尚未明确,成为领域未解决的核心问题。
在此背景下,本文回顾性分析328例初治BRAF突变CRC患者的肿瘤突变谱,旨在探究1/2/3类BRAF突变的临床特征、基因组学差异及预后关联,为不同亚型患者的精准治疗提供依据。
2. 文献综述解析
文献综述以“BRAF突变功能分类”为核心逻辑,系统评述现有研究:
首先,作者总结各亚型分子机制:1类突变通过构象改变激活BRAF单体,不依赖RAS;2类通过二聚体维持活性,同样不依赖RAS;3类则需依赖RAS才能激活下游通路。其次,现有研究证实1类患者对BRAF抑制剂敏感,但2/3类患者无法获益,且针对2/3类的治疗(如二代BRAF抑制剂、联合EGFR抑制剂)仍在探索中。
然而,现有研究存在局限性:一是2/3类样本量小,基因组特征分析不充分;二是预后差异未明确。本文创新在于首次以大样本队列分析1/2/3类BRAF突变的基因组特征,并通过外部数据集验证预后,填补了2/3类研究空白,为精准治疗提供关键依据。
3. 研究思路总结与详细解析
3.1 患者队列与样本收集
本环节核心目标是建立完整的BRAF突变CRC队列。研究纳入328例初治CRC患者,肿瘤样本通过捕获型二代测序(NGS)检测400+癌症相关基因,明确BRAF突变类型。结果显示:1类246例(75%,均为V600E)、2类29例(9%,主要为G469)、3类53例(16%,主要为D594)。临床特征方面,三类患者年龄、性别、分期无差异,但肿瘤位置存在差异(1类 vs 3类,P=0.027)。
实验所用关键产品:文献未提及具体实验产品,领域常规使用捕获型NGS试剂盒(如Agilent SureSelect Human Cancer Panel)。
3.2 基因组特征分析
本环节目标是比较1/2/3类BRAF突变的基因组差异。研究通过分析基因突频率、通路改变、RAS激活突变等位频率(AF)、突变特征(COSMIC数据库)、TMB(肿瘤突变负荷)及MSI(微卫星不稳定),得出以下结论:
- 基因突频率:1类RNF43突变频率更高(vs 2/3类,P<0.05);2/3类KRAS/NRAS/APC突变更常见(P<0.05);2类PI3K通路(PTEN、AKT3)突变更多(P<0.05)。
- 通路改变:1类Wnt/RTK/RAS通路改变更少(vs 2/3类,P<0.05)。
- RAS激活突变:3类RAS激活突变比例(43%)显著高于1类(7%,P<0.001),且BRAF等位频率低于RAS(提示BRAF为亚克隆)。
- 突变特征:1类APOBEC(Signature 2/13)和NER(Signature 22)突变特征更显著(P<0.05)。
- TMB与MSI:1类TMB高于野生型(median 7.6 vs 5.8,P<0.05);MSI-H比例(11%)高于野生型(5%,P<0.001)。
本环节对应图1(BRAF突变位置、基因突频率、通路改变等),图片链接:
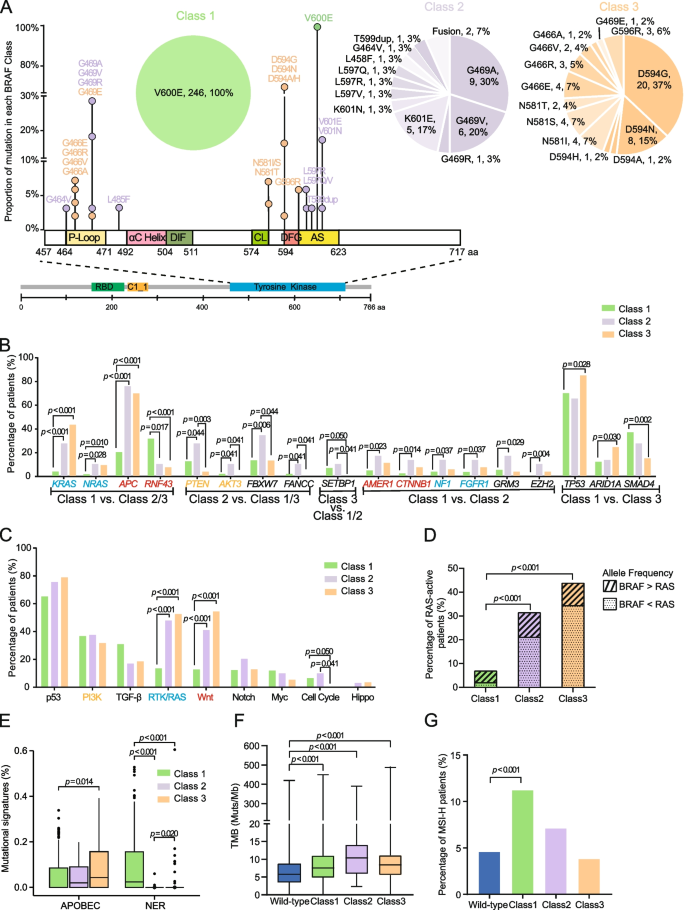
。
3.3 预后分析(外部数据集)
因本队列缺乏生存数据,作者利用cBioPortal外部数据集(455例不可切除转移性CRC)分析预后。结果显示:
- 3类患者预后最佳(中位PFS 7.3个月、OS 31.9个月);1类最差(中位PFS 5.0个月、OS 12.7个月,P<0.05)。
- 外部数据集验证了本队列的基因组特征:1类无RAS激活突变(vs 3类50%,P<0.001);1类MSI-H比例(24%)高于2/3类(P<0.05)。
本环节对应图2(RAS激活突变、MSI-H比例、PFS/OS曲线),图片链接:
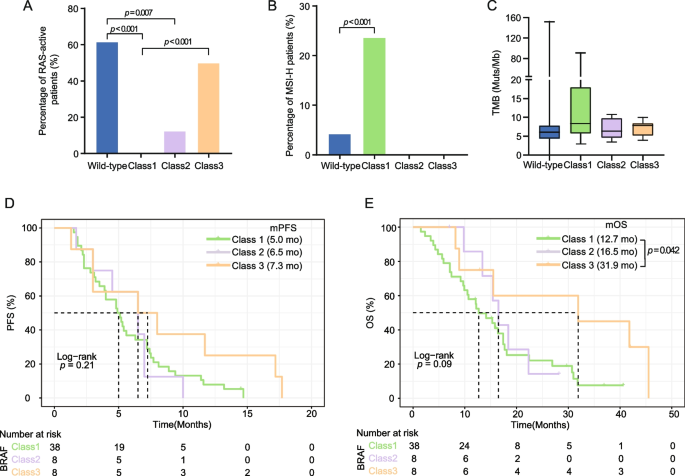
。
4. Biomarker研究及发现成果解析
Biomarker定位与验证逻辑
本文核心Biomarker是BRAF突变功能亚型(1/2/3类),筛选与验证遵循“功能分类→队列验证→外部数据集验证”链条:
1. 功能分类:基于BRAF是否依赖RAS、激酶活性,分为1/2/3类;
2. 队列验证:在328例队列中验证各亚型的突变频率与基因组特征;
3. 外部验证:通过cBioPortal验证预后关联。
研究过程与成果
- Biomarker来源:初治CRC患者肿瘤组织,通过捕获型NGS检测并分类。
- 验证方法:基因组特征分析(基因突频率、通路、TMB、MSI)与预后分析(外部数据集)。
- 核心成果:
- 1类BRAF突变:是不良预后Biomarker(中位OS 12.7个月,P<0.05),与RNF43突变、MSI-H、高TMB显著相关(P<0.05);
- 3类BRAF突变:是良好预后Biomarker(中位OS 31.9个月,P<0.05),与RAS激活突变显著相关(43%,P<0.001),为联合EGFR抑制剂治疗提供依据;
- 创新性:首次明确2/3类BRAF突变的基因组特征与预后差异,为BRAF亚型作为CRC预后/治疗Biomarker提供证据。
本文通过系统分析1/2/3类BRAF突变的临床与基因组差异,为不同亚型患者的精准治疗(如1类用BRAF抑制剂、3类联合EGFR抑制剂)提供了重要依据,推动了BRAF突变CRC的精准医学进展。
