1. 领域背景与文献引入
文献英文标题:Development of a fully automated chemiluminescence immunoassay for urine monomeric laminin-γ2 as a promising diagnostic tool of non-muscle invasive bladder cancer;发表期刊:Biomarker Research;影响因子:未明确;研究领域:膀胱癌诊断生物标志物研究。
膀胱癌是发达国家(如日本)发病率快速上升的恶性肿瘤,主要归因于人口老龄化。早期诊断与治疗是实现膀胱癌治愈和病情控制的关键,但当前诊断体系存在明显缺陷:尿细胞学检查虽能准确诊断高级别肌层浸润性膀胱癌(MIBC),但对占比约70%的低级别非肌层浸润性膀胱癌(NMIBC)敏感性仅38%-61%,因NMIBC患者尿液中癌细胞释放量少。此外,已批准用于膀胱癌诊断的尿液肿瘤标志物(如核基质蛋白-22(NMP-22)、膀胱肿瘤抗原(BTA))诊断准确性不足,无法满足临床需求。因此,开发高敏感性、高特异性的NMIBC诊断生物标志物成为领域亟待解决的问题。
前期研究发现,尿液中的单体层粘连蛋白-γ2(mono-Ln-γ2)是潜在的膀胱癌生物标志物,其在膀胱癌患者尿液中水平升高。但现有检测方法(如夹心酶联免疫吸附试验(ELISA))使用的抗体无法区分mono-Ln-γ2与层粘连蛋白-332(Ln-332)的γ2链(Ln-332是正常上皮基底膜的主要成分),导致良性泌尿系统疾病患者或健康人群检测出现假阳性,限制了其临床应用。基于此,本研究旨在开发一种基于mono-Ln-γ2特异性单克隆抗体(2H2 mAb)的全自动化学发光免疫分析(CLIA)系统,提高尿液mono-Ln-γ2检测的敏感性与特异性,评估其作为NMIBC诊断工具的潜力。
2. 文献综述解析
文献综述部分以“现有诊断方法缺陷→ 潜在生物标志物的不足→ 检测技术的局限性”为核心逻辑,对领域内研究进行评述。现有研究结论显示:尿细胞学检查对NMIBC诊断敏感性低,无法满足早期筛查需求;已有的尿液肿瘤标志物(NMP-22、BTA)诊断准确性有限,未被广泛用于临床;前期基于常规单抗的夹心ELISA虽能检测到膀胱癌患者尿液中mono-Ln-γ2升高,但因抗体无法区分mono-Ln-γ2与Ln-332的γ2链,导致假阳性率较高,影响结果可靠性。现有技术的优势在于夹心ELISA可实现mono-Ln-γ2的定量检测,但其局限性也较为明显:检测下限仅200 pg/mL,敏感性不足;且受Ln-332干扰,特异性差。
本研究的创新价值在于针对现有技术的核心缺陷,首次采用mono-Ln-γ2特异性单抗(2H2 mAb)构建全自动CLIA系统:一方面,2H2 mAb仅识别mono-Ln-γ2,避免了Ln-332的干扰,提高检测特异性;另一方面,CLIA技术相比ELISA具有更高的敏感性(检测下限降至10 pg/mL)和更快的检测速度(<30分钟),更适合临床批量样本检测。通过临床样本验证,本研究旨在明确该系统对NMIBC的诊断价值,为膀胱癌早期诊断提供新的工具。
3. 研究思路总结与详细解析
本研究以“开发高特异性、高敏感性的尿液mono-Ln-γ2检测系统,并验证其作为NMIBC诊断生物标志物的潜力”为核心目标,围绕“2H2 mAb的特异性”“CLIA系统的性能”“临床样本的检测结果”“诊断准确性”四大科学问题展开,技术路线遵循“单抗验证→ 系统建立→ 样本检测→ 准确性评估”的闭环逻辑。
3.1 抗mono-Ln-γ2单抗(2H2 mAb)的特异性验证
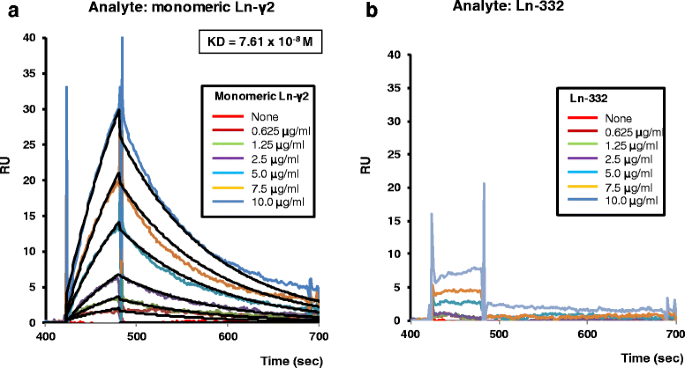
实验目的是确认2H2 mAb对mono-Ln-γ2的特异性结合能力,排除其与Ln-332的交叉反应。方法细节:采用表面等离子体共振(SPR)技术,将2H2 mAb或抗Ln-α3 mAb(用于验证Ln-332的质量)固定在CM5传感器芯片上,分别检测不同浓度(0、0.625、1.25、2.5、5.0、7.5、10.0 μg/mL)mono-Ln-γ2和Ln-332的结合信号,通过Biacore 3000系统采集数据并分析平衡解离常数(Kd)。结果解读:2H2 mAb与mono-Ln-γ2呈浓度依赖性结合,而与Ln-332无明显结合;抗Ln-α3 mAb与Ln-332呈浓度依赖性结合(验证了Ln-332的完整性),表明2H2 mAb对mono-Ln-γ2具有高度特异性。实验所用关键产品:GE Healthcare的CM5传感器芯片、Biacore 3000系统;R&D systems的抗Ln-α3 mAb。
3.2 全自动CLIA系统的建立与性能评估
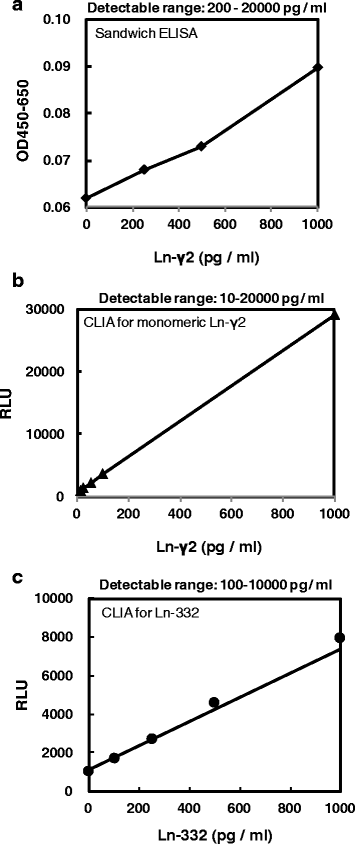
实验目的是构建基于2H2 mAb的全自动CLIA系统,并评估其检测mono-Ln-γ2的性能。方法细节:将2H2 mAb通过羧基基团固定在磁性微球上,将抗Ln-γ2结构域III(DIII)多克隆抗体用吖啶标记,采用两步夹心 assay模式,利用ARCHITECT系统(Abbott Laboratories)进行全自动检测。制备mono-Ln-γ2标准品(浓度0、10、20、50、100、1000、10000、20000 pg/mL)和Ln-332标准品(0、100、250、500、1000、10000 pg/mL),绘制标准曲线;选取3份尿液样本进行加标回收率实验(加标浓度50 pg/mL和1000 pg/mL)。结果解读:CLIA系统对mono-Ln-γ2的检测范围为10-20000 pg/mL,较之前的夹心ELISA(200-20000 pg/mL)敏感性提高约20倍;加标回收率为82.3%-96.2%,符合临床检测要求;对Ln-332的检测范围为100-10000 pg/mL,表明系统可区分mono-Ln-γ2与Ln-332。实验所用关键产品:Abbott Laboratories的ARCHITECT系统;GE Healthcare的Hi-Trap Protein G HP柱(用于单抗纯化);Thermo Fisher的pDEST15表达载体(用于DIII蛋白表达)。
3.3 临床尿液样本中mono-Ln-γ2的检测与分析
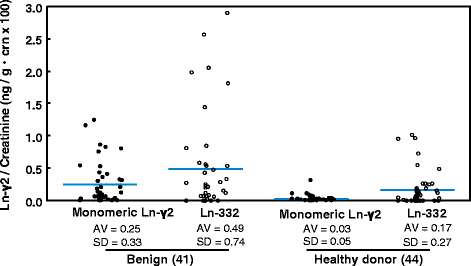
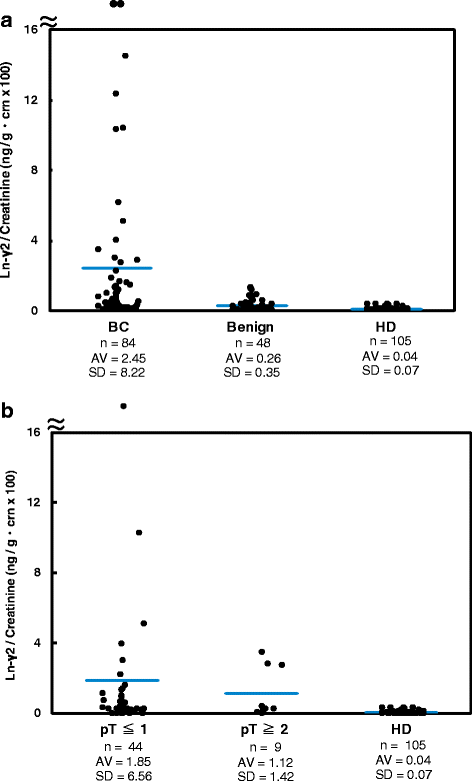
实验目的是评估CLIA系统检测临床样本中mono-Ln-γ2的能力,比较不同人群(膀胱癌患者、良性泌尿系统疾病患者、健康供体)的mono-Ln-γ2水平。方法细节:收集2008年7月至2016年11月期间的237份尿液样本,其中膀胱癌患者84例(含NMIBC 44例、MIBC 9例)、良性泌尿系统疾病患者48例(如良性前列腺增生、附睾炎、尿路结石)、健康供体105例。样本收集后离心(1000 rpm,5分钟),-80℃保存1-6个月;检测前再次离心(15000 rpm,4℃,10分钟),取250 μL上清用CLIA检测mono-Ln-γ2,结果用尿肌酐(CRE)标准化(单位:ng/g·crn×100),尿肌酐通过比色法(Determiner-L CRE系统)检测。结果解读:膀胱癌患者mono-Ln-γ2均值为2.45±8.22 ng/g·crn×100,显著高于良性疾病患者(0.26±0.35)和健康供体(0.04±0.07),差异有统计学意义(p=0.0006和p<0.0001);NMIBC患者均值为1.85±6.56 ng/g·crn×100,MIBC患者为1.12±1.42 ng/g·crn×100,均显著高于健康供体(p<0.0001);良性疾病患者的Ln-332均值(0.49±0.74 ng/g·crn×100)高于mono-Ln-γ2(0.25±0.33 ng/g·crn×100),表明Ln-332是之前夹心ELISA假阳性的主要原因。实验所用关键产品:Kyowa Medex的Determiner-L CRE系统。
3.4 诊断准确性评估(ROC曲线分析)
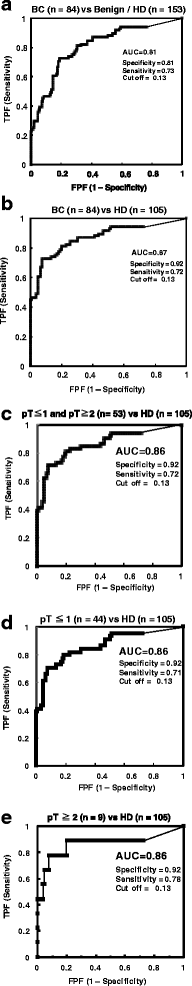
实验目的是评估mono-Ln-γ2作为膀胱癌(尤其是NMIBC)诊断生物标志物的准确性。方法细节:使用Analyse-it软件(版本3.90.5)绘制受试者工作特征(ROC)曲线,计算曲线下面积(AUC),评估诊断准确性;以健康供体均值+2倍标准差确定最佳截断值。结果解读:膀胱癌vs良性疾病+健康供体的AUC为0.81,截断值0.13 ng/g·crn×100时,特异性0.81,敏感性0.73;膀胱癌vs健康供体的AUC为0.87,特异性0.92,敏感性0.72;NMIBC vs健康供体的AUC为0.86,特异性0.92,敏感性0.71;MIBC vs健康供体的AUC为0.86,特异性0.92,敏感性0.78。上述结果表明,mono-Ln-γ2对膀胱癌(包括NMIBC)具有良好的诊断准确性。实验所用关键产品:Analyse-it软件(版本3.90.5)。
4. Biomarker研究及发现成果解析
Biomarker定位:本研究涉及的生物标志物为尿液中的单体层粘连蛋白-γ2(mono-Ln-γ2),属于蛋白质类生物标志物。其筛选/验证逻辑为:前期研究发现mono-Ln-γ2在膀胱癌患者尿液中升高→ 通过SPR技术验证2H2 mAb对mono-Ln-γ2的特异性→ 建立CLIA系统实现定量检测→ 利用临床样本(膀胱癌、良性疾病、健康供体)验证其诊断价值,形成“发现→ 验证→ 临床评估”的完整链条。
研究过程详述:Biomarker来源为临床尿液样本(膀胱癌患者、良性疾病患者、健康供体的中段尿);验证方法采用基于2H2 mAb的全自动CLIA系统,通过两步夹心 assay实现mono-Ln-γ2的定量检测,结果用尿肌酐标准化以消除尿液稀释影响;特异性与敏感性数据显示:膀胱癌vs健康供体的AUC为0.87,截断值0.13 ng/g·crn×100时,特异性0.92,敏感性0.72;NMIBC vs健康供体的AUC为0.86,特异性0.92,敏感性0.71。
核心成果提炼:① 尿液mono-Ln-γ2可作为膀胱癌(尤其是NMIBC)的潜在诊断生物标志物,其水平在膀胱癌患者中显著升高,且与良性疾病和健康人群差异有统计学意义(p<0.0001);② 基于2H2 mAb的CLIA系统可特异性检测mono-Ln-γ2,避免Ln-332干扰,检测下限降至10 pg/mL,敏感性较夹心ELISA提高20倍;③ ROC曲线分析显示,mono-Ln-γ2对NMIBC的诊断准确性良好(AUC=0.86),优于现有部分生物标志物。本研究的创新性在于首次将mono-Ln-γ2特异性单抗应用于全自动CLIA系统,解决了之前检测方法的假阳性问题,为NMIBC诊断提供了新的工具。