1. 领域背景与文献引入
文献英文标题:Serum levels of VEGF and MCSF in HER2+ / HER2- breast cancer patients with metronomic neoadjuvant chemotherapy;发表期刊:Biomarker Research;影响因子:未公开;研究领域:乳腺癌新辅助治疗与血管生成生物标志物研究
领域共识:新辅助化疗最初用于将不可切除的乳腺病灶转化为可切除病灶,目前已扩展至可手术肿瘤的降期治疗,为保乳手术创造条件。节拍式化疗作为新辅助治疗的新兴策略,以低剂量、高频次、无长间歇给药为特点,其临床获益的分子机制尚未完全明确,尤其是抗血管生成相关通路的作用仍需深入探索。当前乳腺癌新辅助治疗的研究热点集中在不同亚型患者的精准治疗方案优化,以及可预测治疗响应的生物标志物筛选,但针对HER2阳性/阴性亚型在节拍式化疗联合曲妥珠单抗治疗中,血管生成因子的动态变化及与病理缓解的关联研究仍存在空白。本文旨在通过动态监测血清血管内皮生长因子(VEGF)和巨噬细胞集落刺激因子(MCSF)的水平变化,明确血管生成通路是否参与曲妥珠单抗在新辅助治疗中的抗肿瘤作用,为乳腺癌精准治疗提供临床证据。
2. 文献综述解析
作者按新辅助化疗的发展脉络、节拍式化疗的机制与临床数据、HER2靶向治疗的抗血管生成作用三个维度梳理现有研究。现有研究显示,新辅助化疗的应用场景从不可切除病灶转化扩展至可手术肿瘤降期,节拍式化疗在乳腺癌中的临床缓解率(完全缓解+部分缓解)可达39%(范围12%~88%),临床获益率(完全缓解+部分缓解+稳定疾病>6个月)可达57%(范围24%~93%),机制上被证实可靶向肿瘤血管生成,选择性抑制活化内皮细胞的增殖、凋亡与迁移,调节血小板反应蛋白-1等血管生成相关因子。HER2靶向药物曲妥珠单抗被认为可降低肿瘤血管直径、体积及通透性,下调VEGF等促血管生成因子的mRNA表达,但曲妥珠单抗通过血管生成通路发挥抗肿瘤作用的具体机制仍不明确,且缺乏在节拍式化疗联合应用中的临床验证数据。现有研究的局限性在于,多数节拍式化疗的机制研究基于体外或动物模型,临床研究多为单臂设计,缺乏针对不同HER2亚型的血管生成因子动态变化数据,且尚未明确可预测治疗响应的特异性生物标志物。本文的创新点在于首次在HER2阳性/阴性乳腺癌患者中,动态监测节拍式新辅助化疗(联合或不联合曲妥珠单抗)过程中血清VEGF和MCSF的水平变化,并关联病理完全缓解率,为曲妥珠单抗的抗血管生成作用提供直接临床证据。
3. 研究思路总结与详细解析
本研究的整体框架为:入组HER2阳性/阴性局部晚期乳腺癌患者,给予标准化节拍式新辅助化疗(联合或不联合曲妥珠单抗),动态采集治疗过程中的血清样本,采用酶联免疫吸附试验(ELISA)检测VEGF和MCSF水平,通过统计分析明确因子变化趋势与病理缓解率的关联,最终探索血管生成通路在曲妥珠单抗抗肿瘤作用中的角色。
3.1 研究对象入组与治疗方案设计
实验目的是明确入组患者的临床特征,建立标准化的节拍式新辅助化疗联合曲妥珠单抗治疗方案。方法细节为入组经组织学确诊的浸润性导管癌患者,其中HER2阳性患者9例,HER2阴性患者11例,HER2阳性定义符合2007年美国临床肿瘤学会/美国病理学家协会(ASCO/CAP)指南;HER2阳性组接受每周紫杉醇100mg/m²共8周,随后每周多柔比星24mg/m²联合每日口服环磷酰胺100mg共9周,同时给予曲妥珠单抗负荷剂量4mg/kg,维持剂量2mg/kg每周;HER2阴性组仅接受相同的节拍式化疗方案,总治疗周期17周。实验所用关键产品:R&D Systems的VEGF和MCSF ELISA试剂盒。结果解读显示,入组患者中HER2阳性组均为III期乳腺癌,HER2阴性组36%为III期;HER2阳性组病理完全缓解率为55.5%(n=9),HER2阴性组为18%(n=11)。
3.2 血清样本采集与检测方法优化
实验目的是获取合格的血清样本,准确检测VEGF和MCSF的动态水平。方法细节为在治疗基线(首次给药±7天)及每3周(±7天)采集血清样本,直至第18周,样本采集后室温孵育30分钟,4℃下1500g离心10分钟,分装后-80℃保存,排除溶血等不合格样本;采用酶联免疫吸附试验检测血清VEGF和MCSF水平,严格按照试剂盒说明书操作;统计学处理采用末次观测结转法(LOCF)处理缺失数据,线性回归分析因子变化趋势。结果解读显示,共纳入HER2阳性组96份样本、HER2阴性组108份样本,HER2阴性组2例因样本采集量不足50%被排除;基线时HER2阴性组血清VEGF水平高于HER2阳性组。
3.3 血清VEGF与MCSF水平动态变化分析
实验目的是对比不同HER2亚型患者在治疗过程中VEGF和MCSF的水平变化趋势。方法细节为对两组患者各时间点的血清因子水平进行线性回归趋势分析,绘制散点图并计算R²值。结果解读显示,HER2阳性组血清MCSF水平在治疗过程中保持稳定(范围约50pg/mL至450pg/mL),VEGF水平呈轻微下降趋势;HER2阴性组血清VEGF和MCSF水平均呈上升趋势。
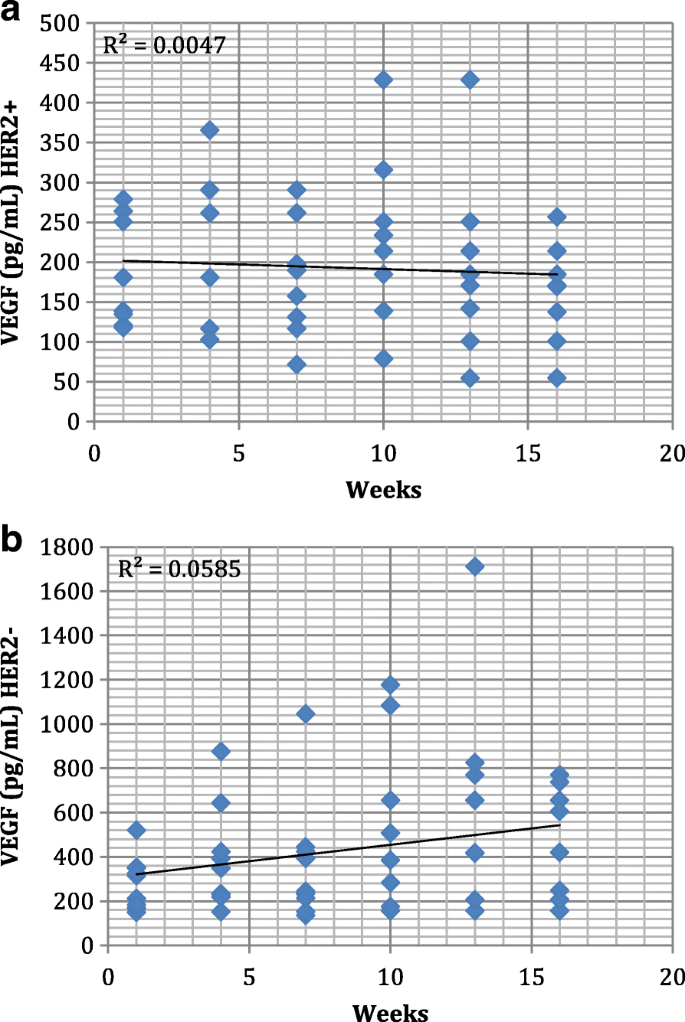
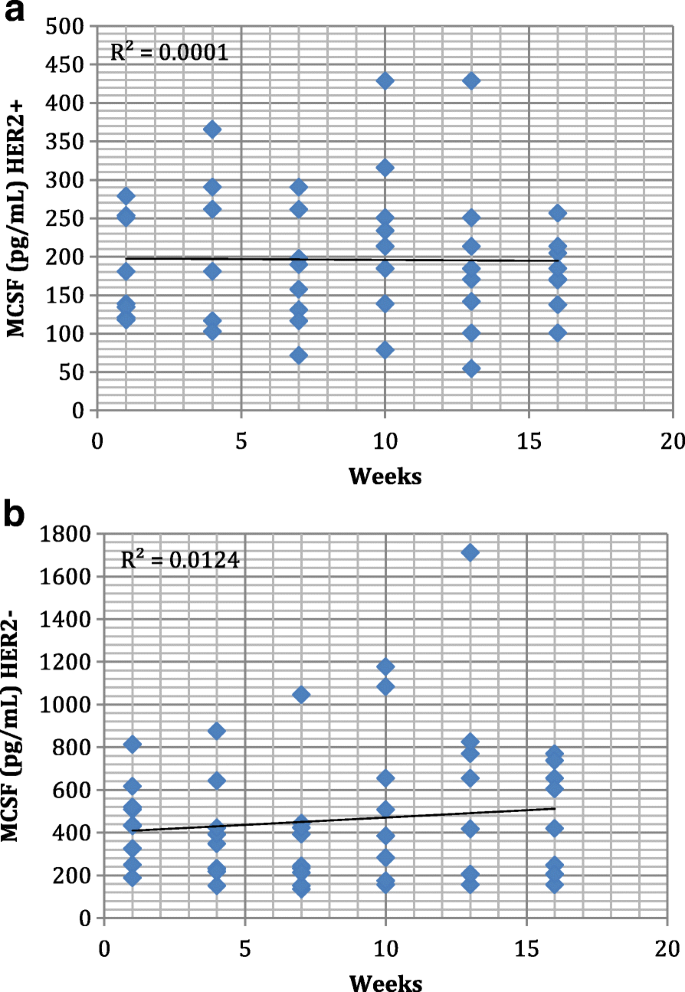
3.4 因子水平变化与病理缓解的关联分析
实验目的是明确血管生成因子变化与病理完全缓解率的关联。方法细节为对比HER2阳性与阴性组的病理完全缓解率,结合因子变化趋势进行关联分析。结果解读显示,HER2阳性组病理完全缓解率显著高于HER2阴性组,且该组VEGF水平呈下降趋势,提示VEGF水平变化可能与曲妥珠单抗的治疗响应相关。
4. Biomarker研究及发现成果解析
Biomarker定位
本文涉及的生物标志物为血清血管内皮生长因子(VEGF)和巨噬细胞集落刺激因子(MCSF),属于循环蛋白类生物标志物;筛选与验证逻辑为:基于血管生成在乳腺癌治疗中的核心作用,选择VEGF和MCSF作为候选标志物→在节拍式新辅助化疗联合或不联合曲妥珠单抗的患者中动态采集血清样本→采用酶联免疫吸附试验定量检测→分析不同HER2亚型中的变化趋势→关联病理缓解率进行临床验证,逻辑链条完整。
研究过程详述
Biomarker来源为乳腺癌患者治疗过程中的血清样本;验证方法为酶联免疫吸附试验,采用R&D Systems的专用试剂盒;特异性与敏感性数据方面,文献未明确提供ROC曲线等定量数据,但基线时HER2阴性组VEGF水平高于HER2阳性组(文献未明确具体数值),HER2阳性组VEGF水平呈下降趋势,HER2阴性组呈上升趋势;MCSF在HER2阳性组保持稳定,HER2阴性组呈上升趋势。
核心成果提炼
该研究发现,在节拍式新辅助化疗联合曲妥珠单抗治疗的HER2阳性乳腺癌患者中,血清VEGF水平呈下降趋势,且病理完全缓解率(55.5%,n=9)显著高于仅接受节拍式化疗的HER2阴性患者(18%,n=11);MCSF在HER2阳性组保持稳定,HER2阴性组呈上升趋势。创新性在于首次在临床研究中动态监测了不同HER2亚型患者在节拍式新辅助化疗下的血管生成因子变化,为曲妥珠单抗通过血管生成通路发挥抗肿瘤作用提供了临床证据。统计学结果显示,HER2阳性组病理完全缓解率高于HER2阴性组,但文献未明确组间比较的P值。推测:VEGF可能作为预测HER2阳性乳腺癌患者曲妥珠单抗联合节拍式新辅助化疗响应的潜在生物标志物,需更大样本量的随机对照研究进一步验证。
