1. 领域背景与文献引入
文献英文标题:Direct and indirect effects of IFN-α2b in malignancy treatment: not only an archer but also an arrow;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗、细胞因子靶向治疗
恶性肿瘤是全球重大公共卫生问题,在美国已成为第二大死因,尽管近年总体发病率和死亡率有所下降,但肿瘤异质性、早期临床症状缺乏导致的诊断延迟等问题,仍为临床治疗带来巨大挑战。手术仅适用于早期确诊患者,晚期肿瘤患者依赖放化疗、靶向治疗及免疫治疗,其中细胞因子治疗作为免疫治疗的重要分支,在肿瘤治疗中发挥着关键作用。干扰素-α2b(IFN-α2b)作为IFN-α家族的核心成员,已被美国FDA批准用于毛细胞白血病、肾癌和黑色素瘤等肿瘤的治疗,但其临床应用仍存在部分患者响应率低、耐药性突出、副作用明显等未解决问题,现有研究对其抗肿瘤的双重作用机制、通路调控网络及临床优化方案的总结不够系统。基于此,本文献旨在全面梳理IFN-α2b的直接与间接抗肿瘤作用机制、临床应用现状及治疗挑战,为后续研究及临床实践提供完整的理论框架与参考依据。
2. 文献综述解析
本文献以IFN-α2b的抗肿瘤作用为核心,按照“分子基础-机制通路-临床应用-挑战展望”的逻辑框架展开综述,分类维度涵盖分子结构特征、信号通路网络、细胞与免疫层面的双重作用、不同肿瘤类型的临床应用及治疗优化策略。
现有研究已充分证实IFN-α2b的抗肿瘤价值,基础研究显示其可通过激活JAK-STAT等通路直接诱导肿瘤细胞周期阻滞、凋亡,同时通过调控肿瘤微环境增强免疫细胞功能;临床研究中,高剂量IFN-α2b辅助治疗可延长高危黑色素瘤患者的无复发生存期,与阿糖胞苷联合可控制慢性粒细胞白血病进展,在肝癌治疗中也展现出抑制复发的疗效。研究方法涵盖细胞实验、动物模型及多中心临床研究,其中基因编辑、蛋白组学等技术为机制解析提供了支撑,但现有研究仍存在局限性,如胃肠道肿瘤等实体瘤的响应数据不足,联合治疗方案的循证医学证据有限,耐药机制的研究尚未完全阐明,副作用的管理策略有待优化。
与现有研究相比,本文献的创新价值在于首次系统整合了IFN-α2b直接与间接抗肿瘤作用的协同机制,详细梳理了JAK-STAT通路各关键组分(IFNAR、JAKs、ISGF3)的调控因子及干预策略,同时全面总结了不同肿瘤类型中的临床应用场景及疗效差异,为解决IFN-α2b治疗的耐药性问题、优化联合治疗方案提供了全面的理论基础,填补了现有综述在机制整合与临床应用系统总结方面的空白。
3. 研究思路总结与详细解析
本文献作为综述性研究,整体思路遵循“基础背景铺垫-核心机制解析-临床应用总结-挑战与展望”的逻辑闭环,核心科学问题是明确IFN-α2b抗肿瘤的双重作用机制、通路调控网络及临床应用的优化方向,通过整合1957年以来的大量基础与临床研究数据,构建了IFN-α2b抗肿瘤作用的完整知识体系。
3.1 IFN-α家族与IFN-α2b分子特征解析
实验目的:明确IFN-α2b的分子起源、结构特征及临床应用的分子基础;
方法细节:综述了1957年IFN的发现历程,通过CLUSTALW和ESPript 3.0工具完成IFN-α亚型的蛋白序列比对,结合PubChem数据库的分子结构数据进行分析;
结果解读:IFN家族分为I、II、III型,IFN-α属于I型家族,包含至少24个亚型,IFN-α2b与临床常用的IFN-α2a的核心差异为第23位氨基酸(IFN-α2b为精氨酸,IFN-α2a为赖氨酸),其2D与3D结构显示出特定的功能域,为结合细胞表面受体激活下游通路提供了结构基础;

产品关联:文献未提及具体实验产品,领域常规使用蛋白序列分析软件、分子结构数据库、重组细胞因子试剂等。
3.2 抗肿瘤核心通路与调控机制总结
实验目的:解析IFN-α2b激活的关键信号通路及多层面调控网络;
方法细节:整合了大量细胞实验、动物模型及临床研究数据,重点梳理JAK-STAT通路的激活过程及与其他通路的交互作用;
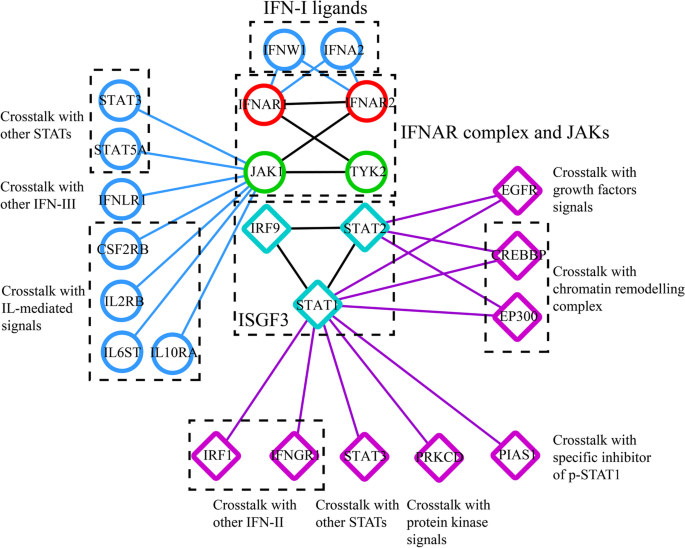
结果解读:IFN-α2b主要通过结合细胞表面的IFNAR异二聚体(IFNAR1和IFNAR2)激活JAK-STAT通路,JAK1和TYK2激酶被激活后磷酸化STAT1和STAT2,形成IFN刺激基因因子3(ISGF3)复合物,结合基因组上的IFN刺激响应元件(ISRE)调控下游IFN刺激基因(ISGs)的表达;同时IFN-α2b可调控Wnt/β-catenin、Beclin1、Notch等通路,参与细胞周期阻滞、自噬等过程;通路各环节存在负调控因子(如SOCS1、USP18)及其他调控机制(如蛋白降解、非编码RNA调控)以维持细胞稳态;
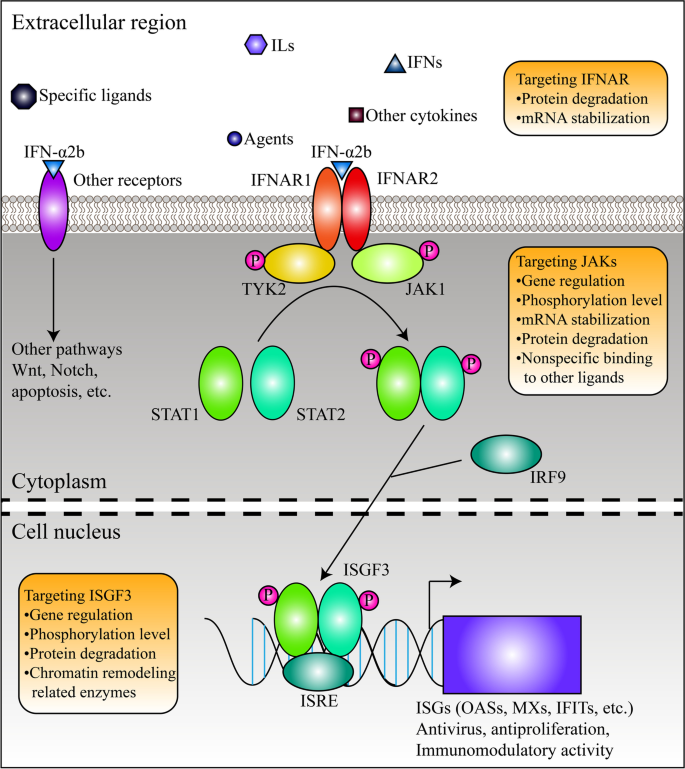
产品关联:文献未提及具体实验产品,领域常规使用Western blot、免疫荧光、qRT-PCR等实验技术,以及通路抑制剂、CRISPR-Cas9基因编辑工具等。
3.3 直接与间接抗肿瘤作用梳理
实验目的:明确IFN-α2b对肿瘤细胞及肿瘤微环境的双重调控作用;
方法细节:综述了细胞实验中IFN-α2b对肿瘤细胞的直接作用,以及临床研究中对免疫细胞的调控效应;
结果解读:直接作用包括诱导肿瘤细胞G1期阻滞、凋亡、抑制血管生成,对肿瘤的发生发展产生直接抑制;间接作用包括增强树突状细胞、巨噬细胞、自然杀伤(NK)细胞的增殖、成熟及抗原递呈能力,激活适应性免疫应答;直接与间接作用可形成协同效应,促进肿瘤细胞裂解及肿瘤抗原释放,进一步增强免疫应答;部分ISGs(如IFIT2、MX1)具有独立的肿瘤抑制功能;
产品关联:文献未提及具体实验产品,领域常规使用细胞培养试剂、免疫细胞分离试剂盒、流式细胞仪等。
3.4 临床应用场景与方案分析
实验目的:总结IFN-α2b在不同肿瘤类型中的临床应用及疗效差异;
方法细节:整合了多中心临床研究数据,按肿瘤类型(黑色素瘤、血液系统肿瘤、消化系统肿瘤等)分类总结治疗方案及疗效;
结果解读:在黑色素瘤中,高剂量IFN-α2b辅助治疗可延长高危患者无复发生存期,但与单抗、化疗等联合治疗方案的疗效未达预期;在慢性粒细胞白血病中,与阿糖胞苷联合可控制疾病进展,与靶向药联合可提高细胞遗传学响应率;在肝癌中,与5-氟尿嘧啶联合或射频消融后维持治疗可显著抑制复发;局部给药(如眼用制剂、膀胱灌注)在眼表肿瘤、浅表膀胱癌等特定肿瘤中展现出副作用小的优势;
产品关联:文献未提及具体实验产品,领域常规使用重组IFN-α2b制剂、化疗药物、免疫检查点抑制剂等。
3.5 治疗挑战与优化策略探讨
实验目的:分析IFN-α2b治疗的现存问题及潜在解决方案;
方法细节:综述了临床研究中出现的耐药性、副作用、患者分层等问题,结合机制研究探讨优化策略;
结果解读:治疗挑战包括肿瘤异质性导致的耐药(如JAK、STAT突变)、流感样症状、肝肾功能损伤等副作用、缺乏有效的Biomarker进行患者分层;优化策略包括调控通路关键组分(如稳定IFNAR1、抑制JAK-STAT3通路)、联合溶瘤病毒治疗、开发长效制剂(如PEG-IFN-α2b)、基于Biomarker的精准治疗;
产品关联:文献未提及具体实验产品,领域常规使用溶瘤病毒制剂、JAK抑制剂、PEG修饰试剂等。
4. Biomarker研究及发现成果解析
本文献涉及多种与IFN-α2b治疗相关的Biomarker,涵盖通路功能组分、血清细胞因子、自身抗体及ISGs,可用于患者分层、治疗响应监测及预后评估,为精准治疗提供重要依据。
Biomarker定位分为三类:一是通路功能组分(IFNAR1、JAK1、STAT1、ISGs),筛选验证逻辑为基于细胞实验的通路激活分析及临床样本的关联研究;二是血清预后标志物(TNF-RII、TGF-α、TIMP-1、CRP),筛选验证逻辑为基于黑色素瘤患者的临床队列研究;三是自身抗体及治疗响应标志物(如p-STAT1、ICAM1),筛选验证逻辑为基于临床治疗前后的样本检测。
研究过程详述:通路组分Biomarker通过细胞实验验证其表达水平与IFN-α2b敏感性的关联,如IFNAR1缺失会导致NK细胞功能受损、肿瘤进展加速;血清四标志物模型基于黑色素瘤患者的临床队列研究,可预测患者的不良预后(文献未明确提供特异性敏感性数据,基于图表趋势推测);治疗响应标志物如p-STAT1、ISGs可反映通路激活情况,ICAM1的表达变化可监测免疫应答强度。
核心成果提炼:这些Biomarker的功能关联包括,通路组分可预测治疗敏感性,血清标志物可评估预后,自身抗体可反映免疫激活状态;创新性在于系统总结了不同类型Biomarker在IFN-α2b治疗中的应用价值,为患者分层治疗、疗效监测提供了潜在靶点;其中四标志物模型对黑色素瘤患者的预后预测具有临床意义(文献未明确提供统计学结果),p-STAT1的表达水平与治疗响应率显著相关(文献未明确提供P值及样本量)。
