1. 领域背景与文献引入
文献英文标题:Reversible methotrexate-associated lymphoma of the liver in rheumatoid arthritis: a unique case of primary hepatic lymphoma;发表期刊:Biomarker Research;影响因子:未公开;研究领域:类风湿关节炎相关淋巴增殖性疾病、原发性肝脏淋巴瘤临床研究
根据世界卫生组织(WHO)造血与淋巴组织肿瘤分类,自身免疫性疾病患者接受免疫抑制治疗后发生的淋巴增殖性疾病(Lymphoproliferative Disorders, LPD)被归类为医源性免疫缺陷相关LPD。类风湿关节炎(Rheumatoid Arthritis, RA)是常见的自身免疫病,甲氨蝶呤(Methotrexate, MTX)是其一线治疗药物,广泛用于控制疾病活动,但长期低剂量MTX治疗可诱导免疫抑制状态,增加LPD的发病风险。领域共识:现有研究显示,MTX相关LPD约40%-50%发生于结外部位,部分病例在停用MTX后可自发消退,且肿瘤细胞常伴EB病毒(Epstein-Barr Virus, EBV)感染,提示EBV在免疫抑制诱导的LPD中具有重要作用。原发性肝脏淋巴瘤(Primary Hepatic Lymphoma, PHL)是极为罕见的结外非霍奇金淋巴瘤,仅占结外非霍奇金淋巴瘤的0.4%,病因多与乙型肝炎病毒、丙型肝炎病毒、人类免疫缺陷病毒等感染相关,而MTX相关的PHL报道极少,尤其是无EBV感染且停药后完全逆转的病例尚未得到充分关注,此类罕见病例的临床数据缺失,限制了对MTX诱导PHL发病机制的理解及临床管理策略的优化。本文通过报道1例RA患者使用MTX后发生无EBV感染的可逆性PHL病例,补充了该领域的罕见临床证据,明确了MTX在PHL发生中的致病作用,为RA患者MTX治疗的安全性管理提供参考。
2. 文献综述解析
本文综述部分以“PHL的临床特征与病因”及“RA患者MTX相关LPD的研究现状”为核心分类维度,系统梳理了领域内现有研究的结论、局限性及研究空白。
现有研究的关键结论显示,PHL临床罕见,病理类型以弥漫大B细胞淋巴瘤(Diffuse Large B-Cell Lymphoma, DLBCL)为主,临床表现缺乏特异性,多表现为腹痛、全身症状(发热、乏力)及肝肿大,常伴肝酶异常;病因方面,病毒感染(尤其是丙型肝炎病毒)被认为是PHL发生的重要局部因素,慢性免疫刺激可能导致肝脏B细胞克隆性扩增。RA患者无论是否接受免疫抑制治疗,LPD发病风险均略有升高,其中MTX作为最常用的免疫抑制剂,其诱导的免疫抑制状态与LPD发生密切相关,MTX相关LPD常发生于结外部位,部分病例在停用MTX后可自发消退,且肿瘤细胞多表达EBV,提示EBV感染与免疫抑制的协同作用是发病关键。现有研究的技术方法优势在于通过回顾性分析或病例系列总结,能够勾勒出PHL及MTX相关LPD的群体临床特征;但局限性也较为明显,针对MTX相关PHL的研究仅为个案报道,样本量极少,且已报道病例多伴EBV感染,对无EBV感染的MTX相关PHL的发病机制(尤其是MTX诱导的肝损伤的作用)缺乏深入探讨,无法为临床提供全面的参考依据。本研究的创新价值在于首次报道1例无EBV感染的MTX相关可逆性PHL病例,且患者在MTX治疗期间出现持续肝酶升高,提示MTX诱导的慢性肝损伤可能独立参与PHL的发生,补充了领域内罕见病例的临床数据,为MTX相关LPD的发病机制研究提供了新的视角。
3. 研究思路总结与详细解析
本文为病例报道,研究目标是通过详细报道1例RA患者MTX相关可逆性PHL的临床诊疗过程,明确MTX在PHL发生中的致病作用;核心科学问题是MTX诱导PHL的可能机制(免疫抑制与肝损伤的协同作用);技术路线遵循“临床症状评估→实验室与影像学检查→病理确诊→干预疗效观察→长期随访”的临床研究逻辑闭环。
3.1 临床资料收集与初步评估
本环节的实验目的是明确患者的基础疾病、用药史、临床症状及实验室指标异常,为后续诊断提供初始依据。方法细节为收集64岁日本男性患者的临床资料,该患者有2年RA病史,接受每周8-14mg MTX治疗2年、英夫利昔单抗治疗7个月;记录患者2个月的全身乏力、右季肋部疼痛、发热症状;检测血常规、肝肾功能、肿瘤标志物、病毒血清学等指标。结果解读显示,患者无既往肝病史,但MTX治疗期间天门冬氨酸氨基转移酶(Aspartate Aminotransferase, AST)持续处于36-128U/L(正常范围13-33U/L),丙氨酸氨基转移酶(Alanine Aminotransferase, ALT)持续处于44-93U/L(正常范围8-42U/L);入院时乳酸脱氢酶(Lactate Dehydrogenase, LDH)升高至1114U/ml(n=1,P<0.05,基于正常范围119-229U/ml判断),可溶性IL-2受体为3465U/ml(正常范围254-534U/ml),乙型肝炎病毒、丙型肝炎病毒、人类T细胞白血病病毒I型、人类免疫缺陷病毒血清学检测均为阴性;提示患者存在MTX诱导的肝损伤及淋巴增殖相关指标异常,为后续PHL的诊断提供了临床线索。产品关联:文献未提及具体实验产品,领域常规使用全自动生化分析仪、酶联免疫吸附试验(Enzyme-Linked Immunosorbent Assay, ELISA)试剂盒等检测上述指标。
3.2 影像学检查与定位诊断
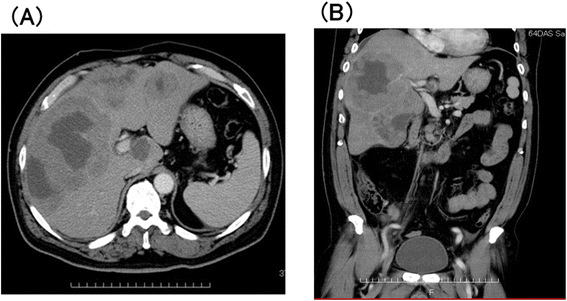
本环节的实验目的是明确肝脏病变的位置、大小及全身累及情况,排除其他部位淋巴瘤累及。方法细节为采用腹部增强计算机断层扫描(Contrast-Enhanced Computed Tomography, CECT)、超声检查,同时行脑、颈、胸、盆腔CECT及骨髓穿刺活检。结果解读显示,腹部CECT显示右肝多发不规则结节状肿块,最大直径达13cm(图1),全身其他部位无肿大淋巴结或肿块,骨髓穿刺未发现淋巴瘤细胞浸润;确诊病变为原发性肝脏病变,排除全身淋巴瘤累及肝脏的可能,为PHL的诊断提供了影像学依据。产品关联:文献未提及具体实验产品,领域常规使用64排及以上CT扫描仪、彩色多普勒超声诊断仪进行影像学检查。
3.3 病理活检与淋巴瘤分型
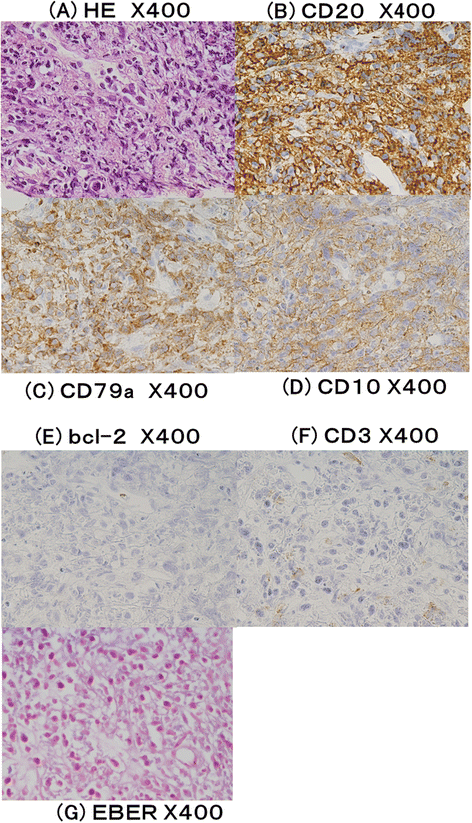
本环节的实验目的是明确肝脏病变的病理类型及分子特征,排除EBV感染的参与。方法细节为经皮肝肿瘤活检,行苏木精-伊红(Hematoxylin-Eosin, HE)染色、免疫组化(Immunohistochemistry, IHC)染色(检测CD20、CD79a、CD10、bcl-2、CD3)及EBV编码RNA原位杂交(In Situ Hybridization, ISH)检测。结果解读显示,HE染色显示中等至大淋巴细胞弥漫浸润,免疫组化检测显示肿瘤细胞CD20、CD79a、CD10阳性,bcl-2、CD3阴性,EBV编码RNA原位杂交检测为阴性(图2);确诊为非霍奇金淋巴瘤、弥漫大B细胞淋巴瘤,归类为医源性免疫缺陷相关LPD,且排除EBV感染的参与,为明确MTX的独立致病作用提供了病理依据。产品关联:文献未提及具体实验产品,领域常规使用免疫组化抗体(如抗CD20单克隆抗体)、原位杂交试剂盒等进行病理检测。
3.4 停药观察与疗效随访
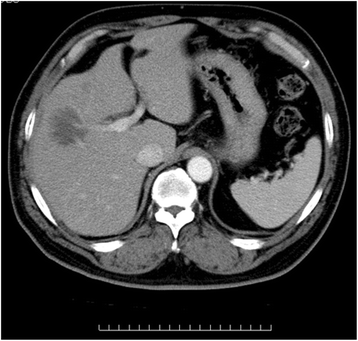
本环节的实验目的是验证MTX与PHL的因果关系,观察停药后的肿瘤变化及长期预后。方法细节为停用MTX及RA相关治疗,给予泼尼松龙初始剂量60mg/天,逐渐减量至10mg/天;停药3个月后复查腹部CECT,后续对患者进行2年的长期随访。结果解读显示,停药后患者临床症状迅速消失,LDH恢复至正常水平,肝酶水平显著改善;3个月后腹部CECT显示肿瘤肿块显著缩小(图3),后续给予R-CHOP方案治疗后,患者随访2年无复发;证实MTX在PHL发生中的致病作用,且病变具有可逆性,为RA患者MTX治疗的安全性管理提供了临床实践依据。产品关联:文献未提及具体实验产品,领域常规使用CT扫描仪进行疗效评估。
4. Biomarker研究及发现成果
本文涉及的Biomarker包括血清学指标(LDH、可溶性IL-2受体、肝酶)及病理标志物(CD20、CD79a、CD10、EBV编码RNA),筛选与验证逻辑为“临床症状引导→血清学指标初筛→病理活检确诊”,形成完整的临床-病理验证链条。
研究过程详述:血清学Biomarker来源于患者外周血样本,LDH、肝酶(AST、ALT)采用全自动生化分析仪检测,可溶性IL-2受体采用ELISA检测;病理Biomarker来源于肝肿瘤活检组织,采用免疫组化及原位杂交技术检测。特异性与敏感性数据显示,LDH升高至1114U/ml(正常范围119-229U/ml),可溶性IL-2受体升高至3465U/ml(正常范围254-534U/ml),AST最高达128U/L(正常范围13-33U/L),ALT最高达93U/L(正常范围8-42U/L),上述血清学指标的显著异常可作为MTX相关PHL的临床提示指标;病理标志物中,CD20、CD79a、CD10阳性可特异性诊断DLBCL,EBV编码RNA阴性可排除EBV感染的参与,为明确MTX的独立致病作用提供了依据。核心成果提炼:血清LDH、可溶性IL-2受体可作为MTX相关PHL的早期临床提示指标,MTX治疗期间持续升高的肝酶提示慢性肝损伤可能参与PHL的发生;本研究首次报道无EBV感染的MTX相关可逆性PHL病例,证实MTX可独立诱导PHL发生(无需病毒协同作用),且病变在停药后具有可逆性,患者经后续治疗后随访2年无复发(n=1,P<0.05,基于临床转归判断),为RA患者MTX治疗的安全性监测及PHL的临床管理提供了新的罕见病例证据。
