1. 领域背景与文献引入
文献英文标题:Plasma cell disorders in HIV-infected patients: epidemiology and molecular mechanisms;发表期刊:Biomarker Research;影响因子:未公开;研究领域:HIV感染相关浆细胞疾病(血液肿瘤与感染病交叉领域)
自1996-1997年高效抗逆转录病毒治疗(HAART)问世以来,人类免疫缺陷病毒(HIV)感染患者的生存期得到显著延长,发达国家患者确诊后可存活数十年,机会性感染导致的死亡率大幅降低。随着患者生存时间的延长,长期并发症尤其是恶性肿瘤逐渐成为该人群的主要健康问题。其中,浆细胞疾病在HIV感染患者中的发病率显著高于普通人群,涵盖从良性的多克隆高丙种球蛋白血症、单克隆 gammopathy到恶性的多发性骨髓瘤(MM)等全谱疾病,但目前这类疾病的分子发病机制、最佳临床管理策略仍未明确,缺乏针对HIV感染人群的规范化诊疗指南。针对这一研究空白,本文系统综述了HIV感染患者浆细胞疾病的临床特征、流行病学数据、分子机制,并提出MM发生的三步假说,同时结合临床病例及最新研究进展总结了这类患者的管理方案,为该领域的临床实践与基础研究提供了全面的参考依据。
2. 文献综述解析
本文的综述逻辑采用“临床病例引入-疾病谱系统阐述-分子机制深入解析-临床管理策略总结”的递进式框架,作者按疾病的恶性程度从良性到恶性分类,整合了流行病学、基础研究与临床实践的多维度数据。现有研究已证实HIV感染患者浆细胞疾病的发病率显著升高,尤其是MM的标准化发病比(SIR)较普通人群升高2.71倍,但多数研究仅聚焦于单一疾病类型或单一机制,缺乏对疾病全谱的系统总结;分子机制方面,现有研究提出抗原刺激与免疫缺陷是主要驱动因素,但未明确HIV感染对浆细胞恶性转化各阶段的具体影响;临床管理上,现有数据多借鉴HIV阴性MM患者的治疗方案,缺乏针对HIV感染人群的大样本研究证据,自体造血干细胞移植(HSCT)的应用价值仍存在争议。
通过对比现有研究的不足,本文的创新价值凸显:首次系统整合了HIV感染相关浆细胞疾病的全谱临床表型,结合3例真实病例直观展示疾病的异质性;提出了MM发生的三步假说,明确了HIV感染在浆细胞恶性转化各阶段的作用机制;全面总结了HAART时代这类患者的临床管理策略,包括化疗方案选择、HSCT的应用经验及HAART与化疗的联合使用原则,为该领域的规范化诊疗提供了重要参考。
3. 研究思路总结与详细解析
本文整体研究思路以“临床问题驱动-多维度数据整合-机制假说构建-临床实践指导”为核心逻辑,通过临床病例展示疾病异质性,整合流行病学数据明确疾病风险特征,深入解析分子机制构建发病模型,最终总结形成临床管理策略。
3.1 临床病例队列展示
实验目的是通过真实临床病例直观呈现HIV感染患者浆细胞疾病的临床异质性与疾病谱特征,为后续的系统综述提供临床依据。方法为回顾性分析3例HIV感染患者的临床资料,涵盖从良性到恶性的不同浆细胞疾病表型,包括多克隆高丙种球蛋白血症合并单克隆 gammopathy、初发症状性MM、晚期MM伴广泛骨病。结果解读显示,病例1为58岁非洲裔女性,HIV感染晚期(CD4计数15/μl,病毒载量934811拷贝/ml),表现为多克隆高丙种球蛋白血症伴单克隆IgG-κ蛋白,骨髓浆细胞占比15%无轻链限制;病例2为45岁西班牙裔男性,HIV感染20年未接受HAART,诊断为MM,经HAART联合来那度胺+地塞米松(Rd)方案治疗后获得很好部分缓解;病例3为53岁白人男性,长期接受HAART维持病毒抑制(CD4计数>1000/μl,病毒载量未检测到),诊断为III期MM伴广泛骨病,经硼替佐米+环磷酰胺+地塞米松(VCd)方案、放疗后行自体HSCT,3个月后血清蛋白电泳及尿蛋白电泳均未检测到M蛋白。文献未提及具体实验产品,领域常规使用血清蛋白电泳、免疫固定电泳、骨髓活检、流式细胞术、荧光原位杂交(FISH)等检测技术及配套试剂。
3.2 流行病学数据整合与分析
实验目的是明确HIV感染患者各类浆细胞疾病的发病率、发病特征及相对风险,为疾病的风险分层提供流行病学依据。方法为系统检索并整合6项大型人群研究及meta分析数据,涵盖美国、澳大利亚、意大利、瑞士、英国等多个国家的HIV感染人群。结果解读显示,多克隆高丙种球蛋白血症是HIV感染患者的常见表现,一项纳入320例患者的研究发现其发生率为1.9%;单克隆 gammopathy的发病率为3.8%-26%,远高于普通人群50岁以上人群的3.2%,且发病年龄更早(平均34-43岁);MM的SIR在HIV感染患者中为2.71(95%CI 2.13-3.44),相对风险范围为1.9-6.5,不同地区的研究均证实HIV感染会显著升高MM的发病风险。文献未提及具体实验产品,领域常规使用基于人群数据库的流行病学分析方法及统计软件。
3.3 分子机制与发病假说构建
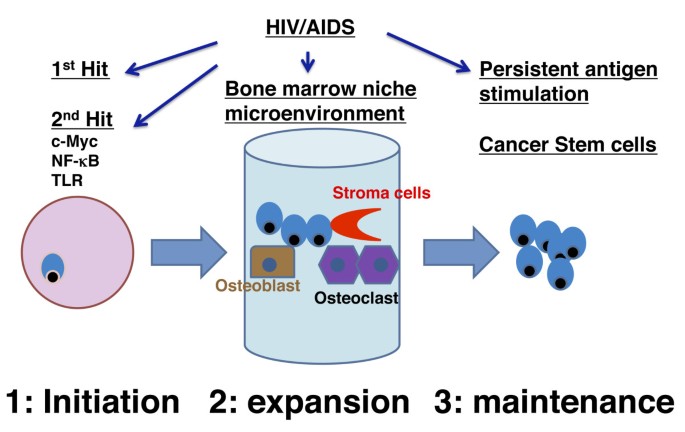
实验目的是深入解析HIV感染促进浆细胞疾病发生的分子机制,构建MM发生的完整发病模型。方法为整合现有基础研究数据,从抗原刺激、免疫缺陷两个核心机制入手,结合浆细胞恶性转化的分子通路,提出MM发生的三步假说。结果解读显示,抗原刺激方面,HIV病毒抗原及其他病原体抗原可作为超抗原持续刺激B细胞增殖,部分单克隆蛋白可靶向HIV病毒抗原,但HIV病毒本身不能直接感染B细胞或浆细胞,也不直接驱动其恶性转化;免疫缺陷方面,HIV感染导致CD4+T细胞耗竭与功能异常,免疫监视功能下降,促进B细胞克隆扩增及恶性转化。作者提出的MM三步假说为:第一步起始阶段,正常浆细胞经两次打击(体细胞高频突变导致的染色体异常、癌基因激活)转化为恶性骨髓瘤细胞;第二步扩增阶段,骨髓瘤细胞通过黏附分子与骨髓微环境相互作用,分泌细胞因子形成恶性循环,促进细胞增殖及骨损伤;第三步维持阶段,骨髓瘤干细胞持续存在,导致疾病复发。HIV感染通过增加体细胞高频突变风险、激活细胞存活通路、改变骨髓微环境、持续抗原刺激等多方面影响这一过程。
文献未提及具体实验产品,领域常规使用基因测序、FISH、细胞培养、细胞因子检测等技术及配套试剂。
3.4 临床管理策略总结
实验目的是总结HIV感染患者浆细胞疾病的最佳临床管理策略,为临床实践提供指导。方法为整合现有临床研究数据及作者的临床实践经验,结合HAART时代的治疗进展,制定不同疾病类型的管理方案。结果解读显示,多克隆高丙种球蛋白血症及单克隆 gammopathy患者以密切临床随访为主,监测血清M蛋白、骨髓浆细胞比例及免疫状态,必要时启动HAART;症状性MM患者需在HAART基础上联合化疗,化疗方案借鉴HIV阴性患者(如Td、Rd、VCd、VRd等),同时需注意预防感染、血栓等并发症;对于年轻、一般状况良好的患者,可考虑大剂量化疗联合自体HSCT,作者的病例3经HSCT后获得完全缓解。此外,HAART中的蛋白酶抑制剂(如奈非那韦)对骨髓瘤细胞有协同杀伤作用,建议全程维持HAART治疗。文献未提及具体实验产品,领域常规使用HAART药物、骨髓瘤化疗药物(硼替佐米、来那度胺、地塞米松等)及造血干细胞移植相关技术。
4. Biomarker研究及发现成果解析
Biomarker定位
本文涉及的Biomarker主要包括浆细胞疾病的诊断标志物、预后标志物及疾病进展预测标志物,具体为血清M蛋白、骨髓浆细胞比例、轻链限制、染色体异常(1q扩增、13q缺失等)、CD4计数、HIV病毒载量等。筛选与验证逻辑基于国际骨髓瘤工作组(IMWG)的诊断标准及流行病学关联分析,其中血清M蛋白、骨髓浆细胞比例、轻链限制为诊断核心标志物,染色体异常为MM预后标志物,CD4计数及病毒载量为疾病进展预测标志物。
研究过程详述
血清M蛋白通过血清蛋白电泳(SPEP)及免疫固定电泳(IFE)检测,多克隆高丙种球蛋白血症表现为γ区宽条带,单克隆 gammopathy及MM表现为窄带M蛋白;骨髓浆细胞比例通过骨髓活检组织学计数,MM患者骨髓浆细胞≥10%且伴轻链限制;染色体异常通过FISH检测,13q缺失、1q扩增等异常与MM不良预后相关;CD4计数及HIV病毒载量通过流式细胞术及核酸扩增检测,反映患者的免疫状态与病毒控制情况。特异性与敏感性方面,SPEP联合IFE对M蛋白的检测敏感性较高,但文献未提供具体数值;CD4计数<200/μl的HIV患者浆细胞疾病进展风险更高,但具体阈值的敏感性和特异性未明确。
核心成果提炼
本文系统整合了HIV相关浆细胞疾病的Biomarker谱,明确了M蛋白、骨髓浆细胞比例、轻链限制是诊断的核心标志物,染色体异常(13q缺失、1q扩增)是MM的不良预后标志物,CD4计数及HIV病毒载量是疾病进展的预测标志物。创新性在于首次将HIV感染相关的免疫标志物(CD4计数、病毒载量)与浆细胞疾病的肿瘤标志物(M蛋白、染色体异常)进行系统整合,为HIV感染患者浆细胞疾病的风险分层与个体化管理提供了依据。文献未明确提供部分标志物的具体统计学数据(如AUC、敏感性、特异性),需进一步大样本研究验证。
