1. 领域背景与文献引入
文献英文标题:CAR-NK cells for cancer immunotherapy: from bench to bedside;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗(CAR-NK细胞免疫治疗)
肿瘤免疫治疗历经数十年发展,2014年PD-1抑制剂获批开启免疫检查点治疗时代,2017年首款CAR-T细胞产品获批为血液瘤患者带来突破性治疗选择,但CAR-T细胞治疗存在细胞因子释放综合征(CRS)、移植物抗宿主病(GVHD)等严重毒性,且依赖个性化制备、实体瘤疗效有限,限制了其广泛应用。当前领域热点聚焦于开发通用型、低毒性、可大规模制备的细胞免疫治疗产品,而自然杀伤(NK)细胞凭借无需预致敏、非MHC限制性杀伤、毒性低等特性,成为CAR修饰的理想载体。本研究针对CAR-T治疗的局限性,系统综述CAR-NK细胞免疫治疗的研究进展,旨在为其大规模临床转化提供理论支撑与实践参考。
2. 文献综述解析
作者以细胞免疫治疗的技术演进与临床应用为分类维度,系统梳理了CAR-T、NK细胞免疫治疗及CAR-NK细胞治疗的研究现状,重点对比不同治疗策略的优劣,明确CAR-NK细胞治疗的创新价值与应用前景。
现有研究显示,CAR-T细胞在B细胞急性淋巴细胞白血病等血液瘤中客观缓解率较高,但存在严重的免疫相关不良反应,且实体瘤治疗中因肿瘤微环境抑制、细胞浸润不足等问题疗效不佳;NK细胞免疫治疗虽毒性较低,但缺乏肿瘤特异性,体内存活时间短,难以持续发挥抗肿瘤作用。针对上述不足,CAR-NK细胞治疗通过将CAR修饰于NK细胞,兼具CAR的肿瘤特异性识别与NK细胞的天然抗肿瘤活性,可有效降低免疫毒性,且有望实现通用型“off-the-shelf”产品制备,为解决现有细胞治疗的痛点提供新方向。本研究的创新点在于首次全面整合CAR-NK细胞的来源、CAR设计、转导技术及临床应用数据,为领域内的研究与转化提供系统性参考框架。
3. 研究思路总结与详细解析
本研究为系统性综述,核心目标是全面梳理CAR-NK细胞免疫治疗的关键技术环节与临床应用进展,核心科学问题是如何优化CAR-NK细胞的制备与应用以提升抗肿瘤疗效并降低毒性,技术路线为“分类梳理现有研究→对比分析优劣→总结进展与挑战”的逻辑闭环。
3.1 CAR-NK细胞来源分类与特性解析
实验目的:明确不同来源NK细胞用于CAR修饰的适用性与优劣;方法细节:系统综述已发表的临床前研究与临床试验,涵盖NK细胞系(NK-92、YT)、外周血来源NK(PB-NK)、脐带血来源NK(UC-NK)、胎盘血来源NK(P-NK)、干细胞来源NK(hPSC-NK)及记忆样NK(ML-NK)六大类,分析各类细胞的扩增效率、CAR转导效率、抗肿瘤活性及临床安全性;结果解读:NK-92细胞系易体外扩增,CAR转导效率较高,但源于淋巴瘤患者,输注前需辐照以降低恶变风险,临床研究显示其对急性髓系白血病具有一定抗肿瘤活性(文献未明确提供具体数据,基于图表趋势推测);UC-NK细胞具有异体反应性优势,适合制备通用型产品,一项I/II期临床试验中CD19-CAR-UC-NK治疗复发难治CD19+B细胞淋巴瘤,7例患者达到完全缓解,未出现严重毒性;hPSC-NK细胞可大规模标准化制备,有望解决细胞来源不足问题,但目前仍处于临床前研究阶段;产品关联:文献未提及具体实验产品,领域常规使用细胞培养基、细胞因子(IL-2、IL-15等)、基因转导载体等试剂与仪器。
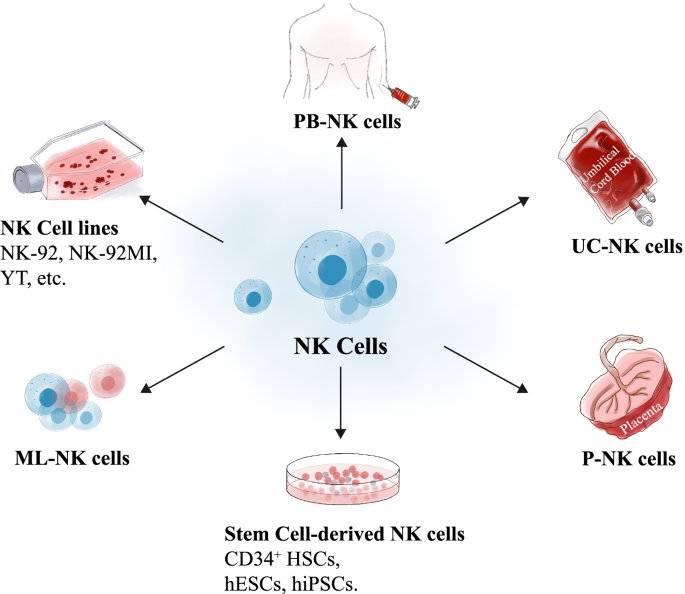
3.2 CAR靶点选择与结构设计
实验目的:筛选适合CAR-NK的肿瘤靶点并优化CAR结构以提升抗肿瘤活性;方法细节:综述已报道的CAR-NK靶点(CD19、CD20、HER2、EGFRvIII、ROBO-1等),分析靶点的肿瘤特异性表达情况,同时对比不同代次CAR(第一代至第四代)的结构差异与功能特性;结果解读:CD19是目前研究最成熟的靶点,在B细胞淋巴瘤与白血病中特异性表达,CD19-CAR-NK在临床研究中显示出73%的响应率与64%的完全缓解率(n=11,P值未明确);第四代“装甲”CAR通过整合细胞因子(如IL-15)编码序列,可提升CAR-NK细胞的体内存活时间与抗肿瘤活性;产品关联:文献未提及具体实验产品,领域常规使用重组抗体、基因合成载体等试剂。
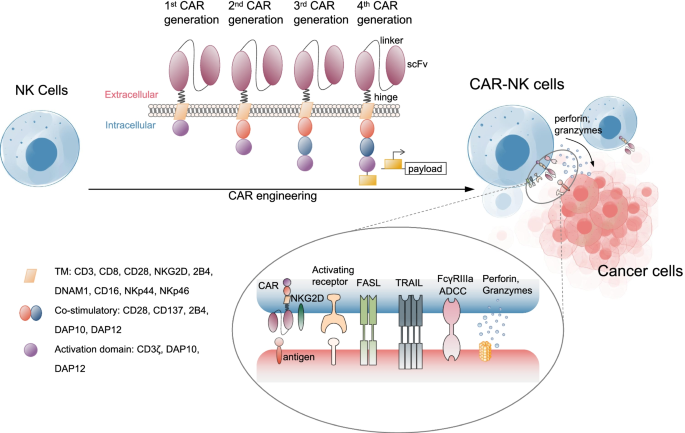
3.3 CAR转导技术比较
实验目的:对比不同CAR转导方法的效率与安全性,为CAR-NK细胞制备提供最优方案;方法细节:综述病毒转导(逆转录病毒、慢病毒)与非病毒转导(电穿孔、转座子系统)在CAR-NK细胞制备中的应用,分析转导效率、细胞毒性、转基因稳定性等指标;结果解读:慢病毒转导效率较高,对NK细胞毒性较低,适合原代NK细胞转导;转座子系统(如PiggyBac、Sleeping Beauty)具有低免疫原性、可转导大片段基因的优势,转导后转基因表达稳定,是未来通用型CAR-NK制备的潜在技术;产品关联:文献未提及具体实验产品,领域常规使用病毒载体、转座子试剂盒等试剂。
3.4 CAR-NK在血液瘤与实体瘤中的应用解析
实验目的:明确CAR-NK细胞在不同类型肿瘤中的临床疗效与应用前景;方法细节:梳理已完成或正在进行的CAR-NK临床试验,对比血液瘤与实体瘤中的治疗数据,分析疗效差异的原因;结果解读:在血液瘤中,CD19-CAR-NK治疗B细胞淋巴瘤的响应率达73%(n=11,P值未明确),且未出现严重CRS或GVHD;在实体瘤中,ROBO-1-CAR-NK-92治疗胰腺癌的临床试验显示出一定可行性,但目前临床数据有限,实体瘤疗效不佳主要源于肿瘤微环境抑制、细胞浸润不足等问题;产品关联:文献未提及具体实验产品,领域常规使用肿瘤细胞系、动物模型等实验材料。
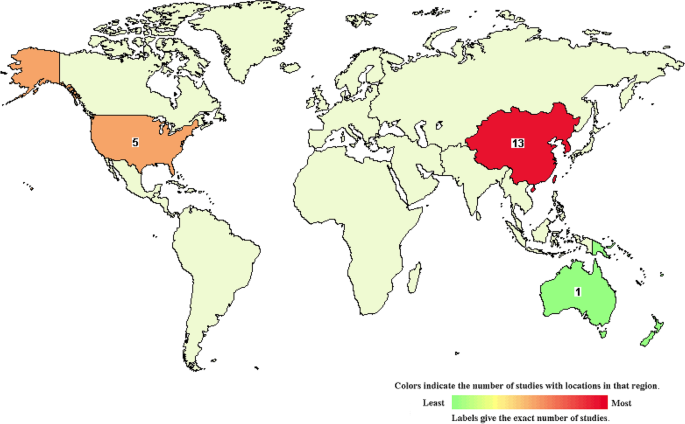
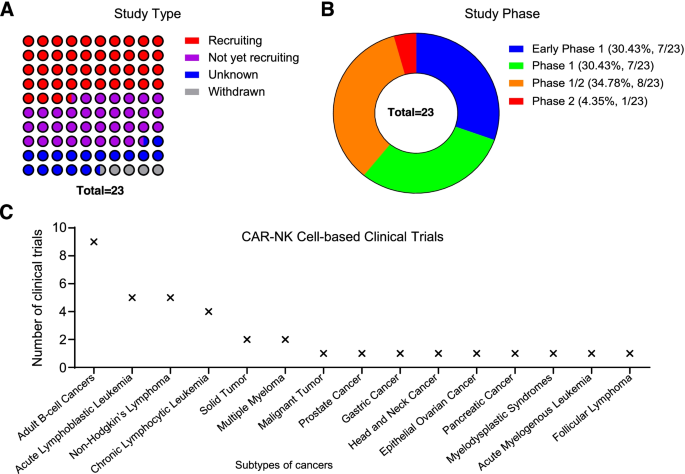
4. Biomarker研究及发现成果
本研究涉及的Biomarker包括CAR靶向的肿瘤表面抗原Biomarker、NK细胞功能Biomarker及临床疗效Biomarker,通过系统综述明确各类Biomarker的筛选逻辑与临床价值。
Biomarker定位:CAR靶向的肿瘤表面抗原(如CD19、HER2)为治疗性Biomarker,筛选逻辑为基于肿瘤特异性表达,经临床前验证后进入临床试验;NK细胞功能Biomarker(如CD56、CD16)用于鉴定NK细胞纯度与活性;临床疗效Biomarker(如完全缓解率、响应率)用于评估治疗效果。研究过程详述:CD19作为B细胞肿瘤的特异性Biomarker,通过CAR-NK靶向治疗,在11例复发难治CD19+B细胞淋巴瘤患者中实现64%的完全缓解率(n=11,P值未明确);HER2在乳腺癌、胃癌等实体瘤中高表达,HER2-CAR-NK在临床前研究中显示出对HER2阳性肿瘤细胞的特异性杀伤活性(文献未明确提供具体数据,基于图表趋势推测)。核心成果提炼:CD19等肿瘤表面抗原Biomarker为CAR-NK的精准治疗提供了特异性靶点,其中CD19-CAR-NK在血液瘤中的临床疗效已得到初步验证,风险比HR未明确;本研究首次系统性总结了CAR-NK相关Biomarker的研究进展,为后续Biomarker的开发与临床应用提供了参考框架。
