1. 领域背景与文献引入
文献英文标题:The CXCR4 antagonist plerixafor enhances the effect of rituximab in diffuse large B-cell lymphoma cell lines;发表期刊:Biomarker Research;影响因子:未公开;研究领域:弥漫大B细胞淋巴瘤靶向治疗。
弥漫大B细胞淋巴瘤(DLBCL)是一类具有高度异质性的侵袭性血液系统恶性肿瘤,占成人非霍奇金淋巴瘤的25%-30%。领域共识:当前DLBCL的标准一线治疗方案为利妥昔单抗联合环磷酰胺、多柔比星、长春新碱及泼尼松的R-CHOP方案,该方案使患者的总体生存率得到显著提升,但仍有30%-40%的患者会出现原发耐药或疾病复发,且复发难治性患者的预后极差,缺乏有效的后续治疗手段。
CXCR4-CXCL12轴在肿瘤的发生发展、侵袭转移及耐药形成中发挥关键作用,已有研究证实CXCR4高表达与DLBCL患者的不良预后显著相关,且CXCR4拮抗剂可通过阻断肿瘤细胞与骨髓微环境的相互作用,逆转肿瘤细胞的化疗耐药。此前在Burkitt淋巴瘤中已观察到CXCR4拮抗剂普乐沙福(plerixafor)可增强利妥昔单抗的抗肿瘤疗效,但该效应在DLBCL中尚未得到验证。因此,本研究旨在通过体外实验探讨普乐沙福对DLBCL细胞响应利妥昔单抗的调控作用,为DLBCL的联合治疗策略提供实验依据。
2. 文献综述解析
作者对现有研究的评述主要围绕三个维度展开:DLBCL的治疗现状与局限性、CXCR4-CXCL12轴在DLBCL中的作用及机制、CXCR4拮抗剂在淋巴瘤治疗中的研究进展。
现有研究结论显示,R-CHOP方案是DLBCL的标准一线治疗,利妥昔单抗通过补体依赖的细胞毒性(CDC)、抗体依赖的细胞介导的细胞毒性(ADCC)及诱导凋亡等机制发挥抗肿瘤作用,但部分患者会因肿瘤细胞异质性、肿瘤微环境保护等因素产生耐药。CXCR4作为G蛋白偶联受体,在DLBCL细胞表面高表达,其与配体CXCL12结合后可激活下游增殖、存活及迁移信号通路,同时介导肿瘤细胞归巢至骨髓微环境,逃避化疗药物的杀伤。CXCR4拮抗剂普乐沙福已被FDA批准用于非霍奇金淋巴瘤患者的造血干细胞动员,且在Burkitt淋巴瘤的体内实验中显示出增强利妥昔单抗疗效的作用,但DLBCL中相关研究仍为空白,且普乐沙福与利妥昔单抗联合的给药方式、剂量效应等关键问题尚未明确。
本研究的创新价值在于,首次在DLBCL细胞系中系统验证了普乐沙福与利妥昔单抗的协同抗肿瘤效应,明确了联合治疗的最优给药顺序(同时给药优于序贯给药)及剂量依赖性,同时揭示了普乐沙福下调CXCR4表面表达的作用机制,为DLBCL的联合治疗提供了新的潜在策略,填补了CXCR4拮抗剂在DLBCL中与利妥昔单抗联合应用的研究空白。
3. 研究思路总结与详细解析
本研究的核心目标是验证CXCR4拮抗剂普乐沙福对利妥昔单抗抗DLBCL细胞效应的增强作用,核心科学问题包括普乐沙福与利妥昔单抗的协同作用模式、给药顺序及剂量对效应的影响,以及普乐沙福对CXCR4表达的调控机制。研究采用“细胞模型构建→药物处理与增殖检测→凋亡分析→CXCR4表达检测”的闭环技术路线,通过两种不同分子亚型的DLBCL细胞系(ABC亚型RIVA、GCB亚型FARAGE)开展体外实验,利用线性混合效应模型进行统计学分析。
3.1 细胞模型构建与验证
实验目的:构建并验证具有不同利妥昔单抗敏感性的DLBCL细胞模型,为后续药物效应研究提供基础。
方法细节:选取人DLBCL细胞系RIVA和FARAGE,前者为ABC亚型,携带MYC重排及BCL2扩增;后者为GCB亚型,仅存在11号染色体三体。采用MTS实验确定两株细胞对利妥昔单抗的50%生长抑制(GI50)值,RIVA为3.3μg/mL,FARAGE为27.8μg/mL,证实RIVA对利妥昔单抗更敏感。细胞培养于含10%胎牛血清、青霉素及链霉素的RPMI 1640培养基中,定期传代并在实验前验证细胞身份(短串联重复序列分型)及无支原体污染。
结果解读:成功构建了具有利妥昔单抗敏感性差异的DLBCL细胞模型,RIVA细胞对利妥昔单抗的敏感性显著高于FARAGE细胞,为后续研究药物协同效应提供了理想的实验体系。
实验所用关键产品:RPMI 1640培养基(Life Technologies)、胎牛血清(Invitrogen)、EZ-PCR支原体检测试剂盒(Biological Industries)、DNeasy Blood and Tissue Kit(Qiagen)、AmpFlSTR® Identifiler® PCR扩增试剂盒(Applied Biosystems)。
3.2 药物处理与细胞增殖检测
实验目的:探讨普乐沙福与利妥昔单抗联合对DLBCL细胞增殖的影响,明确给药顺序及剂量的效应差异。
方法细节:采用台盼蓝排斥法和MTS实验检测细胞增殖,设置单药组(利妥昔单抗10μg/mL或普乐沙福500μM)、联合给药组(同时给药或序贯给药,间隔24h),以及剂量梯度组(利妥昔单抗4.17-66.67μg/mL,普乐沙福208.33-3333.33μM)。实验中加入20%人AB血清以提供补体及CXCL12,模拟体内微环境。
结果解读:台盼蓝排斥法结果显示,同时给予普乐沙福和利妥昔单抗可显著降低DLBCL细胞的活细胞数,与单药治疗相比差异具有统计学意义(RIVA细胞24-72h,P<0.001;FARAGE细胞72h,P<0.01),且协同作用呈剂量依赖性。序贯给药的效应显著弱于同时给药,RIVA细胞同时给药后活细胞数较对照组降低4倍,而序贯给药仅降低1.8倍。MTS实验进一步证实,在多数测试浓度下,联合治疗的增殖抑制效应均优于单药治疗。
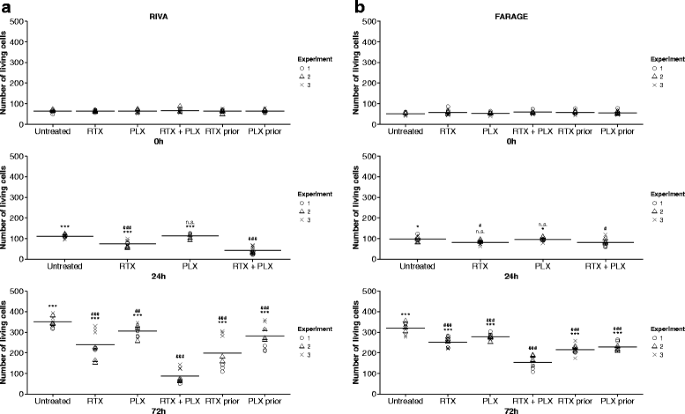
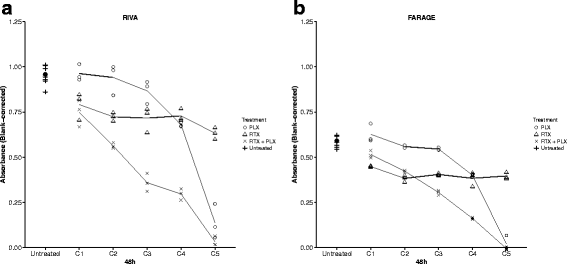
实验所用关键产品:利妥昔单抗(MabThera®,Roche)、普乐沙福(InSolution™ CXCR4 Antagonist I,Merck Millipore)、Pooled Human AB Serum(Novakemi AB)、CellTiter 96® AQueous One Solution Reagent(Promega)。
3.3 细胞凋亡状态检测
实验目的:探究普乐沙福增强利妥昔单抗效应的机制,明确联合治疗对DLBCL细胞凋亡的诱导作用。
方法细节:采用流式细胞术(FCM)检测细胞凋亡状态,给药48h后用PE标记的Annexin V和7-氨基放线菌素D(7-AAD)染色,区分活细胞、早期凋亡细胞及晚期凋亡/死亡细胞。
结果解读:联合治疗组的早期凋亡细胞比例及晚期凋亡/死亡细胞比例均显著高于单药组,RIVA细胞早期凋亡比例升高尤为明显(P<0.001),证实普乐沙福可通过增强利妥昔单抗的促凋亡作用发挥协同效应,且该效应在利妥昔单抗敏感的细胞系中更为显著。
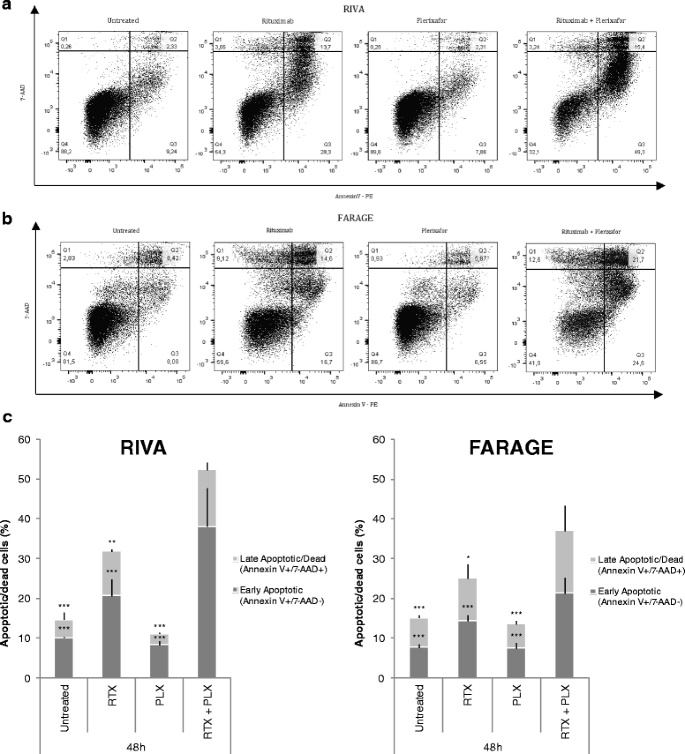
实验所用关键产品:PE Annexin V凋亡检测试剂盒I(BD Biosciences)、BD FACSCanto™ II流式细胞仪、FlowJo软件。
3.4 CXCR4表面表达检测
实验目的:分析普乐沙福及利妥昔单抗对DLBCL细胞表面CXCR4表达的调控作用,探讨其与药物效应的关联。
方法细节:给药48h后采用流式细胞术检测细胞表面CXCR4的中位荧光强度,使用APC标记的抗CXCR4抗体(clone 12G5)进行染色。
结果解读:普乐沙福单药治疗可显著降低两株细胞的CXCR4中位荧光强度(与对照组相比,P<0.001),且RIVA细胞的降低幅度更为明显;利妥昔单抗单药对CXCR4表达无显著影响,联合治疗组的CXCR4表达水平与普乐沙福单药组无显著差异,提示普乐沙福可通过下调CXCR4表面表达增强利妥昔单抗的疗效。
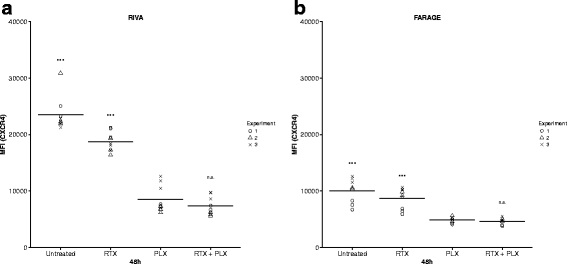
实验所用关键产品:APC标记的抗CXCR4抗体(clone 12G5,BD Biosciences)、BD FACSCanto™ II流式细胞仪、FlowJo软件。
4. Biomarker研究及发现成果
Biomarker定位
本研究涉及的Biomarker为细胞表面趋化因子受体CXCR4,属于预后及疗效预测Biomarker。筛选与验证逻辑为:基于前期研究中CXCR4高表达与DLBCL不良预后的相关性,通过体外实验验证CXCR4拮抗剂普乐沙福对CXCR4表达的调控作用,以及其与利妥昔单抗协同效应的关联,形成“临床预后关联→体外功能验证→机制探讨”的完整逻辑链条。
研究过程详述
Biomarker来源为DLBCL细胞系表面的CXCR4蛋白,验证方法为流式细胞术定量检测细胞表面CXCR4的中位荧光强度。实验结果显示,普乐沙福处理后,RIVA细胞的CXCR4中位荧光强度显著降低(n=3,P<0.001),FARAGE细胞的CXCR4表达也呈显著下降趋势(n=3,P<0.001)。未检测该Biomarker的特异性与敏感性数据(文献未明确提供该数据,基于图表趋势推测)。
核心成果提炼
本研究首次证实CXCR4拮抗剂普乐沙福可下调DLBCL细胞表面的CXCR4表达,且该下调作用与普乐沙福增强利妥昔单抗的抗增殖及促凋亡效应密切相关。在利妥昔单抗敏感的RIVA细胞中,普乐沙福与利妥昔单抗的协同效应更为显著,提示CXCR4表达水平可作为预测DLBCL患者对普乐沙福联合利妥昔单抗治疗响应的潜在Biomarker。此外,研究明确了联合治疗的最优给药方式为同时给药,为后续临床转化研究提供了关键的实验依据。
