1. 领域背景与文献引入
文献英文标题:Deciphering genes associated with diffuse large B-cell lymphoma with lymphomatous effusions: A mutational accumulation scoring approach;发表期刊:Biomarker Research;影响因子:未公开;研究领域:淋巴瘤分子生物学、肿瘤生物标志物研究。
弥漫大B细胞淋巴瘤(DLBCL)是最常见的侵袭性淋巴瘤亚型,全球范围内约占所有淋巴瘤病例的33%,台湾地区占比达40%。领域发展关键节点包括2004年Hans等通过免疫组化(IHC)技术确认DLBCL的分子亚型分类,2018年Chapuy等与Schmitz等分别解析不同DLBCL分子亚型的致病机制与预后差异,推动了DLBCL的精准诊疗进程。当前研究热点聚焦于分子亚型的细化分类、靶向治疗靶点挖掘、预后生物标志物鉴定等方向,但仍存在未解决的核心问题:伴淋巴瘤性积液的DLBCL患者预后极差,甚至比IV期无积液患者的预后更差,然而这类特殊亚型DLBCL的潜在分子致病机制、核心驱动基因及针对性治疗靶点尚未明确,临床缺乏有效的预后分层指标和干预策略。基于此,本研究假设存在与淋巴瘤性积液发生相关的特异性遗传异常,旨在通过全外显子测序结合自主设计的突变累积评分方法,筛选致病基因、解析相关通路,为这类患者的精准诊疗提供理论依据和潜在靶点。
2. 文献综述解析
作者对DLBCL领域现有研究的分类维度主要涵盖研究技术类型(基因组测序、基因表达谱分析)与研究方向(分子亚型分类、预后影响因素、致病机制解析)。
现有研究已明确DLBCL存在多种分子亚型,不同亚型的临床预后与治疗响应差异显著;淋巴瘤性积液是DLBCL患者的不良预后因素,与患者生存期缩短密切相关。全外显子测序技术能够全面解析基因组编码区的突变谱,基因表达谱分析可系统揭示细胞通路的异常激活状态,为分子机制研究提供多维度数据支持。但现有研究多聚焦于原发淋巴结来源的DLBCL,针对伴淋巴瘤性积液DLBCL的遗传机制研究较为匮乏,缺乏大样本的基因组学分析数据,尚未明确与积液形成相关的核心致病通路及驱动基因,也未建立有效的预后生物标志物。
本研究的创新价值在于,首次采用自主设计的突变累积评分方法,结合全外显子测序与基因表达谱分析,系统对比伴积液与无积液DLBCL的基因组差异,筛选出与肿瘤迁移侵袭相关的致病基因,并在独立临床队列中验证了核心基因的表达与积液存在及预后的关联,明确了TP53-MDM2通路及HDAC相关染色质重塑机制在积液形成中的关键作用,填补了该领域的研究空白,为这类患者的预后分层和靶向治疗提供了新的方向。
3. 研究思路总结与详细解析
本研究的整体框架为“样本收集→多组学测序分析→生物信息学筛选→实验验证→机制解析”,研究目标是鉴定与DLBCL淋巴瘤性积液相关的致病基因及核心通路,核心科学问题是明确伴积液DLBCL的特异性遗传异常及分子致病机制,技术路线遵循“假设驱动-实验验证-数据整合-结论推导”的闭环逻辑。
3.1 样本收集与多组学测序实验
实验目的是获取伴积液与无积液DLBCL样本的基因组与转录组数据,为后续分析提供基础。方法细节:收集9例伴淋巴瘤性积液的DLBCL样本(来自台湾成大医院,肿瘤细胞占比>80%),同时从TCGA数据库获取22例原发淋巴结DLBCL样本,对所有样本进行全外显子测序(WES);采用Agilent SureSelect XT HS Reagent kit构建测序文库,Illumina NovaSeq 6000测序仪进行150bp双端测序;另外选取4例样本(2例伴积液、2例无积液)进行基因芯片分析,采用Agilent 8×60K Microarray chip检测基因表达谱。结果解读:WES获得高质量测序数据,伴积液样本的平均测序深度为197.4x至377.2x,中位数达301.9x;共检测到3919个单核苷酸变异(SNVs)和209个插入缺失(indels),其中多数变异具有蛋白功能改变潜力。实验所用关键产品:Agilent SureSelect XT HS Reagent kit(catalog#G9704K)、Illumina NovaSeq 6000 Sequencer、Agilent 8×60 K Microarray chip。
3.2 突变累积评分与致病基因筛选
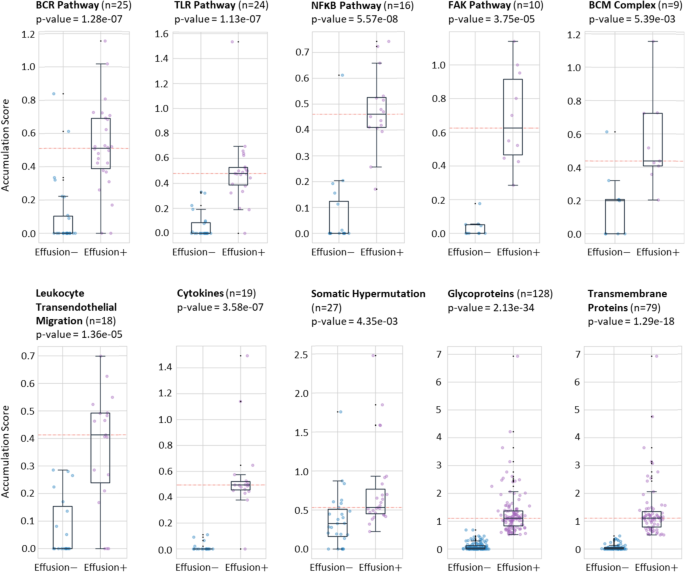
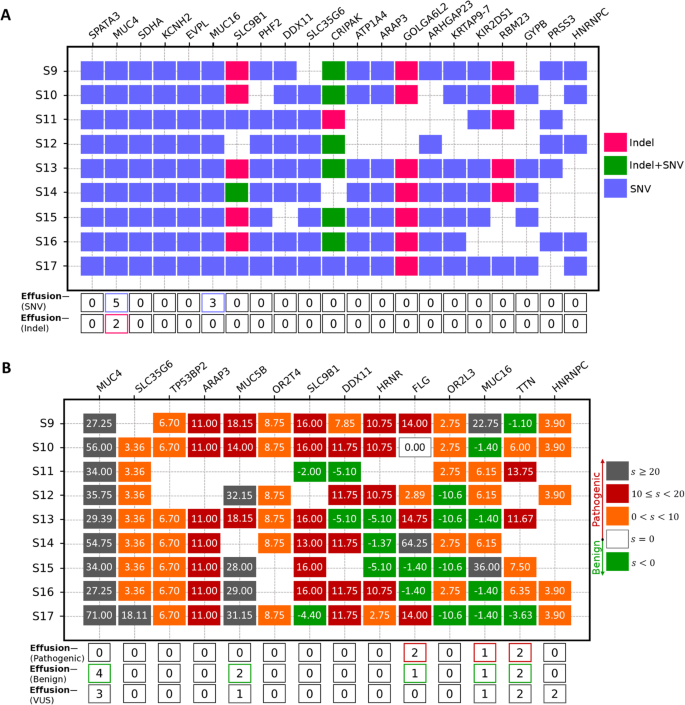
实验目的是筛选与DLBCL淋巴瘤性积液相关的高突变及致病性基因。方法细节:自主设计基于区域突变密度(RMD)的突变累积评分方法,计算每个基因在两组样本中的累积评分,评分综合考虑突变的等位基因频率与突变间的位置距离;同时采用InterVar、ClinVar、SIFT、CADD四种突变注释工具评估突变的致病性,筛选在伴积液样本中高频出现致病性突变的基因。结果解读:伴积液DLBCL样本中迁移/侵袭相关通路(包括B细胞受体(BCR)、核因子κB(NFκB)、 Toll样受体(TLR)等)的基因累积评分显著高于无积液样本,伴积液组平均评分>0.4,而无积液组多数基因评分<0.2;筛选出MUC4、SLC35G6、ARAP3等7个在至少5例伴积液样本中存在致病性突变的基因。
3.3 通路富集与分子机制解析
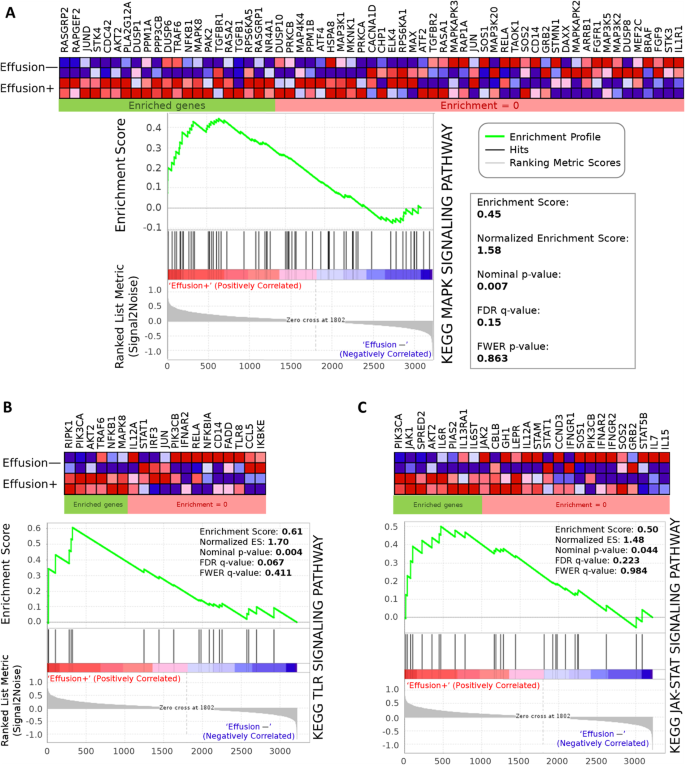
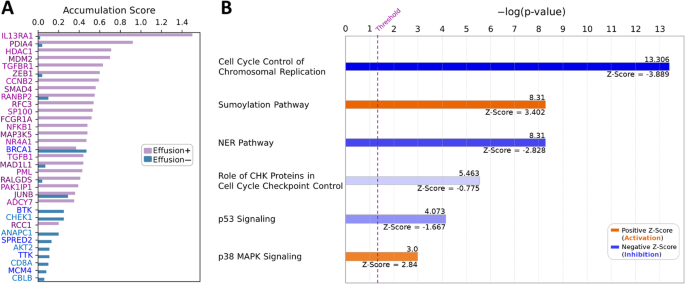
实验目的是解析伴积液DLBCL的核心通路异常,揭示积液形成的分子机制。方法细节:对基因芯片数据进行基因集富集分析(GSEA)和Ingenuity通路分析(IPA),对比伴积液与无积液样本的基因表达差异,筛选显著富集的通路。结果解读:GSEA结果显示,伴积液样本中MAPK、TLR、JAK-STAT等通路显著激活;IPA分析显示SUMOylation和p38 MAPK通路处于激活状态,而p53信号通路、细胞周期检查点控制通路等被抑制,提示这些通路的异常可能参与了淋巴瘤细胞的迁移侵袭与积液形成过程。
3.4 细胞系与临床队列验证
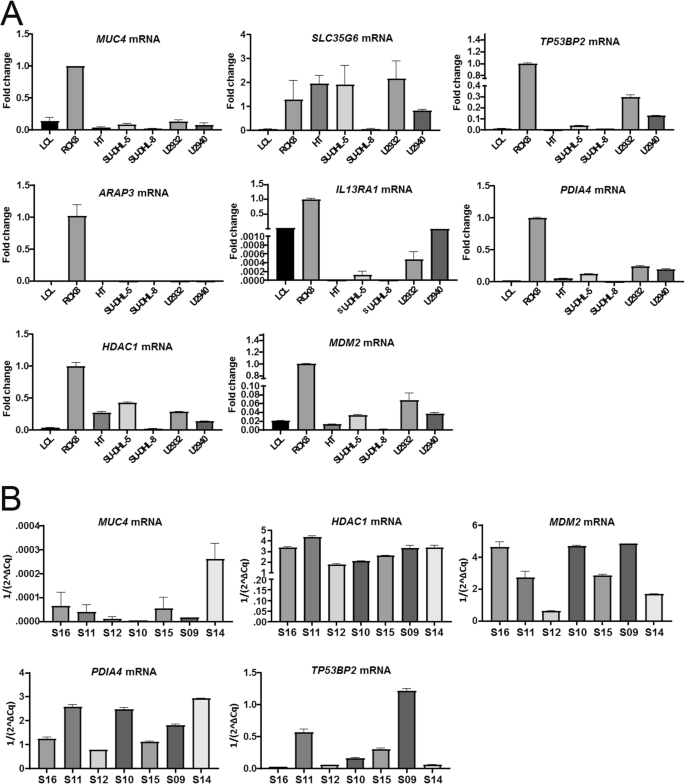
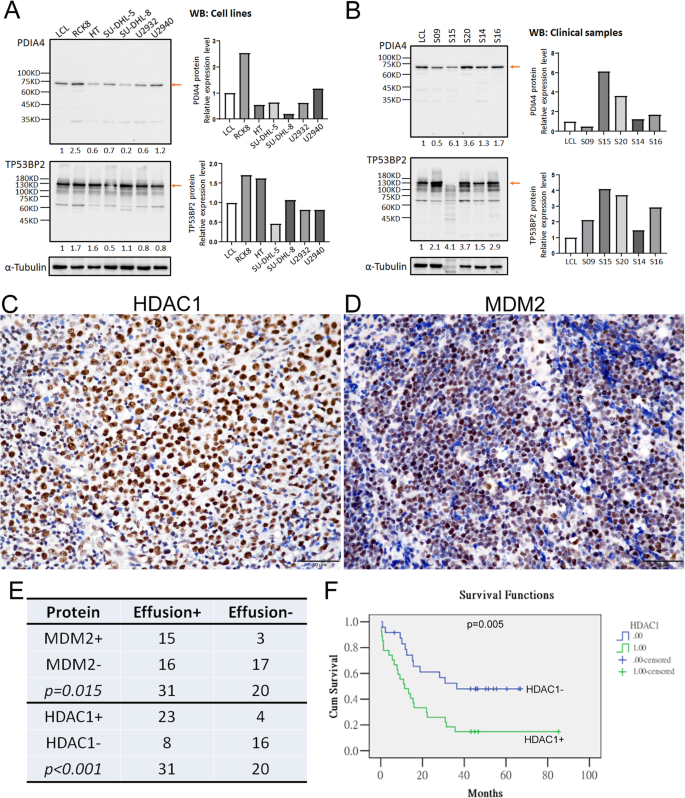
实验目的是验证候选基因的表达水平及临床意义。方法细节:采用实时定量PCR(qRT-PCR)检测8个候选基因(MUC4、SLC35G6、TP53BP2等)在DLBCL细胞系和临床样本中的mRNA表达;采用蛋白质免疫印迹(WB)检测PDIA4、TP53BP2的蛋白表达;在51例独立临床队列(31例伴积液、20例无积液)中,采用免疫组化(IHC)检测MUC4、HDAC1、MDM2的蛋白表达,并通过Kaplan-Meier生存分析评估基因表达与预后的关联。结果解读:qRT-PCR结果显示HDAC1、MDM2等基因在DLBCL细胞系和临床样本中呈高表达;IHC结果显示HDAC1和MDM2过表达与淋巴瘤性积液的存在显著相关(P<0.05),且HDAC1过表达与患者最差预后相关(P=0.005);WB结果验证了PDIA4、TP53BP2在DLBCL细胞系和临床样本中的高表达。实验所用关键产品:TaqMan qRCR引物探针、RIPA裂解液、抗HDAC1抗体(1:400, 4E1, GeneTex)、抗MDM2抗体(1:100, IF2, Invitrogen)。
4. Biomarker研究及发现成果
本研究鉴定的HDAC1、MDM2为伴淋巴瘤性积液DLBCL的潜在预后生物标志物,筛选与验证逻辑为“全外显子测序筛选高突变基因→通路富集分析锁定核心基因→独立临床队列免疫组化验证”。
生物标志物的来源为51例DLBCL临床组织样本(伴积液n=31,无积液n=20);验证方法为免疫组化染色,HDAC1阳性定义为≥50%的肿瘤细胞核染色,MDM2阳性定义为≥10%的肿瘤细胞核染色;HDAC1过表达在伴积液样本中的阳性率显著高于无积液样本(文献未明确具体数值,基于图表趋势推测),ROC曲线相关数据未提供。核心成果提炼:HDAC1和MDM2过表达与DLBCL淋巴瘤性积液的存在显著相关,其中HDAC1过表达与患者最差预后相关(P=0.005);首次明确伴积液DLBCL的分子致病机制与TP53-MDM2通路及HDAC相关染色质重塑机制密切相关,HDAC1和MDM2可作为这类患者的预后分层标志物,同时为HDAC抑制剂、MDM2抑制剂的应用提供了理论依据。
