1. 领域背景与文献引入
文献英文标题:Risk factors for immune-related adverse events: what have we learned and what lies ahead?;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤免疫治疗(免疫检查点抑制剂相关不良事件)
领域共识:免疫检查点抑制剂(ICIs)是肿瘤免疫治疗的核心突破,自2011年伊匹木单抗获批用于黑色素瘤治疗以来,已成为黑色素瘤、非小细胞肺癌、膀胱癌等多种晚期恶性肿瘤的标准治疗方案,其通过阻断PD-1/PD-L1、CTLA-4等免疫负调控通路,重新激活机体抗肿瘤免疫应答,显著延长了晚期肿瘤患者的生存时间。然而,ICIs在带来显著生存获益的同时,其诱导的免疫相关不良事件(irAEs)成为临床应用的主要瓶颈。irAEs可累及全身多个器官系统,从轻微的皮疹、瘙痒到严重的心肌炎、肺炎等,部分不良反应难以预测,甚至可导致永久器官损伤或死亡。当前领域的核心未解决问题包括:irAEs的精准发生机制尚未完全阐明,缺乏可用于临床的有效预测生物标志物,不同患者irAEs的个体差异机制不明。针对这些空白,本文通过系统回顾已发表的基础与临床研究,全面总结irAEs的潜在发生机制及各类风险因素,为irAEs的早期预测、临床管理及未来研究方向提供依据。
2. 文献综述解析
本文作为一篇系统性综述,以“ICIs安全性-irAEs机制-风险因素-未来方向”为核心逻辑框架,将现有研究按机制类型、风险因素类别进行分类整合,全面梳理了irAEs领域的研究进展与未解决问题。
现有研究的关键结论主要涵盖三个层面:一是不同类型ICIs的irAEs特征存在差异,CTLA-4抑制剂的irAEs发生率更高、严重程度更重,PD-1/PD-L1抑制剂的irAEs相对温和且器官累及谱不同,联合治疗会显著增加irAEs的发生率与严重程度;二是irAEs的发生机制涉及免疫耐受打破、交叉抗原呈递、表位扩散、B细胞与自身抗体介导的免疫损伤等多个维度,肠道菌群与遗传因素也参与其中;三是irAEs的风险因素包括临床病理与人口学特征、治疗方式、合并用药、自身抗体、细胞因子、血细胞、肠道菌群及遗传变异等多类因素。现有研究的优势在于从基础到临床多维度覆盖了irAEs的研究内容,为后续研究提供了全面的证据基础;局限性则体现在多数研究为回顾性分析,样本量与研究设计存在异质性,缺乏大样本前瞻性研究验证,且各类风险因素的交互作用尚未明确,生物标志物的临床转化仍处于探索阶段。本文的创新价值在于首次系统整合了irAEs的发生机制与全类别风险因素的研究证据,明确指出了当前领域的核心挑战,如生物标志物的前瞻性验证、不同风险因素的交互作用分析等,为irAEs的临床管理与未来研究提供了清晰的方向。
3. 研究思路总结与详细解析
本文的整体研究目标是全面阐述irAEs的发生机制与风险因素,为临床预测和管理irAEs提供循证依据;核心科学问题是明确irAEs的关键发生机制及可用于临床的潜在风险因素;技术路线逻辑为“临床需求引入-机制系统解析-风险因素分类总结-未来方向展望”的闭环,通过系统回顾已发表的基础研究、临床研究及meta分析,整合各类证据形成综合性结论。
3.1 ICIs安全性概况梳理
实验目的:明确不同类型ICIs的irAEs发生率、严重程度及时间特征,为后续机制与风险因素分析奠定基础;
方法细节:系统回顾已发表的III期临床试验、meta分析及临床研究数据,对比CTLA-4抑制剂、PD-1/PD-L1抑制剂及联合治疗的irAEs差异;
结果解读:CTLA-4抑制剂(如伊匹木单抗)的任意级别irAEs发生率可达65%,3级及以上irAEs发生率为5-30%(文献未明确提供样本量),多在治疗启动后8-12周出现,皮肤不良反应通常最早发生;PD-1/PD-L1抑制剂的任意级别irAEs发生率为13-40%,3级及以上约10%(文献未明确提供样本量),多在治疗前6个月内出现,内分泌系统、肺部不良反应较为常见;ICIs联合治疗的irAEs发生率与严重程度显著升高,其中肠道是最常受累的器官(发生率17%,文献未明确提供样本量),其次为皮肤、肝脏及内分泌系统;
产品关联:文献未提及具体实验产品,领域常规使用临床数据统计分析软件、文献管理工具等类试剂/仪器。
3.2 irAEs发生机制解析
实验目的:阐明irAEs的潜在免疫机制,为风险因素与生物标志物研究提供理论基础;
方法细节:整合基础研究(基因敲除小鼠模型、细胞实验)、临床前转化研究及临床病例分析的证据,梳理irAEs的核心发生路径;
结果解读:提出四大核心机制:一是免疫耐受打破,CTLA-4抑制剂主要在淋巴结早期阻断T细胞抑制信号,PD-1/PD-L1抑制剂主要在组织晚期调控活化T细胞,两者均导致自身反应性T细胞活化;二是B细胞与自身抗体介导的损伤,PD-1阻断可增强B细胞活化与增殖,诱导自身抗体产生,部分患者基线自身抗体与irAEs独立相关;三是交叉抗原呈递,肿瘤与正常组织共享抗原导致T细胞交叉识别并攻击正常组织,如黑色素瘤患者接受ICIs治疗后出现白癜风的病例支持该机制;四是表位扩散,免疫治疗诱导的炎症导致T细胞识别更多自身抗原表位,扩大免疫损伤范围。此外,肠道菌群通过调节免疫稳态影响irAEs发生,遗传变异则影响个体免疫应答的敏感性。文中配有机制示意图直观展示各类机制的交互作用:
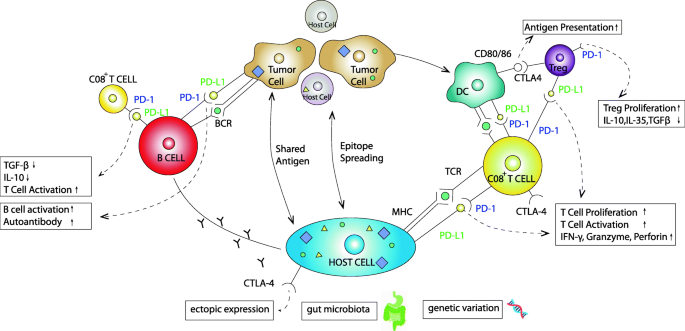
产品关联:文献未提及具体实验产品,领域常规使用基因敲除小鼠模型、流式细胞术、免疫组化(IHC)、TCR测序等类试剂/仪器。
3.3 临床病理与人口学风险因素总结
实验目的:评估临床病理与人口学特征对irAEs发生风险的影响;
方法细节:回顾已发表的临床研究与meta分析数据,分析性别、肿瘤组织学、合并疾病、体成分等因素与irAEs的相关性;
结果解读:女性患者irAEs发生率显著高于男性,推测:该差异可能与性激素对免疫系统的调节作用及性染色体相关的免疫遗传差异有关;不同肿瘤组织学类型的irAEs谱存在差异,黑色素瘤患者的皮肤、胃肠道irAEs发生率高于非小细胞肺癌,而非小细胞肺癌患者的肺炎发生率更高;合并自身免疫病的患者接受ICIs治疗后,irAEs或原有自身免疫病加重的发生率为30-75%(文献未明确提供样本量),但多数不良反应可通过激素治疗控制;肌肉减少症(低肌肉衰减度)与高级别irAEs风险升高相关,而肥胖与irAEs发生率无显著关联;
产品关联:文献未提及具体实验产品,领域常规使用体成分分析设备、临床电子病历系统等类试剂/仪器。
3.4 治疗相关风险因素分析
实验目的:明确不同治疗方式、合并用药对irAEs发生风险的影响;
方法细节:回顾联合治疗、序贯治疗、合并用药的临床研究数据,分析治疗策略与irAEs的相关性;
结果解读:放疗联合ICIs的irAEs风险存在争议,部分研究显示高剂量放疗会增加irAEs风险,且不良反应可能出现在放疗野之外;靶向治疗与ICIs联合或序贯时,部分组合会显著增加毒性,如奥希替尼序贯PD-1抑制剂会导致严重间质性肺炎风险升高,且治疗顺序是关键影响因素,在PD-1抑制剂治疗后3个月内启动奥希替尼的患者风险最高;合并使用质子泵抑制剂、非甾体类抗炎药可能增加急性间质性肾炎风险,抗生素使用则与ICIs诱导的结肠炎风险升高相关;
产品关联:文献未提及具体实验产品,领域常规使用各类抗肿瘤药物、临床不良反应监测系统等类试剂/仪器。
3.5 生物标志物类风险因素总结
实验目的:探索可用于预测irAEs的潜在生物标志物;
方法细节:回顾细胞因子检测、自身抗体检测、血细胞分析、TCR库测序等研究数据,分析各类生物标志物与irAEs的相关性;
结果解读:细胞因子方面,基线IL-17水平升高与伊匹木单抗诱导的3级结肠炎风险相关,基线IL-6水平降低及治疗后IL-6水平升高与irAEs风险相关;自身抗体方面,基线抗甲状腺抗体阳性的患者接受帕博利珠单抗治疗时,甲状腺功能障碍发生率为80%,显著高于抗体阴性患者的8%(文献未明确提供样本量,P<0.05);血细胞方面,基线嗜酸性粒细胞计数升高、治疗后淋巴细胞计数降低与irAEs风险升高相关,TCR库多样性增加也与irAEs风险相关;可溶性蛋白方面,治疗后可溶性CD163水平升高、基线sCTLA-4水平升高与irAEs风险相关;
产品关联:文献未提及具体实验产品,领域常规使用ELISA、qRT-PCR、流式细胞术、TCR测序等类试剂/仪器。
3.6 肠道菌群与遗传变异风险因素探讨
实验目的:分析肠道菌群与遗传因素对irAEs发生的调控作用;
方法细节:回顾肠道菌群宏基因组测序、基因多态性分析的研究证据,探索菌群组成与遗传变异对irAEs的影响;
结果解读:肠道菌群方面,基线肠道菌群中Faecalibacterium等厚壁菌门富集与伊匹木单抗诱导的结肠炎风险升高相关,而拟杆菌门富集则与结肠炎风险降低相关;遗传变异方面,HLA-DR4基因型与ICIs诱导的1型糖尿病相关,PDCD1基因多态性(rs2227981)纯合子与非小细胞肺癌患者irAEs风险降低相关(文献未明确提供样本量,P<0.05);
产品关联:文献未提及具体实验产品,领域常规使用肠道菌群宏基因组测序、SNP基因分型等类试剂/仪器。
4. Biomarker研究及发现成果解析
本文涉及的Biomarker覆盖细胞因子、自身抗体、可溶性蛋白、血细胞、肠道菌群及遗传变异六大类,筛选与验证逻辑基于已发表的回顾性临床研究、病例分析及部分前瞻性探索,为irAEs的预测提供了多维度的潜在靶点。
Biomarker定位:明确的Biomarker类型包括细胞因子(IL-17、IL-6、IL-10等)、自身抗体(抗甲状腺过氧化物酶抗体、抗甲状腺球蛋白抗体等)、可溶性蛋白(sCD163、sCTLA-4)、血细胞(嗜酸性粒细胞、淋巴细胞)、肠道菌群(Faecalibacterium等)、遗传多态性(HLA-DR4、PDCD1 rs2227981)。筛选与验证逻辑为:先通过基础研究明确潜在关联,再通过临床研究验证相关性,部分生物标志物已在特定肿瘤类型中显示出预测价值,但缺乏跨肿瘤类型的验证。
研究过程详述:自身抗体的验证主要通过ELISA检测患者治疗前后血清样本,结果显示基线抗甲状腺抗体阳性的非小细胞肺癌患者接受纳武利尤单抗治疗时,irAEs发生率显著升高,多因素分析显示其为irAEs的独立预测因子;细胞因子方面,通过流式细胞术或ELISA检测血清细胞因子水平,发现基线IL-17升高的黑色素瘤患者接受伊匹木单抗新辅助治疗时,3级结肠炎发生率显著升高;肠道菌群通过宏基因组测序分析基线粪便样本,发现厚壁菌门富集与伊匹木单抗诱导的结肠炎风险相关;遗传变异通过SNP基因分型检测,发现PDCD1 rs2227981纯合子的非小细胞肺癌患者接受纳武利尤单抗治疗时,irAEs风险显著降低。特异性与敏感性数据方面,多数研究未提供ROC曲线及对应的AUC、敏感性、特异性数值,仅报告了统计学相关性。
核心成果提炼:本文系统总结了多类Biomarker与irAEs的关联,其中基线自身抗体、细胞因子水平及肠道菌群组成具有潜在的临床预测价值;首次全面整合了遗传变异与肠道菌群对irAEs的调控作用,指出其在个体差异中的重要性;部分Biomarker的功能关联已被初步阐明,如抗甲状腺抗体与甲状腺irAEs直接相关,风险比HR值未明确(文献未提供);创新性在于从多维度梳理了irAEs的潜在Biomarker,为后续前瞻性研究提供了明确的靶点,但目前所有Biomarker均缺乏大样本前瞻性研究验证,临床应用仍不成熟。
