1. 领域背景与文献引入
文献英文标题:ZG16 promotes T-cell mediated immunity through direct binding to PD-L1 in colon cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:结直肠癌免疫治疗
结直肠癌是一类高度异质性的消化道恶性肿瘤,错配修复缺陷(dMMR)和微卫星高度不稳定(MSI-H)是其重要分子亚型,该亚型肿瘤因免疫检查点基因高表达,对PD-1/PD-L1免疫检查点抑制剂响应良好,已成为当前免疫治疗的核心方向之一。领域共识:PD-L1的活性调控涉及转录、翻译及翻译后修饰多个层面,其中N-糖基化修饰对PD-L1的蛋白稳定性及功能活性至关重要,靶向糖基化PD-L1的治疗策略是当前研究前沿。然而,现有研究仍存在核心空白,包括PD-L1翻译后调控的具体分子机制尚未完全阐明,部分结直肠癌患者对现有免疫治疗存在耐药性,缺乏新的免疫调控靶点及可直接递送的蛋白类免疫治疗药物。前期研究已发现胰酶原颗粒蛋白16(ZG16)与结直肠癌中PD-L1表达呈负相关,且ZG16可阻断PD-L1的表达,但该调控作用的分子机制尚未明确,因此本研究旨在阐明ZG16调控PD-L1的具体机制,并验证其在结直肠癌免疫治疗中的潜在应用价值,为领域提供新的免疫治疗靶点及策略。
2. 文献综述解析
作者围绕PD-L1的调控机制及ZG16的已知功能构建综述逻辑,将现有研究分为PD-1/PD-L1免疫治疗的临床应用、PD-L1的翻译后调控机制、ZG16的结构与功能三类进行评述。现有研究显示,PD-1/PD-L1免疫检查点抑制剂在dMMR/MSI-H结直肠癌患者中展现出显著疗效,其作用机制与肿瘤组织中高表达的PD-1、PD-L1、CTLA-4等免疫检查点基因相关;PD-L1的活性受N-糖基化修饰调控,靶向糖基化PD-L1的单克隆抗体可阻断其与PD-1的结合,并诱导PD-L1蛋白降解;ZG16是一种主要在黏液分泌细胞中高表达的分泌蛋白,具有Jacalin样凝集素结构域,前期研究发现其与结直肠癌中PD-L1表达负相关,但不影响PD-L1的转录水平,调控机制未知。现有研究的局限性在于,缺乏对ZG16调控PD-L1的分子机制的深入阐明,也未明确ZG16对T细胞免疫功能的直接调控作用,无法为其临床应用提供理论依据。本研究的创新价值在于,首次发现ZG16通过凝集素结构域直接结合糖基化PD-L1并促进其降解,同时可直接调控T细胞上的免疫检查点分子表达,激活T细胞介导的抗肿瘤免疫,弥补了现有研究在ZG16功能及PD-L1调控机制方面的空白。
3. 研究思路总结与详细解析
本研究的核心目标是阐明ZG16调控PD-L1的分子机制及在结直肠癌免疫治疗中的作用,核心科学问题包括ZG16与PD-L1的相互作用方式、依赖结构域,以及ZG16对T细胞免疫的调控作用,技术路线遵循“假设提出→细胞实验验证→动物模型验证→临床应用潜力评估”的闭环逻辑。
3.1 ZG16与PD-L1相互作用的分子机制验证
实验目的:验证ZG16与PD-L1的直接结合作用,明确该结合是否依赖ZG16的凝集素结构域及PD-L1的糖基化修饰。方法细节:构建带有Flag标签的ZG16过表达质粒和带有His标签的PD-L1过表达质粒,共转染至SW480和HCT116结直肠癌细胞系,采用免疫共沉淀实验检测两者的结合;构建ZG16凝集素结构域突变体(D151A单突变、M5多突变)及PD-L1糖基化缺失突变体(4NQ,4个糖基化位点突变),共转染后进行免疫共沉淀实验验证结合的依赖性;同时采用免疫荧光共定位实验在细胞内直观验证两者的结合。结果解读:免疫共沉淀实验结果显示,ZG16与PD-L1在两种结直肠癌细胞系中均存在直接结合,免疫荧光共定位实验也证实了细胞内的共定位;当ZG16的凝集素结构域引入突变后,其与PD-L1的结合显著降低;当PD-L1的糖基化位点突变后,与ZG16的结合同样显著降低,表明ZG16通过其凝集素结构域特异性结合糖基化修饰的PD-L1。
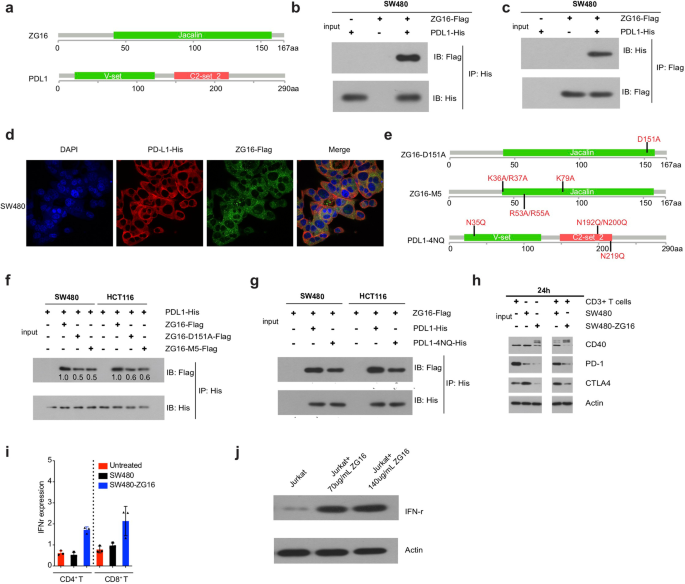
产品关联:文献未提及具体实验产品,领域常规使用免疫共沉淀试剂盒、Flag/His标签抗体、免疫荧光染色试剂等。
3.2 ZG16对T细胞免疫功能的调控作用验证
实验目的:探究ZG16对T细胞上免疫检查点分子表达及活化状态的影响。方法细节:将过表达ZG16的SW480细胞与原代CD3+T细胞共培养不同时间点,采用蛋白质免疫印迹检测CD40、PD1、CTLA4的表达水平,通过流式细胞术检测CD4+和CD8+T细胞中干扰素-γ(IFN-γ)的表达;同时使用纯化的ZG16蛋白处理Jurkat细胞48小时,检测PD1、CTLA4的表达及IFN-γ水平。结果解读:蛋白质免疫印迹结果显示,共培养后T细胞中PD1和CTLA4的表达显著降低,CD40出现新的异构体;流式细胞术结果显示,CD4+和CD8+T细胞中IFN-γ的水平显著升高,表明T细胞被激活;Jurkat细胞经ZG16蛋白处理后,PD1和CTLA4的表达显著降低,IFN-γ表达显著升高,进一步验证了ZG16对T细胞免疫的激活作用。产品关联:文献未提及具体实验产品,领域常规使用流式细胞术抗体、蛋白质免疫印迹试剂、细胞培养试剂等。
3.3 ZG16体内抑瘤效果及联合化疗作用验证
实验目的:验证ZG16在体内的抗肿瘤作用,以及与化疗药物的协同效果,同时评估ZG16蛋白递送的临床应用潜力。方法细节:构建过表达ZG16的CT26和MC38结直肠癌细胞系,分别皮下接种至BALB/c和C57BL/6小鼠,建立同源肿瘤模型,监测肿瘤生长35天和30天;对MC38模型分别给予PBS、5-氟尿嘧啶(5-FU)化疗、ZG16蛋白单独处理及联合处理,监测肿瘤生长;采用免疫组化检测肿瘤组织中CD3、PD-L1、PD1的表达。结果解读:体内实验结果显示,ZG16过表达显著抑制CT26肿瘤生长,肿瘤体积显著小于对照组(n=6,P<0.01);免疫组化结果显示,ZG16过表达的肿瘤组织中CD3+T细胞增多,PD-L1和PD1的表达显著降低;ZG16过表达与5-FU联合处理对MC38肿瘤生长的抑制作用显著强于单药处理(n=3,P<0.001);ZG16蛋白经尾静脉注射后,可显著抑制MC38肿瘤生长,表明ZG16可作为蛋白药物递送。
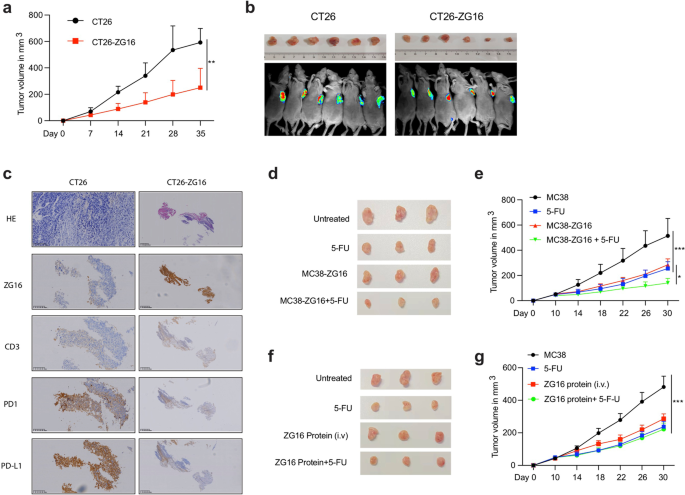
产品关联:文献未提及具体实验产品,领域常规使用动物造模试剂、化疗药物5-氟尿嘧啶、免疫组化试剂等。
4. Biomarker研究及发现成果
本研究中涉及的Biomarker为ZG16,属于免疫调控分子,其筛选与验证逻辑基于前期临床样本发现的ZG16与PD-L1的负相关关系,通过细胞实验、动物实验及蛋白递送实验逐步验证其功能及机制。ZG16主要来源于结直肠黏液分泌细胞,在结直肠癌患者肿瘤组织中与PD-L1表达呈负相关;通过细胞实验验证,ZG16通过凝集素结构域特异性结合糖基化PD-L1,促进其降解;通过T细胞共培养和Jurkat细胞实验验证,ZG16可抑制T细胞上PD1和CTLA4的表达,激活T细胞,提高IFN-γ的表达水平;体内实验显示,ZG16过表达可显著抑制肿瘤生长,与化疗药物联合应用时抑瘤效果更显著,且ZG16蛋白递送可有效抑制肿瘤生长。
核心成果提炼:ZG16可作为潜在的免疫检查点抑制剂,通过双重机制发挥抗肿瘤免疫作用,一方面直接结合糖基化PD-L1促进其降解,阻断PD-1/PD-L1通路,另一方面抑制T细胞上PD1和CTLA4的表达,解除T细胞免疫抑制;体内实验数据显示,CT26模型中ZG16过表达组肿瘤生长显著受抑(n=6,P<0.01),MC38模型中ZG16与5-FU联合处理组肿瘤生长抑制效果显著优于单药组(n=3,P<0.001);本研究首次阐明了ZG16调控PD-L1的分子机制,为结直肠癌免疫治疗提供了新的靶点,同时证明ZG16可作为蛋白药物递送,具有良好的临床应用潜力。
