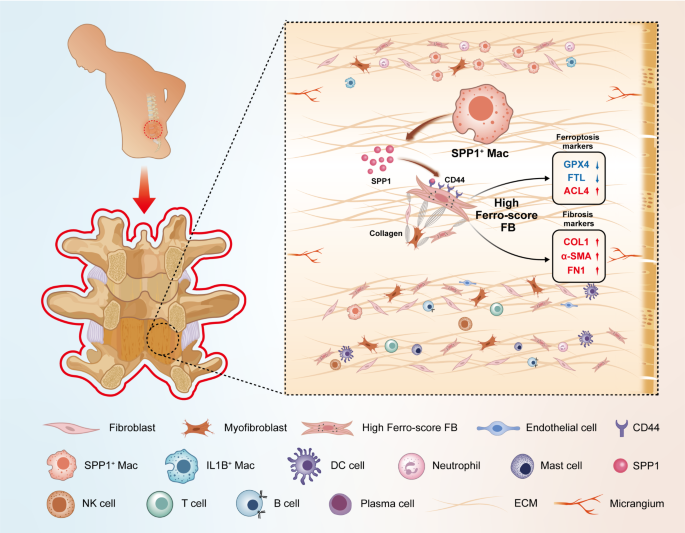
1. 领域背景与文献引入
文献英文标题:Single-cell multi-omics analysis identifies SPP1+ macrophages as key drivers of ferroptosis-mediated fibrosis in ligamentum flavum hypertrophy;发表期刊:Biomarker Research;影响因子:未公开;研究领域:脊柱退行性疾病(黄韧带肥厚纤维化机制研究)
黄韧带肥厚(LFH)是腰椎管狭窄(LSS)的主要病因之一,全球每年约1.03亿人受LSS相关症状困扰,严重影响生活质量并造成沉重的社会经济负担。现有研究已明确机械应力、慢性炎症、氧化应激是LFH纤维化进展的核心诱因,证实成纤维细胞向肌成纤维细胞转化是纤维化的细胞学基础,巨噬细胞浸润参与炎症信号激活,但LFH发生发展的细胞异质性及深层分子调控机制仍未完全阐明。近年来,单细胞转录组技术成为解析纤维化微环境细胞图谱的热点方向,但铁死亡(ferroptosis)这一铁依赖性非凋亡细胞死亡方式在LFH中的作用尚未被揭示,巨噬细胞亚群与成纤维细胞铁死亡的调控关系也缺乏系统研究。针对上述研究空白,本研究通过整合单细胞RNA测序(scRNA-seq)、bulk RNA测序、孟德尔随机化(MR)及临床/动物模型验证,系统解析LFH的纤维化微环境,揭示铁死亡及SPP1+巨噬细胞在LFH中的关键调控作用,为LFH的诊断和治疗提供新的靶点。
2. 文献综述解析
作者从细胞类型异质性、分子机制、技术方法三个维度对LFH领域现有研究进行分类评述,系统梳理了成纤维细胞转化、巨噬细胞浸润、机械应力与炎症信号通路等核心研究方向的进展与局限性。
现有研究的关键结论集中在成纤维细胞功能异常与纤维化的关联,证实成纤维细胞在机械应力刺激下可分化为肌成纤维细胞,大量分泌胶原蛋白等细胞外基质(ECM)成分,推动LFH进展;同时,巨噬细胞浸润被认为是LFH炎症反应的核心触发因素,可通过分泌细胞因子激活成纤维细胞。技术方法层面,传统bulk测序可揭示整体基因表达变化,动物模型(如双足站立小鼠模型)可模拟LFH的机械应力诱因,但这些方法无法解析细胞水平的异质性,难以区分不同细胞亚群的功能差异。现有研究的局限性主要体现在三个方面:一是缺乏单细胞水平的LFH细胞图谱,无法明确成纤维细胞、巨噬细胞等细胞的亚群功能异质性;二是未关注铁死亡这一新型细胞死亡方式在LFH中的作用,铁代谢紊乱与LFH的因果关系尚未验证;三是巨噬细胞亚群与成纤维细胞的具体调控通路仍不明确,缺乏多组学整合的系统分析。本研究的创新价值在于首次将单细胞多组学与孟德尔随机化结合,解析LFH的铁死亡调控机制,鉴定出SPP1+巨噬细胞这一新型促纤维化亚群,揭示其通过SPP1-CD44轴调控成纤维细胞铁死亡的分子通路,填补了LFH领域在细胞异质性与铁死亡机制研究中的空白。
3. 研究思路总结与详细解析
本研究的整体研究目标是系统解析LFH纤维化的细胞异质性与分子调控机制,核心科学问题是铁死亡如何参与LFH纤维化进程,以及巨噬细胞亚群对成纤维细胞铁死亡的调控作用,技术路线遵循“临床样本单细胞图谱构建→多组学整合分析铁死亡机制→孟德尔随机化验证因果关系→临床与动物模型功能验证→细胞互作通路解析”的闭环逻辑,通过多维度实验验证揭示SPP1+巨噬细胞的关键驱动作用。
3.1 临床样本收集与单细胞RNA测序实验
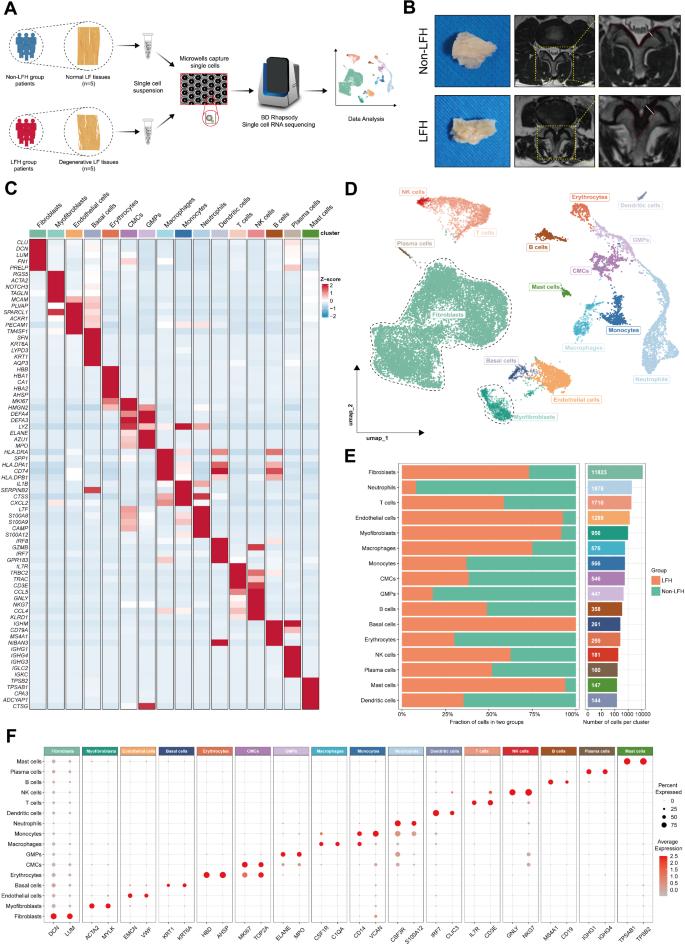
实验目的是构建正常与肥厚黄韧带组织的单细胞转录组图谱,解析LFH中的细胞组成与比例变化。方法细节:本研究共纳入26例临床样本,其中13例腰椎间盘突出症(LDH)患者的非LFH黄韧带组织(厚度≤3.74mm),13例腰椎管狭窄(LSS)患者的LFH组织(厚度>3.74mm);选取其中10例样本(5例非LFH、5例LFH)进行scRNA-seq,采用BD Rhapsody™ Express单细胞分析系统分离单细胞,合成cDNA并构建文库,经Agilent 2100 Bioanalyzer和Qubit Fluorometer质控后,用Illumina HiSeq X Ten测序仪完成测序;测序数据经Seurat软件预处理,过滤低质量细胞后保留21301个细胞进行聚类分析。结果解读:UMAP聚类分析得到21个细胞簇,共鉴定出16种主要细胞类型,其中成纤维细胞、肌成纤维细胞、巨噬细胞在LFH组中的比例显著高于非LFH组(成纤维细胞占比从55.5%升至62.3%,巨噬细胞占比从2.7%升至3.1%,n=5,P<0.05),提示这些细胞类型在LFH纤维化中发挥核心作用。实验所用关键产品:BD Rhapsody™ Express单细胞分析系统、BD Human Single-Cell Multiplexing Kit(#633781)、BD Rhapsody Whole Transcriptome Analysis(WTA)Reagent Kit(#633801)、Agilent 2100 Bioanalyzer、Qubit dsDNA HS Assay Kit(#Q32854)、Illumina HiSeq X Ten测序仪。
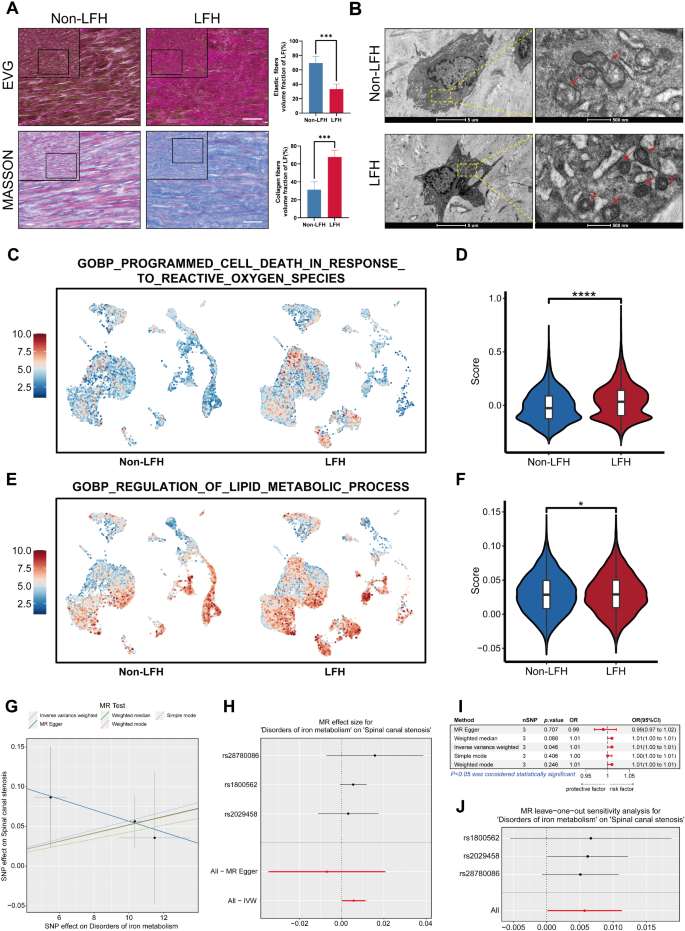
3.2 铁死亡在LFH中的作用验证
实验目的是验证铁死亡是否为LFH纤维化的风险因素,并明确其分子特征。方法细节:对临床样本进行组织学染色(EVG、Masson)和透射电镜(TEM)观察,检测铁离子水平;通过单细胞基因集评分分析ROS和脂质代谢通路活性;采用孟德尔随机化(MR)分析铁代谢紊乱与LFH的因果关系(因LFH无GWAS数据,用脊柱管狭窄(SCS)替代)。结果解读:组织学染色显示LFH组弹性纤维比例显著降低(从78.2%降至32.5%,n=5,P<0.001),胶原蛋白比例显著升高(从21.8%升至67.5%,n=5,P<0.001);TEM观察到LFH组线粒体出现铁死亡特征性改变:线粒体皱缩、膜密度增加、嵴减少或消失;铁离子水平检测显示LFH组铁离子含量显著高于非LFH组(n=5,P<0.05);单细胞基因集评分显示LFH组ROS评分(P<0.05)和脂质代谢评分(P<0.0001)显著高于非LFH组;MR分析采用逆方差加权(IVW)法,结果显示铁代谢紊乱与SCS存在正因果关系(OR=1.01,95%CI 1.00-1.01,P=0.046),敏感性分析证实结果稳定无异质性。实验所用关键产品:Ferrous Ion Content Assay Kit(BC5415,Solarbio)、Tecnai G2 Spirit透射电镜、EVG染色试剂盒(B1053,Baiqiandu)、Masson三色染色试剂盒(B1011,Baiqiandu)。
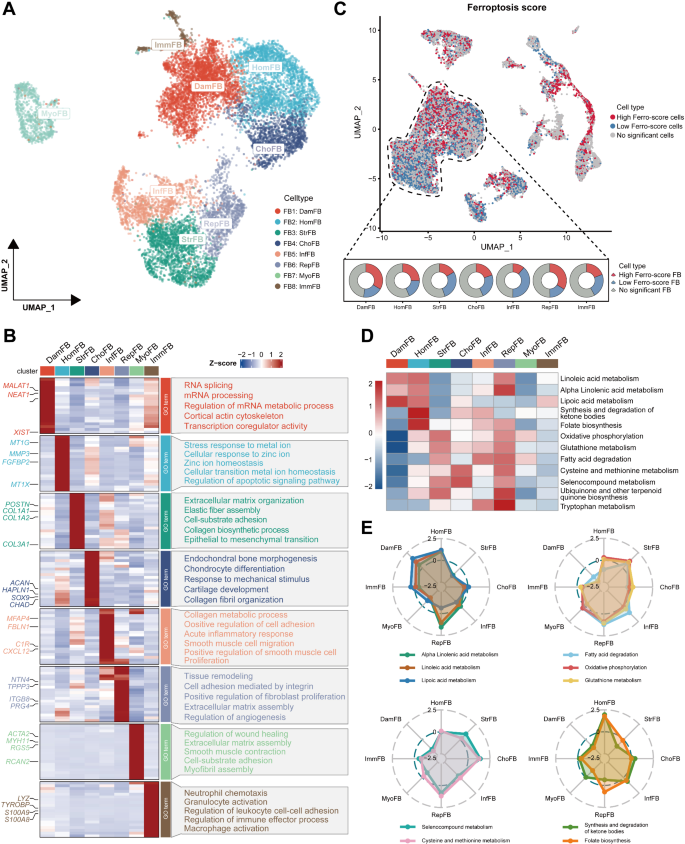
3.3 成纤维细胞亚群功能异质性与铁死亡分析
实验目的是解析成纤维细胞亚群的功能差异,明确铁死亡与成纤维细胞功能的关联。方法细节:对成纤维细胞(含肌成纤维细胞)进行亚群聚类,得到8个亚群;通过GO富集、GSVA、scMetabolism分析各亚群的功能与代谢通路活性;基于铁死亡促进/抵抗基因表达进行铁死亡评分,将成纤维细胞分为高、低、无显著铁死亡评分三类。结果解读:8个成纤维细胞亚群分别为受损成纤维细胞(DamFB)、稳态相关成纤维细胞(HomFB)、结构成纤维细胞(StrFB)、软骨形成成纤维细胞(ChoFB)、炎症相关成纤维细胞(InfFB)、修复相关成纤维细胞(RepFB)、肌成纤维细胞(MyoFB)、免疫相关成纤维细胞(ImmFB);铁死亡评分显示DamFB和RepFB中高铁死亡评分成纤维细胞(High Ferro-score FB)占比最高(分别为42.3%和38.7%);代谢通路分析显示DamFB的铁死亡促进通路(如α-亚麻酸代谢、亚油酸代谢)活性最高,而铁死亡抵抗通路(如谷胱甘肽代谢、脂肪酸降解)活性最低;伪时间分析显示成纤维细胞从StrFB分化为DamFB,LFH组中铁死亡促进基因表达随伪时间持续升高,而铁死亡抵抗基因表达持续降低(n=5,P<0.001)。
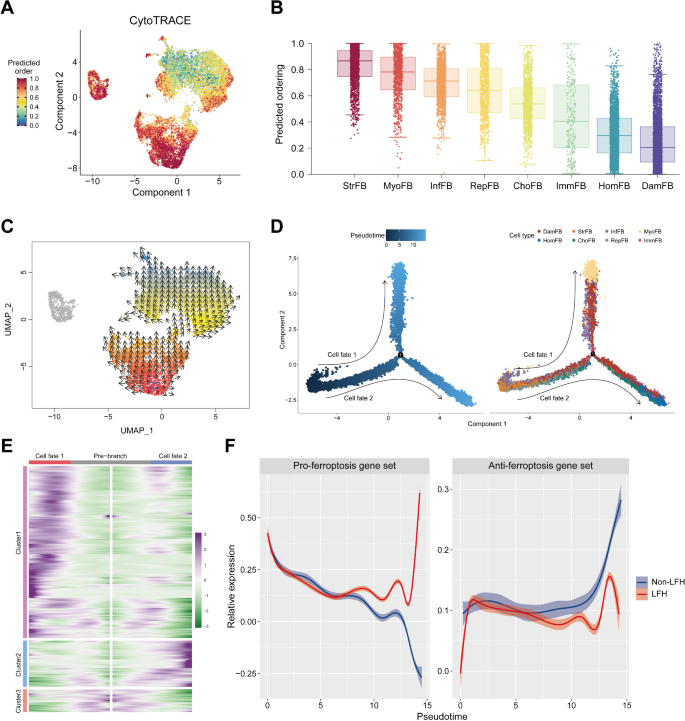
3.4 巨噬细胞亚群鉴定与功能分析
实验目的是解析单核吞噬细胞的亚群异质性,鉴定LFH中富集的巨噬细胞亚群并分析其功能。方法细节:对单核吞噬细胞(包括单核细胞、巨噬细胞、树突状细胞等)进行重新聚类,得到8个亚群;通过GSVA分析各亚群的功能通路,结合免疫组化(IHC)验证关键标志物的表达。结果解读:鉴定出SPP1+巨噬细胞(SPP1+ Mac)这一亚群,在LFH组中的比例显著高于非LFH组(从12.5%升至32.7%,n=5,P<0.001);功能分析显示SPP1+ Mac表现为M2型巨噬细胞表型,高表达CD163、MRC1(CD206)等M2标志物,富集纤维化相关通路(如ECM结合、胶原蛋白结合)及铁代谢通路(如铁离子转运、亚铁结合);IHC验证显示LFH组SPP1、CD206的阳性表达率显著高于非LFH组(SPP1:18.2% vs 45.6%,n=5,P<0.001;CD206:22.3% vs 51.2%,n=5,P<0.01)。
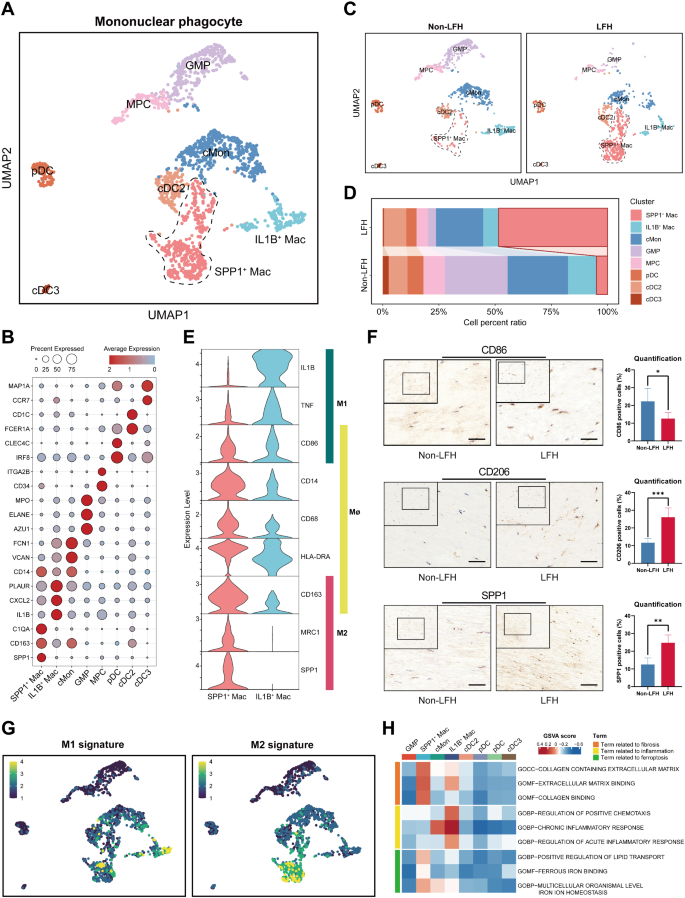
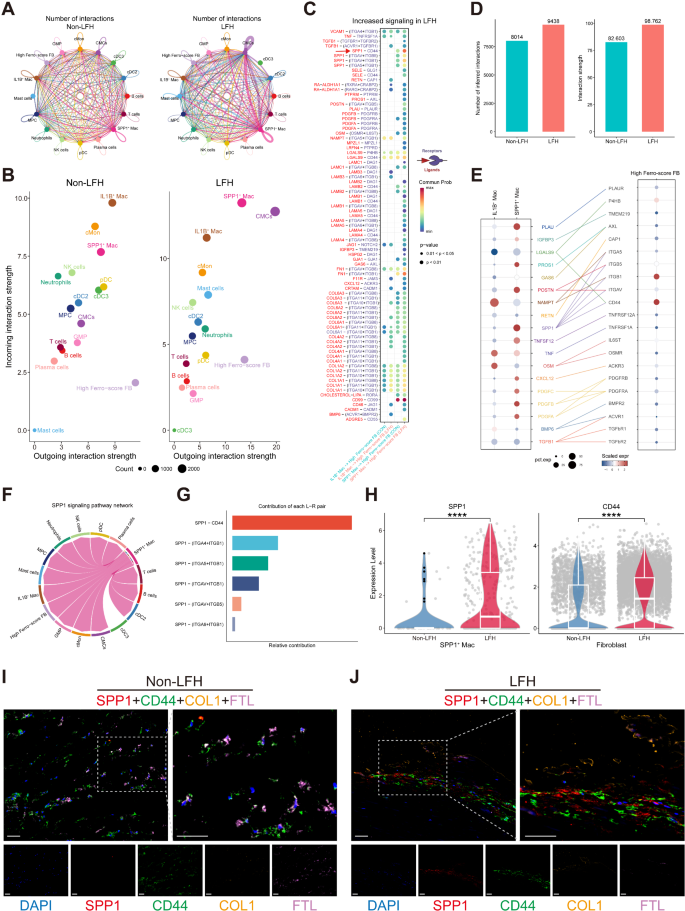
3.5 细胞互作与调控机制验证
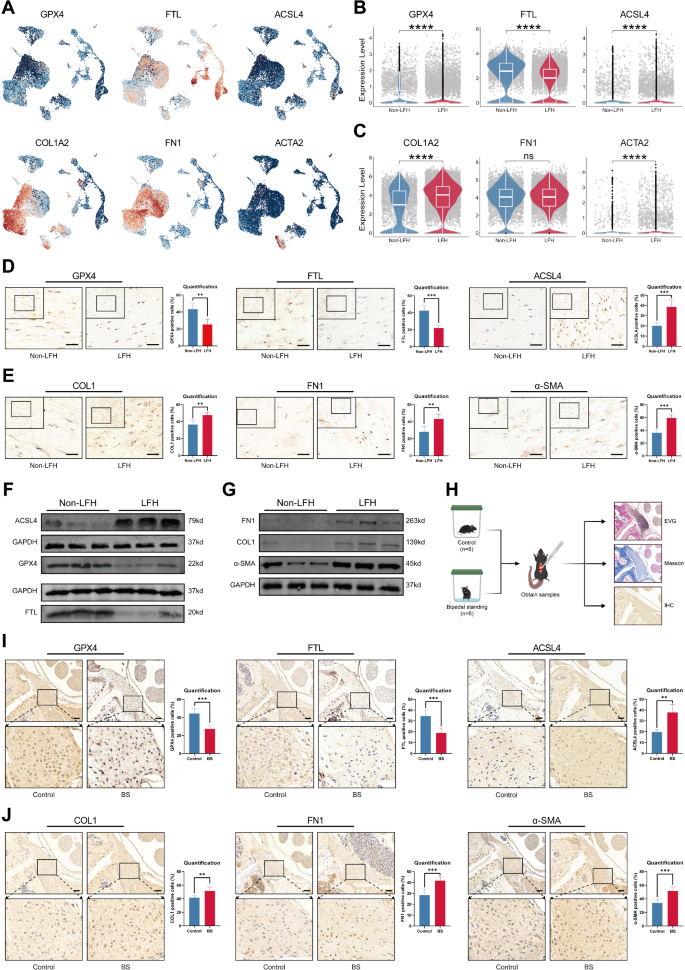
实验目的是解析SPP1+巨噬细胞与成纤维细胞的互作通路,验证其对成纤维细胞铁死亡的调控作用。方法细节:用CellChat软件分析LFH与非LFH组的细胞通讯网络,筛选关键配体-受体对;通过多重免疫荧光验证SPP1与CD44的共定位,以及铁死亡和纤维化标志物的表达;在双足站立(BS)小鼠模型中验证上述结果。结果解读:CellChat分析显示LFH组细胞通讯网络更复杂,SPP1+巨噬细胞的传入/传出通讯强度显著高于IL1B+巨噬细胞,成为LFH中的主要信号调控细胞;关键配体-受体对分析显示SPP1-CD44轴是SPP1+巨噬细胞与High Ferro-score FB的核心互作通路,LFH组中该通路的通讯概率显著升高(P<0.0001);多重免疫荧光显示LFH中SPP1与CD44共定位区域伴随COL1沉积增加(P<0.001)和FTL(铁死亡抵抗基因)表达降低(P<0.001);BS小鼠模型验证显示,模型组铁死亡标志物ACSL4表达升高(P<0.001),GPX4、FTL表达降低(P<0.001),纤维化标志物COL1、FN1、α-SMA表达显著升高(P<0.001),与临床样本结果一致。实验所用关键产品:SPP1抗体(#PB0589,Boster)、CD44抗体(#15675-1-AP,proteintech)、COL1抗体(#AF7001,Affinity)、FTL抗体(#DF6604,Affinity)。
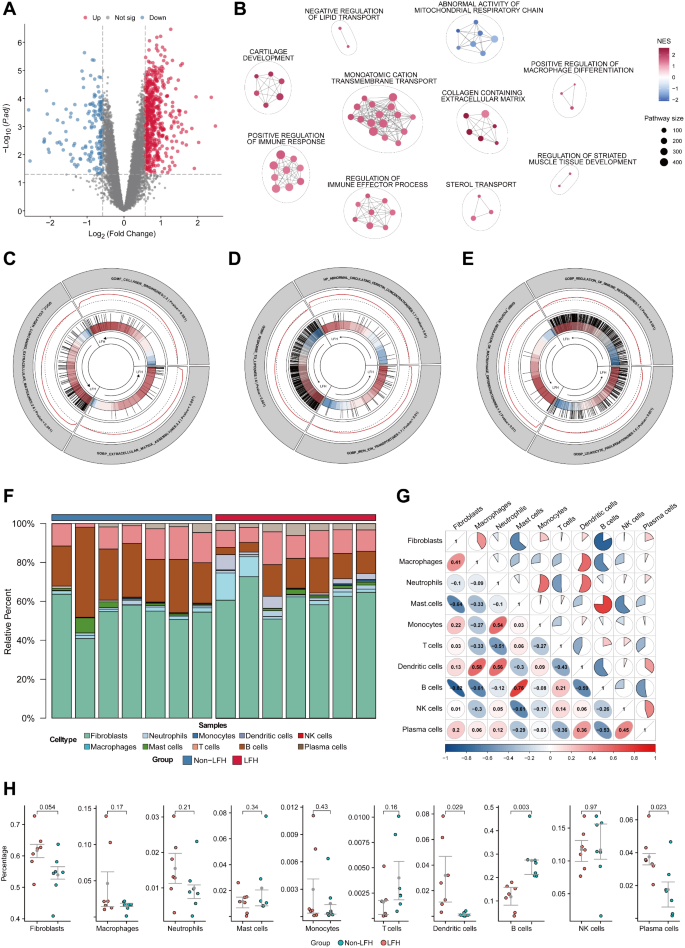
3.6 bulk RNA-seq与去卷积分析
实验目的是扩大样本量验证单细胞测序结果,明确细胞比例变化与基因表达的关联。方法细节:收集6例样本(3例非LFH、3例LFH)进行bulk RNA-seq,结合GEO数据集GSE113212(4例LFH、4例非LFH),去除批次效应后进行差异表达分析;用BayesPrism工具进行去卷积分析,推断细胞比例变化;通过Spearman相关分析细胞类型的关联。结果解读:差异表达分析共鉴定出711个差异基因,其中544个上调、167个下调,富集通路包括纤维化(胶原蛋白结合、ECM组装)、铁代谢(铁离子转运)、巨噬细胞分化(巨噬细胞分化正调控);去卷积分析显示LFH组成纤维细胞和巨噬细胞比例升高,Spearman相关分析显示成纤维细胞与巨噬细胞呈显著正相关(P<0.05),证实两者在LFH纤维化中的协同作用。
4. Biomarker研究及发现成果解析
本研究鉴定出两类与LFH纤维化相关的Biomarker:一是细胞型Biomarker——SPP1+巨噬细胞,二是分子型Biomarker——铁死亡相关基因(GPX4、FTL、ACSL4),通过“单细胞筛选→临床样本验证→动物模型验证→孟德尔随机化因果分析”的完整逻辑链条,证实其在LFH中的诊断与预后价值。
Biomarker定位方面,SPP1+巨噬细胞是LFH中富集的促纤维化巨噬细胞亚群,筛选逻辑为:通过scRNA-seq在单核吞噬细胞中鉴定出SPP1高表达的亚群,经bulk RNA-seq去卷积分析验证其比例在LFH中升高,再通过IHC和多重免疫荧光验证其与纤维化的关联;铁死亡相关基因(GPX4、FTL、ACSL4)作为分子Biomarker,筛选逻辑为:通过单细胞基因集评分发现铁死亡通路在LFH中富集,经临床样本IHC、Western blot验证其表达变化,动物模型进一步确认其与纤维化的关联。研究过程详述:SPP1+巨噬细胞来源于临床黄韧带组织,验证方法包括scRNA-seq、IHC、多重免疫荧光,其特异性表现为仅在LFH组织中显著富集,敏感性为LFH组比例是非LFH组的2.6倍(n=5,P<0.001);铁死亡相关基因的验证方法包括IHC、Western blot,其中GPX4在LFH组的表达水平为非LFH组的0.4倍(n=3,P<0.001),FTL为0.3倍(n=3,P<0.001),ACSL4为2.1倍(n=3,P<0.001);ROC曲线数据文献未明确提供,无法评估其诊断效能。核心成果提炼:SPP1+巨噬细胞作为LFH的新型促纤维化Biomarker,其功能关联为通过SPP1-CD44轴调控High Ferro-score FB的铁死亡,驱动纤维化进程,创新性在于首次在LFH中发现该巨噬细胞亚群的调控作用;铁死亡相关基因作为功能Biomarker,证实铁死亡是LFH的风险因素,孟德尔随机化分析显示铁代谢紊乱与LFH的风险比HR=1.01(95%CI 1.00-1.01,P=0.046);这些Biomarker为LFH的早期诊断和靶向治疗提供了新的候选靶点,具有重要的临床转化价值。