1. 领域背景与文献引入
文献英文标题:Therapeutic targeting of PFKFB3 and PFKFB4 in multiple myeloma cells under hypoxic conditions;发表期刊:Biomarker Research;影响因子:未公开;研究领域:血液系统恶性肿瘤(多发性骨髓瘤)代谢调控与靶向治疗。
多发性骨髓瘤是一种起源于骨髓终末分化浆细胞的恶性肿瘤,近年来随着硼替佐米等蛋白酶体抑制剂的临床应用,患者的治疗格局得到显著改善,但多数患者会逐渐获得耐药性并出现疾病复发,成为临床治疗的核心难题。领域共识:骨髓微环境具有天然的低氧特征,低氧状态可诱导肿瘤细胞发生代谢重编程,通过增强糖酵解等途径满足快速增殖的能量需求,同时参与耐药相关信号通路的激活。目前领域内已证实6-磷酸果糖-2-激酶/果糖-2,6-双磷酸酶(PFKFB)家族是调控糖酵解的关键分子,但针对低氧微环境下PFKFB家族成员与蛋白酶体抑制剂耐药的关联研究仍存在空白,因此亟需探索靶向PFKFB家族逆转低氧介导的多发性骨髓瘤耐药的新策略,本研究正是针对这一问题展开,为临床难治性多发性骨髓瘤的治疗提供新的潜在靶点与联合治疗方案。
2. 文献综述解析
本文的文献综述部分以“多发性骨髓瘤治疗困境-骨髓低氧微环境特征-肿瘤代谢重编程调控”为逻辑主线,系统梳理了领域内现有研究的核心结论与局限性。
首先,作者回顾了多发性骨髓瘤的治疗进展,指出硼替佐米等蛋白酶体抑制剂的应用显著延长了患者生存期,但耐药性的产生导致疾病复发率居高不下,现有研究已证实低氧微环境是介导耐药的重要因素,但具体代谢调控机制尚未完全阐明。其次,针对肿瘤代谢重编程领域,现有研究已明确PFKFB家族通过调控果糖-2,6-双磷酸酶水平激活糖酵解,其中PFKFB3和PFKFB4在多种肿瘤中高表达并促进肿瘤进展,但多数研究未结合骨髓低氧微环境的特异性,也未探讨其与蛋白酶体抑制剂的联合治疗潜力。最后,作者通过对比现有研究的不足,凸显了本研究的创新价值:首次聚焦低氧条件下PFKFB3和PFKFB4在多发性骨髓瘤细胞中的表达特征,验证了靶向抑制这两个分子与蛋白酶体抑制剂的协同治疗效果,尤其是在硼替佐米耐药细胞系中的作用,为解决临床耐药问题提供了新的实验依据。
3. 研究思路总结与详细解析
本研究的整体研究框架为“低氧代谢分子筛选-单药疗效验证-联合治疗效果评估-耐药细胞系验证-机制探讨”,核心研究目标是明确低氧条件下PFKFB3和PFKFB4对多发性骨髓瘤细胞存活与药物敏感性的调控作用,核心科学问题是低氧下PFKFB3/4是否通过调控凋亡相关通路介导蛋白酶体抑制剂耐药,技术路线遵循“假设-实验验证-机制解析”的闭环逻辑。
3.1 低氧条件下PFKFB家族表达特征分析
实验目的为明确低氧环境对多发性骨髓瘤细胞中PFKFB家族基因及蛋白表达的影响,初步筛选潜在的治疗靶点。研究人员首先利用GEO数据库(GSE80140)分析了常氧与低氧组(1% O₂)多发性骨髓瘤样本的基因表达差异,随后选取U266、RPMI8226等多种多发性骨髓瘤细胞系,在常氧或低氧条件下培养24小时,通过免疫印迹实验检测蛋白表达水平,同时采用ELISA实验检测p38丝裂原活化蛋白激酶(p38 MAPK)的磷酸化水平。结果显示,低氧条件下PFKFB3和PFKFB4的基因表达显著高于常氧组(n=4,P<0.05),而PFKFB1和PFKFB2的表达无显著差异;蛋白水平上,PFKFB3和PFKFB4在低氧培养24小时后表达明显上调,且低氧可诱导p38 MAPK磷酸化及低氧诱导因子1α(HIF1α)表达升高,其中PFKFB3在低氧6-24小时持续上调,PFKFB4在低氧24小时后显著上调。
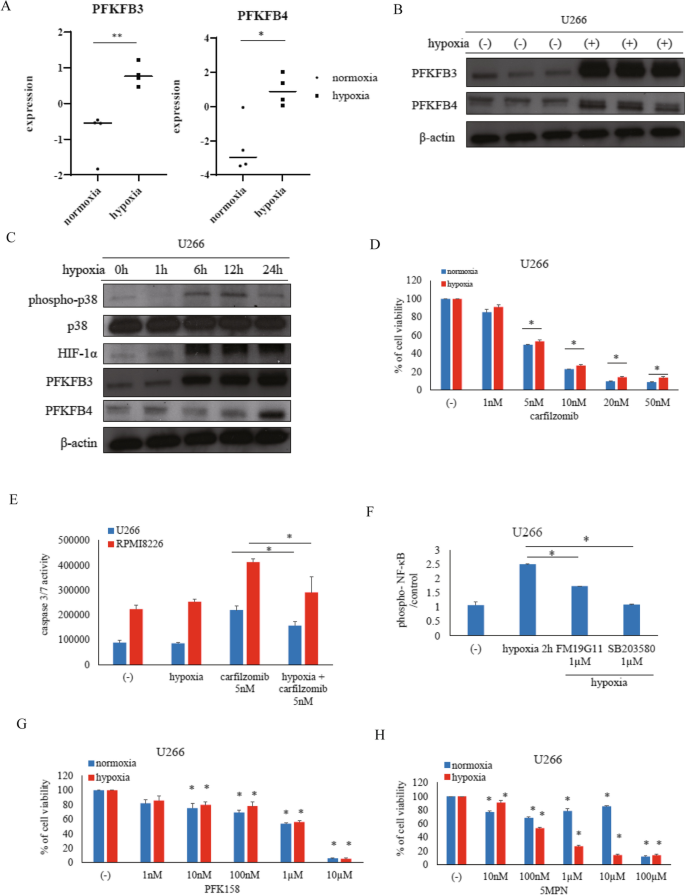
文献未提及具体实验产品,领域常规使用免疫印迹抗体、ELISA检测试剂盒、细胞培养相关试剂等。
3.2 低氧下卡非佐米敏感性及信号通路分析
实验目的为明确低氧环境对第二代蛋白酶体抑制剂卡非佐米疗效的影响,以及相关信号通路的调控作用。研究人员将多发性骨髓瘤细胞系分别在常氧和低氧条件下培养,加入不同浓度的卡非佐米处理72小时后,采用细胞计数试剂盒-8(CCK-8)检测细胞生长;处理48小时后,通过Caspase-Glo® 3/7检测试剂盒检测Caspase 3/7活性以评估细胞凋亡水平;同时在低氧培养2小时后,加入HIF1α抑制剂FM19G11或p38 MAPK抑制剂SB203580,采用ELISA实验检测核因子-κB(NF-κB)的磷酸化水平。结果显示,低氧条件下卡非佐米对细胞生长的抑制作用显著减弱,Caspase 3/7活性也明显降低(n=3,P<0.05),提示低氧可介导卡非佐米耐药;低氧培养2小时后NF-κB磷酸化水平升高,而FM19G11和SB203580可显著抑制NF-κB的磷酸化,表明HIF1α和p38 MAPK参与了低氧介导的NF-κB激活。
文献未提及具体实验产品,领域常规使用Caspase活性检测试剂盒、NF-κB ELISA试剂盒、细胞增殖检测试剂盒等。
3.3 PFKFB3/4抑制剂单药及与卡非佐米联合治疗效果验证
实验目的为验证PFKFB3抑制剂PFK158和PFKFB4抑制剂5MPN的单药治疗效果,以及与卡非佐米联合应用的协同治疗潜力。研究人员在常氧和低氧条件下,用不同浓度的PFK158或5MPN处理多发性骨髓瘤细胞系72小时,采用CCK-8检测细胞生长;随后将细胞与卡非佐米联合处理,检测Caspase 3/7活性、20S蛋白酶体活性及线粒体膜电位变化,并在硼替佐米耐药细胞系KMS-11/BTZ中验证联合治疗效果。结果显示,PFK158和5MPN可显著抑制多发性骨髓瘤细胞的生长(n=3,P<0.05);与卡非佐米联合处理后,细胞毒性显著增强,Caspase 3/7活性升高,20S蛋白酶体活性降低,线粒体膜电位破坏增加,联合治疗的组合指数(CI)<1,提示具有协同作用;在硼替佐米耐药细胞系KMS-11/BTZ中,联合治疗同样可显著抑制细胞生长并激活Caspase 3/7活性(n=3,P<0.05)。
实验所用关键产品:PFK158(PFKFB3抑制剂)、5MPN(PFKFB4抑制剂)、卡非佐米(第二代蛋白酶体抑制剂)。
3.4 凋亡相关通路与PFKFB3/4的关联机制探讨
实验目的为探讨低氧条件下PFKFB3和PFKFB4调控多发性骨髓瘤细胞存活与药物敏感性的下游机制。研究人员利用GEO数据库分析了低氧条件下BCL2L10的基因表达变化,以及其与PFKFB3/4的表达相关性;随后在低氧培养的U266细胞中加入卡非佐米与PFK158或5MPN联合处理,通过免疫印迹实验检测BCL-2家族蛋白的表达;同时采用短发夹RNA(shRNA)敲低PFKFB3或PFKFB4的表达,检测卡非佐米的敏感性变化。结果显示,低氧条件下BCL2L10的基因表达显著上调(n=4,P<0.01),且其表达与PFKFB3和PFKFB4的表达呈正相关;联合处理后,BCL-2、BCL-XL及BCL2L10的蛋白表达水平显著降低;shRNA敲低PFKFB3或PFKFB4后,细胞对卡非佐米的敏感性显著增强(n=3,P<0.05)。
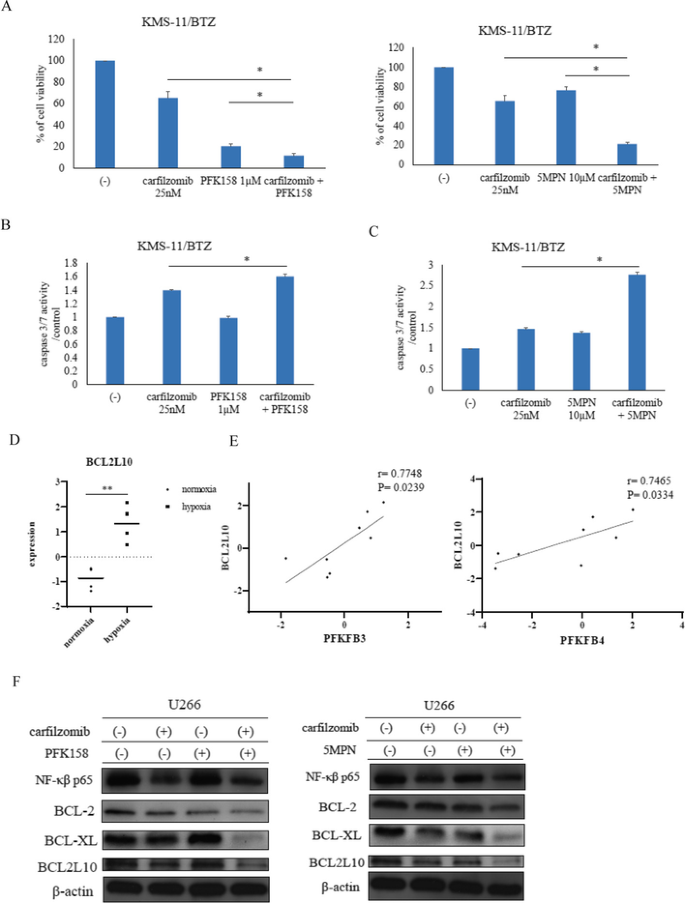
文献未提及具体实验产品,领域常规使用shRNA表达载体、免疫印迹抗体、实时荧光定量PCR试剂等。
4. Biomarker研究及发现成果
本研究中涉及的潜在生物标志物包括PFKFB3、PFKFB4及BCL2L10,筛选与验证逻辑为“数据库筛选-细胞系表达验证-功能关联分析-耐药细胞系验证”,完整覆盖了从分子筛选到功能验证的研究链条。
生物标志物的来源为GEO数据库中的多发性骨髓瘤样本及体外培养的多发性骨髓瘤细胞系,验证方法包括实时荧光定量PCR、免疫印迹实验、ELISA实验等。其中,PFKFB3和PFKFB4在低氧条件下的基因与蛋白表达均显著上调,与BCL2L10的表达呈正相关;在功能验证中,靶向抑制PFKFB3或PFKFB4可增强卡非佐米的细胞毒性,尤其是在硼替佐米耐药细胞系中效果显著。目前研究未提供临床样本的特异性与敏感性数据,但细胞实验结果显示,联合治疗的协同作用显著(CI<1),敲低PFKFB3/4后卡非佐米的IC50显著降低(文献未明确提供具体数值,基于图表趋势推测)。核心成果方面,PFKFB3和PFKFB4可作为低氧条件下多发性骨髓瘤细胞耐药的潜在生物标志物,其表达水平与细胞对蛋白酶体抑制剂的敏感性负相关;本研究首次证实低氧下靶向PFKFB3/4与蛋白酶体抑制剂的协同治疗效果,为临床难治性多发性骨髓瘤的治疗提供了新的潜在靶点;BCL2L10作为下游调控分子,可能参与了PFKFB3/4介导的耐药过程,但其具体调控机制仍需进一步研究。