1. 领域背景与文献引入
文献英文标题:Specific TCR profiles predict clinical outcome of adjuvant EGFR-TKIs for resected EGFR-mutant non-small cell lung cancer;发表期刊:Biomarker Research;影响因子:未公开;研究领域:EGFR突变型非小细胞肺癌辅助治疗与免疫生物标志物研究。
领域共识:非小细胞肺癌(NSCLC)是全球发病率和死亡率最高的恶性肿瘤之一,表皮生长因子受体(EGFR)突变是NSCLC最常见的驱动基因突变类型,针对该突变的表皮生长因子受体-酪氨酸激酶抑制剂(EGFR-TKI)已成为核心治疗方案。ADJUVANT-CTONG1104、ADAURA等前瞻性III期临床试验证实,辅助EGFR-TKI治疗相较于传统化疗,能为EGFR突变型早期NSCLC患者带来更优的生存获益,推动了该类患者的治疗范式转变。但临床实践中发现,不同患者从辅助EGFR-TKI治疗中的获益存在显著异质性,现有生物标志物仍无法精准筛选出最可能获益的人群,亟需探索更具特异性的预测指标。此前研究已从CTONG1104试验中鉴定出部分具有辅助治疗预测价值的T细胞受体(TCR)序列,并发现TCR库与基因组变异存在关联,但针对仅接受辅助EGFR-TKI治疗患者的精准预测TCR序列仍不明确,这一研究空白为本文的开展提供了必要性,旨在为EGFR突变型NSCLC患者的辅助治疗决策提供更精准的免疫生物标志物。
2. 文献综述解析
本文作者对领域内现有研究的分类维度主要包括辅助治疗类型(EGFR-TKI vs 化疗)、生物标志物类型(基因组特征 vs 免疫组库特征)两大方向。现有研究已证实,辅助EGFR-TKI治疗在EGFR突变型II-IIIA期NSCLC患者中的生存获益优于化疗,但患者个体间的获益差异无法通过EGFR突变状态单独解释;基因组特征分析已能区分不同辅助治疗结局的EGFR突变型NSCLC亚型,但免疫层面的生物标志物研究仍处于起步阶段。TCR库作为反映肿瘤微环境抗肿瘤免疫状态的核心指标,已被证实可作为肿瘤患者预后及免疫治疗疗效的预测生物标志物,部分研究也发现TCR序列与NSCLC辅助治疗结局存在关联,但现有研究未针对仅辅助EGFR-TKI治疗的场景构建特异性预测模型,且未整合高低频率TCR序列的协同预测价值。通过对比现有研究的未解决问题,本文的创新价值凸显为首次针对EGFR突变型NSCLC患者的辅助EGFR-TKI治疗场景,构建了由特定高低频率TCR序列组合而成的预后预测模型,填补了该场景下免疫生物标志物的研究空白,为精准筛选获益人群提供了新的技术路径。
3. 研究思路总结与详细解析
本文的研究目标是构建适用于EGFR突变型早期NSCLC患者的辅助EGFR-TKI治疗预后及获益预测模型,核心科学问题是明确哪些特定TCR序列可增强辅助EGFR-TKI治疗的预测价值,技术路线遵循“样本收集与测序→差异TCR筛选→模型构建与优化→独立预测性验证→序列特征分析”的闭环逻辑。
3.1 样本收集与TCRβ基因测序
本环节的核心目标是获取接受辅助吉非替尼治疗的EGFR突变型NSCLC患者的TCR库基础数据。研究从ADJUVANT-CTONG1104试验中收集了57例肿瘤组织样本和12例癌旁组织样本,对所有样本进行TCRβ基因测序,以获取TCR重排的完整序列信息。测序结果成功覆盖了样本中的TCRβ基因重排谱,为后续的差异分析和模型构建提供了核心数据支撑。文献未提及具体实验产品,领域常规使用TCR高通量测序试剂盒、Illumina高通量测序平台等。
3.2 差异表达TCR筛选与组合模型构建
本环节的核心目标是筛选具有预后预测价值的TCR序列,并构建最优的组合预测模型。研究首先采用Mann-Whitney-Wilcoxon检验对比肿瘤组织与癌旁组织的TCR表达差异,鉴定出89个低克隆性、105个高克隆性的差异表达TCR;随后对高克隆性TCR进行单因素Cox回归分析,筛选出与总生存期(OS)相关的候选TCR(P<0.1);最后通过100次重复10折交叉验证,确定由高频率Vβ7-3Jβ2-5、Vβ24-1Jβ2-1与低频率Vβ5-6Jβ2-7、Vβ28Jβ2-2组成的组合模型为最优预测模型,该模型对OS的预测价值显著(P<0.001,风险比[HR]=9.65,95%置信区间[CI]:2.27至41.12)。
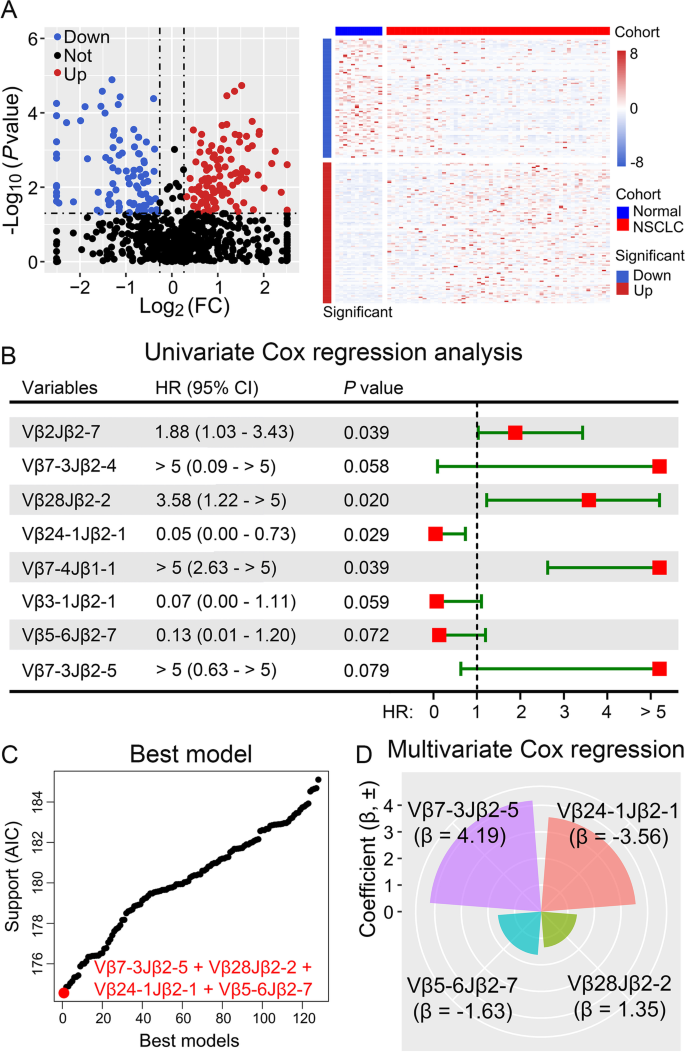
文献未提及具体实验产品,领域常规使用生物信息学分析软件(如R语言、Cox回归分析工具包)等。
3.3 模型预后预测能力与独立验证
本环节的核心目标是验证组合模型对OS和无病生存期(DFS)的预测能力,并确认其独立预后价值。研究通过Kaplan-Meier生存分析发现,基于组合模型计算的风险评分与患者生存获益呈负相关,低风险评分患者的5年生存率达90%,OS和DFS的生存曲线均呈现显著分离(OS:P<0.001,HR=9.65,95%CI:2.27至41.12;DFS:P=0.02,HR=2.61,95%CI:1.13至6.03)。进一步纳入性别、年龄、吸烟史、病理类型、临床分期等多类临床数据进行多因素Cox回归分析,结果显示该模型的风险评分仍是OS(P=0.003,HR=9.49,95%CI:2.21至40.92)和DFS(P=0.015,HR=3.13,95%CI:1.25至7.87)的独立预后预测因子,不受其他临床因素的干扰。
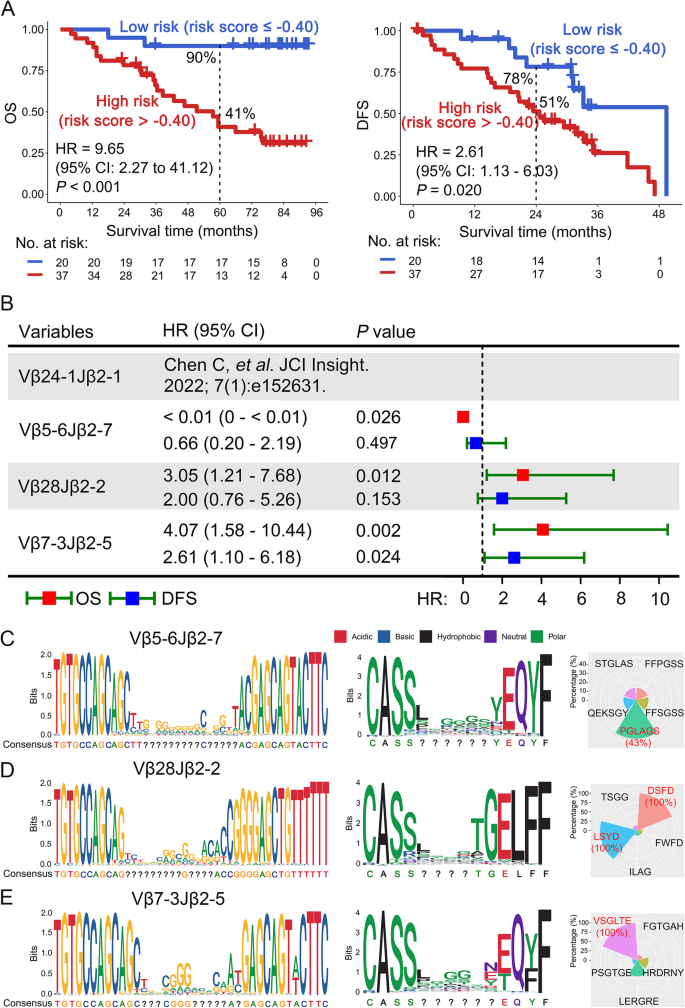
文献未提及具体实验产品,领域常规使用生存分析软件(如GraphPad Prism、R语言survival包)等。
3.4 TCR克隆型序列特征分析
本环节的核心目标是明确组合模型中特定TCR序列的CDR3基序特征,为后续的功能验证提供基础。研究对高频率TCR组的核苷酸和氨基酸序列进行比对分析,鉴定出各TCR序列的Top5 CDR3基序:Vβ5-6Jβ2-7的优势基序为PGLAGS(频率43%),Vβ28Jβ2-2的优势基序为LSYD和DSFD(频率均为100%),Vβ7-3Jβ2-5的优势基序为VSGLTE(频率100%)。这些特异性基序的鉴定为后续探索TCR序列与肿瘤抗原的结合特异性提供了关键线索。文献未提及具体实验产品,领域常规使用序列比对软件(如BLAST、ClustalW)等。
4. Biomarker研究及发现成果
本文涉及的Biomarker为特定TCR重排组合(Vβ7-3Jβ2-5、Vβ24-1Jβ2-1、Vβ5-6Jβ2-7、Vβ28Jβ2-2),其筛选与验证逻辑遵循“临床样本测序筛选→单因素Cox回归初筛→交叉验证优化模型→多因素Cox验证独立预测性→序列特征解析”的完整链条。该Biomarker的来源为接受辅助吉非替尼治疗的EGFR突变型NSCLC患者的肿瘤组织样本,验证方法包括TCRβ基因测序、Cox比例风险回归分析、Kaplan-Meier生存分析。在特异性与敏感性方面,该组合模型对总生存期的预测风险比为9.65(95%CI:2.27至41.12,P<0.001),对无病生存期的预测风险比为2.61(95%CI:1.13至6.03,P=0.02),低风险评分患者的5年生存率达90%,显示出较强的预后区分能力。核心成果方面,该TCR组合模型是首个针对EGFR突变型NSCLC辅助EGFR-TKI治疗场景的独立预后生物标志物,首次整合高低频率TCR序列的协同预测价值,为精准筛选适合辅助EGFR-TKI治疗的患者提供了免疫层面的新依据,其统计学结果明确,基于57例肿瘤组织样本(n=57)完成验证,填补了该领域的研究空白。
