1. 领域背景与文献引入
文献英文标题:Targeting serine-glycine-one-carbon metabolism as a vulnerability in cancers;发表期刊:Biomarker Research;影响因子:未公开;研究领域:肿瘤代谢重编程与靶向治疗
领域共识:细胞代谢重编程是恶性肿瘤的核心特征之一,自Warburg效应提出以来,肿瘤代谢通路的异常调控逐渐成为肿瘤研究的核心方向。2014年Mehrmohamadi等首次提出丝氨酸-甘氨酸-一碳(SGOC)代谢网络的概念,明确其在肿瘤细胞增殖、存活中的关键作用;后续研究证实SGOC通路在神经内分泌前列腺癌、MYCN扩增神经母细胞瘤等多种恶性肿瘤中高度激活,成为肿瘤的可靶向脆弱点。当前研究热点聚焦于SGOC通路的调控机制、与肿瘤免疫微环境的交互作用,以及靶向SGOC的联合治疗策略,但仍存在核心未解决问题:不同肿瘤中SGOC通路的激活机制存在显著异质性,缺乏统一的调控模型;靶向SGOC的抑制剂特异性不足,临床转化效率较低;SGOC相关生物标志物(Biomarker)的临床验证数据匮乏,难以指导个性化治疗。
针对上述研究空白,本文系统综述了SGOC代谢通路的核心组分、在肿瘤中的功能调控机制、与免疫治疗及铁死亡的交叉作用,以及靶向SGOC代谢酶的治疗进展,为领域内进一步探索SGOC的临床转化潜力提供了全面的参考框架,填补了领域内对SGOC通路多维度调控机制及临床应用价值综述的空白。
2. 文献综述解析
本文采用“通路组分-功能调控-交叉作用-治疗策略”的分类维度,系统梳理了SGOC代谢通路在肿瘤中的研究进展,通过整合细胞代谢、分子生物学、临床研究等多层面数据,明确了SGOC通路作为肿瘤治疗靶点的核心价值。
现有研究已证实SGOC通路的核心代谢酶(如磷酸甘油酸脱氢酶PHGDH、丝氨酸羟甲基转移酶SHMT1/2等)在多种肿瘤中高表达,且与肿瘤大小、淋巴结转移、不良预后显著相关;技术层面,稳定同位素示踪、代谢组学分析等方法揭示了SGOC通路为肿瘤提供核苷酸合成前体、甲基供体及氧化还原平衡调控的关键功能。但现有研究存在局限性:多数研究集中于单一肿瘤类型或单一酶的功能,缺乏对SGOC整体调控网络的系统分析;部分靶向抑制剂的研究仅在细胞系或小鼠模型中开展,临床疗效数据不足;SGOC与免疫治疗、铁死亡的交叉作用机制尚未完全阐明,缺乏临床样本的验证数据。
与现有研究相比,本文的创新点在于首次系统整合了SGOC通路的代谢网络、转录与表观调控机制、与肿瘤免疫及铁死亡的交互作用,以及非编码RNA的调控网络,填补了领域内对SGOC通路多维度调控机制综述的空白;同时,本文全面总结了靶向SGOC代谢酶的小分子抑制剂研发进展,为临床联合治疗策略的优化提供了方向,解决了领域内对SGOC临床转化潜力认知不全面的问题。
3. 研究思路总结与详细解析
本文的研究目标是系统阐述SGOC代谢通路在肿瘤中的核心作用、调控机制及临床转化潜力,核心科学问题是明确SGOC通路成为肿瘤治疗脆弱点的关键机制,技术路线为“通路组分解析-功能调控机制-交叉作用分析-治疗策略综述”的逻辑闭环,全面整合了领域内的研究数据。
3.1 SGOC代谢通路核心组分解析
实验目的:明确SGOC代谢通路的核心代谢循环及关键酶的功能。
方法细节:综述领域内采用稳定同位素示踪、代谢组学分析、酶活性检测等方法开展的研究,涵盖丝氨酸-甘氨酸代谢、叶酸介导的一碳代谢、甲硫氨酸循环与转硫通路三个核心部分。
结果解读:丝氨酸可通过细胞膜转运体摄取或从头合成,经PHGDH、磷酸丝氨酸转氨酶1(PSAT1)、磷酸丝氨酸磷酸酶(PSPH)等酶催化生成甘氨酸,同时通过SHMT1/2转移一碳单位至四氢叶酸(THF),进入叶酸循环;叶酸循环产生的一碳单位参与核苷酸合成、甲硫氨酸循环,生成S-腺苷甲硫氨酸(SAM)作为甲基供体,参与DNA、RNA及蛋白的甲基化修饰;转硫通路则将甲硫氨酸循环与谷胱甘肽(GSH)合成关联,调控细胞氧化还原平衡。图1清晰展示了SGOC通路的完整代谢网络,明确了各组分的交互关系。
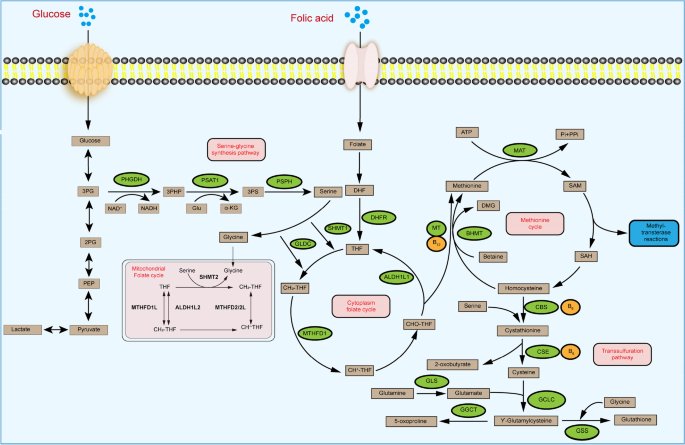
产品关联:文献未提及具体实验产品,领域常规使用代谢组学分析平台(如液相色谱-质谱联用LC-MS)、重组代谢酶试剂、稳定同位素标记底物等。
3.2 SGOC在肿瘤中的功能调控机制解析
实验目的:阐明SGOC通路在肿瘤中的氧化还原平衡、表观遗传及转录调控机制。
方法细节:综述领域内采用基因敲低/过表达、染色质免疫共沉淀测序(ChIP-seq)、RNA测序(RNA-seq)等方法开展的研究,分析SGOC通路对肿瘤细胞氧化还原、表观修饰及转录的调控作用。
结果解读:SGOC通路通过产生烟酰胺腺嘌呤二核苷酸磷酸(NADPH)维持细胞氧化还原平衡,如SHMT2在MYC转化细胞中催化丝氨酸降解,产生NADPH以清除活性氧(ROS);表观调控层面,组蛋白甲基转移酶G9A通过维持组蛋白H3赖氨酸9单甲基化(H3K9me1)修饰激活SGOC酶的转录,核因子E2相关因子2(NRF2)的SUMO化修饰上调PHGDH表达,促进丝氨酸从头合成;转录调控层面,MYC、缺氧诱导因子1/2(HIF-1/2)、转录共激活因子TAZ/YAP等转录因子可结合SGOC酶的启动子区域,上调其表达,支持肿瘤增殖。
产品关联:文献未提及具体实验产品,领域常规使用CRISPR-Cas9基因编辑工具、ChIP试剂盒、RNA-seq测序平台等。
3.3 SGOC与肿瘤免疫治疗的关联分析
实验目的:明确SGOC通路对肿瘤免疫微环境及免疫治疗疗效的影响。
方法细节:综述领域内采用免疫组化(IHC)、流式细胞术、动物模型联合免疫治疗等方法开展的研究,分析SGOC通路与免疫细胞代谢、免疫抑制微环境的关系。
结果解读:SGOC通路调控效应T细胞的代谢,丝氨酸是效应T细胞增殖的必需代谢物,T细胞激活后上调SGOC酶的表达;靶向SGOC通路的抑制剂如培美曲塞可增强T细胞激活,诱导免疫原性细胞死亡,联合PD-1抑制剂可增强抗肿瘤效果;SGOC酶的表达与免疫细胞浸润相关,如PSAT1在肺癌中与肿瘤突变负荷正相关,与免疫抑制负相关,可作为免疫治疗疗效的潜在Biomarker。
产品关联:文献未提及具体实验产品,领域常规使用流式细胞仪、免疫组化(IHC)试剂盒、免疫检查点抑制剂试剂等。
3.4 SGOC与铁死亡的交互作用解析
实验目的:揭示SGOC通路对铁死亡的调控机制。
方法细节:综述领域内采用铁死亡诱导剂处理、基因敲低/过表达、蛋白质免疫印迹(Western blot)等方法开展的研究,分析SGOC通路与铁死亡核心调控因子的交互作用。
结果解读:PHGDH可结合RNA结合蛋白PCBP2,抑制其泛素化降解,进而稳定溶质载体家族7成员11(SLC7A11)的mRNA,上调SLC7A11表达,抑制铁死亡;PSAT1、亚甲基四氢叶酸脱氢酶2(MTHFD2)等酶也被证实参与铁死亡的调控,如PSAT1在肝癌中被c-Jun转录激活,拮抗铁死亡。图2展示了PHGDH调控铁死亡的具体机制。
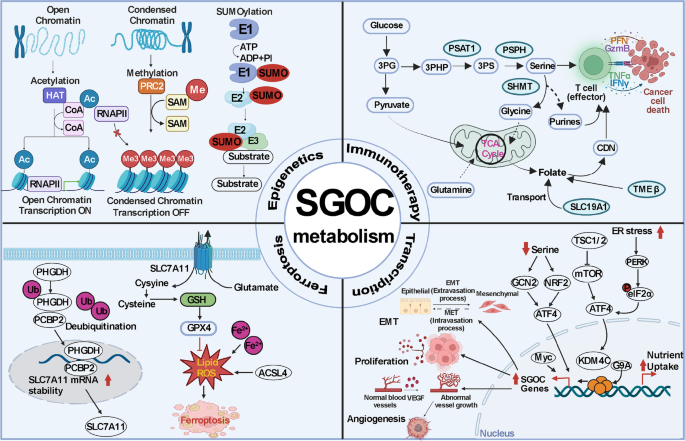
产品关联:文献未提及具体实验产品,领域常规使用铁死亡诱导剂(如Erastin)、Western blot抗体、qRT-PCR试剂盒等。
3.5 非编码RNA对SGOC通路的调控机制解析
实验目的:阐明非编码RNA对SGOC代谢酶的调控作用。
方法细节:综述领域内采用长链非编码RNA(lncRNA)芯片、微小RNA(miRNA)测序、双荧光素酶报告基因实验等方法开展的研究,分析lncRNA、miRNA对SGOC酶的转录后调控。
结果解读:lncRNA如RP4-694A7.2可通过GSK3β/β-catenin通路调控PSAT1的表达,促进肝癌细胞增殖;miRNA如miR-340可靶向PSAT1,抑制食管鳞状细胞癌的进展;环状RNA如circ_0072995可通过海绵吸附miR-149-5p,上调SHMT2表达,促进乳腺癌恶性表型。图3展示了非编码RNA调控SGOC代谢酶的网络。
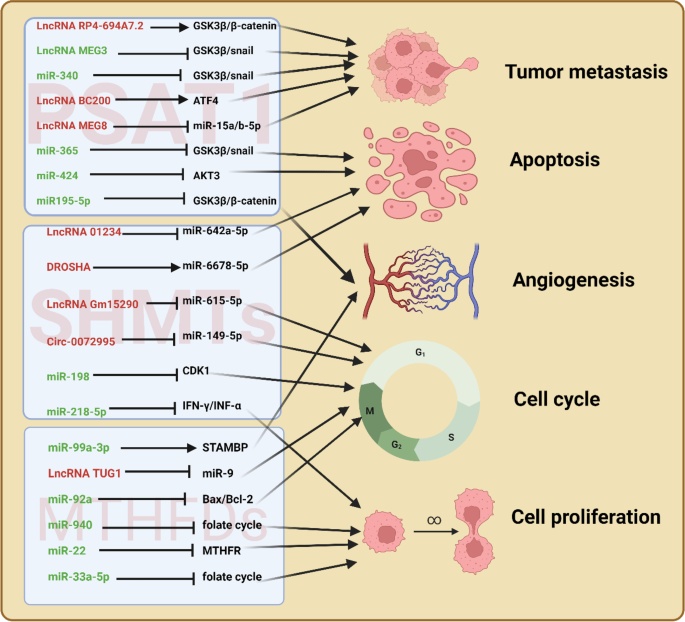
产品关联:文献未提及具体实验产品,领域常规使用双荧光素酶报告基因试剂盒、RNA干扰试剂、lncRNA/miRNA表达检测试剂盒等。
3.6 靶向SGOC代谢酶的治疗策略综述
实验目的:总结靶向SGOC代谢酶的小分子抑制剂研发进展及临床应用潜力。
方法细节:综述领域内采用高通量筛选、药物化学合成、临床实验等方法开展的研究,分析不同类型抑制剂的特异性及疗效。
结果解读:PHGDH抑制剂分为合成类(如BI-4924、NCT-503)和天然产物类(如Azacoccone E),可有效抑制丝氨酸从头合成;SHMT抑制剂如SHIN1具有特异性抑制SHMT活性的作用;叶酸通路抑制剂如培美曲塞已用于临床治疗非小细胞肺癌等肿瘤,联合免疫治疗可增强疗效;饮食限制丝氨酸/甘氨酸摄入联合二甲双胍可抑制肿瘤生长,为临床辅助治疗提供了新方向。
产品关联:实验所用关键产品:PHGDH抑制剂BI-4924、NCT-503,SHMT抑制剂SHIN1,叶酸通路抑制剂培美曲塞。
4. Biomarker研究及发现成果解析
本文系统总结了SGOC代谢通路核心酶作为肿瘤预后及免疫治疗疗效Biomarker的研究成果,明确了其临床应用潜力,为个性化治疗提供了参考。
Biomarker定位
涉及的Biomarker类型为肿瘤组织中高表达的SGOC代谢酶(PHGDH、SHMT1/2、PSAT1、MTHFD2等),筛选/验证逻辑为:基于TCGA数据库的组学分析筛选差异表达酶,通过细胞系实验验证其功能,再通过临床样本免疫组化或qRT-PCR验证其与临床病理特征及预后的相关性。
研究过程详述
Biomarker来源为临床肿瘤组织样本、血液样本;验证方法包括免疫组化(IHC)检测蛋白表达水平、qRT-PCR检测mRNA表达、生存分析评估预后价值;特异性与敏感性数据:PHGDH在胰腺癌中与肿瘤大小、淋巴结转移、TNM分期相关,是独立预后指标(文献未提供AUC、敏感性等具体数据);SHMT1 C1420T多态性与非霍奇金淋巴瘤风险相关(n=7309,P值未明确);PSAT1在肺癌中与肿瘤突变负荷正相关,与免疫抑制负相关(文献未提供具体统计学数据)。
核心成果提炼
这些SGOC代谢酶的高表达与多种肿瘤的不良预后相关,如PHGDH在胰腺癌中提示不良预后,SHMT2在乳腺癌、肝癌等肿瘤中与CD8+T细胞浸润相关;创新性在于首次系统总结了SGOC酶作为Biomarker在不同肿瘤中的临床价值,以及与免疫治疗疗效的相关性;部分数据显示PSAT1可作为肺癌患者生存及免疫治疗疗效的潜在Biomarker,MTHFD2在膀胱癌中与PD-L1激活相关,可作为免疫治疗的预测指标(文献未提供HR值、P值等具体统计学结果)。推测:SGOC代谢酶的表达水平结合肿瘤突变负荷、免疫细胞浸润数据,可进一步优化免疫治疗疗效的预测模型,需大样本临床研究验证。
