1. 领域背景与文献引入
文献英文标题:Pilot clinical trial and phenotypic analysis in chemotherapy-pretreated, metastatic triple-negative breast cancer patients treated with oral TAK-228 and TAK-117 (PIKTOR) to increase DNA damage repair deficiency followed by cisplatin and nab paclitaxel;发表期刊:Biomarker Research;影响因子:未公开;研究领域:转移性三阴性乳腺癌靶向治疗与生物标志物研究
三阴性乳腺癌(TNBC)是乳腺癌中侵袭性最强的亚型,约占所有乳腺癌的15%-20%,其特征是雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(HER2)均为阴性,缺乏针对性内分泌治疗或抗HER2治疗靶点,传统化疗是主要治疗手段,但耐药性问题突出,晚期患者5年生存率不足30%。领域发展关键节点清晰:2014年PARP抑制剂在BRCA突变TNBC中的获批开启了精准治疗时代;2019年免疫检查点抑制剂帕博利珠单抗获批用于PD-L1阳性晚期TNBC,拓展了免疫治疗方向。当前研究热点聚焦于三个方向:靶向PI3K/AKT/mTOR通路的联合治疗策略、DNA损伤修复(DDR)缺陷的诱导与利用、免疫治疗耐药机制的破解。未解决的核心问题依然严峻:对于经多线化疗预处理的转移性TNBC,现有治疗手段有效率不足20%,缺乏能逆转耐药、增强后续化疗及免疫治疗敏感性的系统性策略;同时,如何筛选能从这类联合治疗中获益的患者群体,缺乏特异性、可临床转化的生物标志物。
针对这一临床空白,本研究探索了PIKTOR(TAK-228,TORC1/2抑制剂,联合TAK-117,PI3Kα抑制剂)预处理对转移性TNBC的作用,旨在通过诱导DDR缺陷增加肿瘤对后续顺铂+白蛋白结合型紫杉醇化疗及帕博利珠单抗免疫治疗的敏感性,同时通过多组学分析解析潜在的获益预测生物标志物,为难治性TNBC的治疗提供新的思路与依据。
2. 文献综述解析
作者按“DDR缺陷与TNBC治疗的关联→PI3K/AKT/mTOR通路对DDR的调控→PI3K/mTOR抑制剂联合治疗的临床前与初步临床证据”的逻辑维度对现有研究进行分类评述,系统梳理了领域内的研究进展与不足。
现有研究的关键结论显示,TNBC中约70%存在同源重组缺陷(HRD),HRD状态与PARP抑制剂、铂类化疗的敏感性直接相关,是精准治疗的核心靶点之一;PI3K/AKT/mTOR通路的异常激活在TNBC中发生率超过40%,可通过调控DDR相关蛋白的表达或活性维持基因组稳定性,导致肿瘤对DNA损伤类药物耐药;PI3K或mTOR单药抑制剂可诱导HRD样状态,增强TNBC对铂类或PARP抑制剂的敏感性,但单药抑制效果有限,联合抑制PI3K与mTOR可实现更强的通路阻断,发挥协同抗肿瘤效应。技术方法层面,临床前研究通过细胞系、异种移植模型验证了PI3K/mTOR联合抑制的协同效应,部分临床案例显示这类联合治疗后序贯化疗可实现持久缓解,但现有研究多为小样本或回顾性分析,缺乏针对经多线化疗预处理转移性TNBC的前瞻性系统性研究;同时,对PI3K/mTOR抑制后肿瘤基因组、蛋白质组及免疫微环境的动态变化解析不足,尚未明确能预测后续治疗获益的生物标志物。
本研究的创新价值在于,首次在经化疗预处理的转移性TNBC患者中开展PIKTOR预处理序贯化疗及免疫治疗的前瞻性临床研究,通过多组学(全外显子测序、RNA测序、反向蛋白质阵列)分析,系统解析了PIKTOR治疗后肿瘤DDR、免疫微环境及细胞信号通路的变化,明确了与持久获益相关的生物标志物特征,为这类难治性肿瘤的治疗策略优化提供了直接临床证据,弥补了现有研究在临床人群系统性分析及生物标志物解析方面的空白。
3. 研究思路总结与详细解析
本研究的核心目标是评估PIKTOR预处理序贯顺铂+白蛋白结合型紫杉醇及帕博利珠单抗在经化疗预处理转移性TNBC中的安全性与有效性,同时解析PIKTOR诱导的肿瘤生物学变化及获益预测生物标志物;核心科学问题是PIKTOR是否能通过抑制PI3K/AKT/mTOR通路诱导DDR缺陷,增强肿瘤对后续治疗的敏感性,以及哪些分子特征可预测患者获益;技术路线遵循“患者入组与PIKTOR治疗→疾病进展后序贯化疗→化疗后序贯免疫治疗→多时间点样本采集→多组学分析→生物标志物与临床疗效关联分析”的闭环逻辑,确保研究结果的科学性与关联性。
3.1 临床研究设计与患者入组
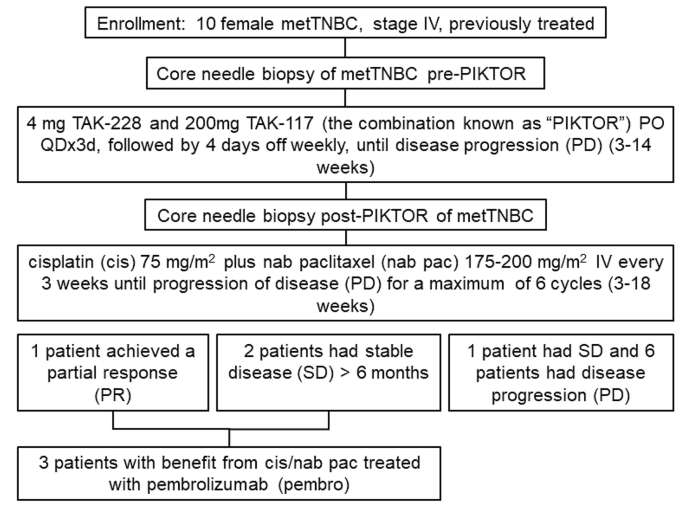
实验目的是明确PIKTOR预处理序贯化疗及免疫治疗的临床疗效与安全性,确定入组患者的基线特征。方法细节为入组10例经化疗预处理的转移性TNBC患者,给予口服4mg TAK-228+200mg TAK-117(PIKTOR),采用连续3天给药、4天停药的每周循环方案,直至疾病进展;随后给予静脉注射顺铂75mg/m²+白蛋白结合型紫杉醇220mg/m²,每3周1次,最多6个周期;化疗后给予帕博利珠单抗单药或联合化疗,同时在PIKTOR治疗前及疾病进展时采集转移灶活检样本及血液样本。结果解读显示,患者中位年龄49.5岁,中位既往化疗方案数为3,7例曾接受卡铂治疗;PIKTOR治疗的中位时间为8周,3例持久获益患者的中位PIKTOR治疗时间为11周;PIKTOR相关不良事件主要为疲劳(90%)、恶心(80%)等,多为轻中度,安全性良好;序贯化疗后,客观缓解率为10%,临床获益率为30%,3例患者在后续帕博利珠单抗治疗中分别获得1.2年、2年、3.6年的持久无进展生存。文献未提及具体实验产品,领域常规使用的临床治疗药物包括TAK-228、TAK-117、顺铂、白蛋白结合型紫杉醇、帕博利珠单抗;样本采集与处理常规使用EDTA采血管、Qiagen核酸提取试剂盒等。
3.2 全外显子测序与基因组变异分析
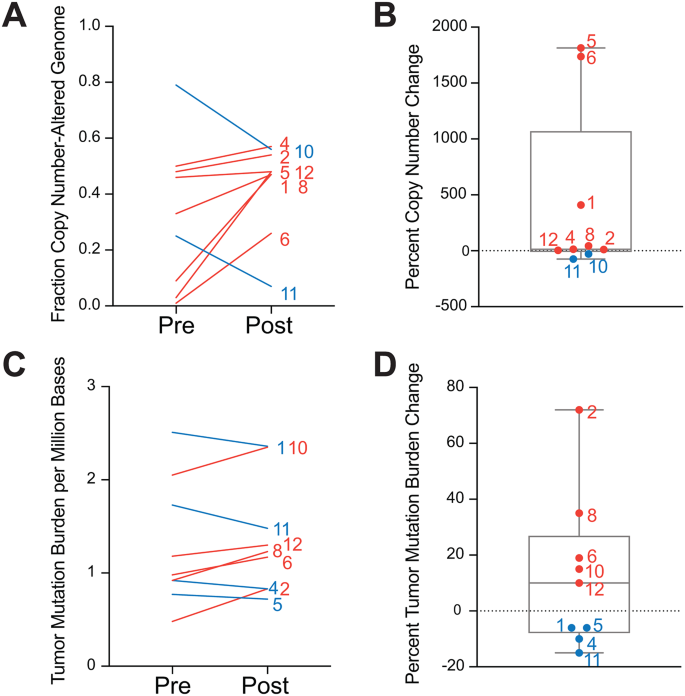
实验目的是解析PIKTOR治疗前后肿瘤基因组的变化,尤其是DDR相关基因变异、拷贝数变异(CNV)及肿瘤突变负荷(TMB)的动态变化。方法细节为对PIKTOR治疗前及疾病进展时的转移灶活检样本进行全外显子测序,使用TGen Jetstream pipeline进行数据分析,包括序列比对、变异检测(体细胞突变、CNV、结构变异)、注释及过滤;计算基因组拷贝数改变比例及TMB。结果解读显示,所有患者均存在TP53突变;8/9例患者(1例样本未通过质控)的PIKTOR治疗后样本显示基因组拷贝数改变比例增加,其中2例持久获益患者的增加幅度位居前3;5/9例患者TMB升高,2例持久获益患者的TMB升高幅度位居前3;持久获益患者治疗后错配修复(MMR)缺陷特征消失,而部分非获益患者出现MMR缺陷特征。文献未提及具体实验产品,领域常规使用的全外显子测序试剂盒包括Agilent SureSelect XT系列,测序平台为Illumina NovaSeq系列。
3.3 RNA测序与基因表达通路分析
实验目的是解析PIKTOR治疗前后肿瘤转录组的变化,明确通路水平的调控特征。方法细节为对活检样本进行RNA测序,使用STAR进行序列比对,Salmon及HTSeq进行基因表达定量,DESeq2进行差异表达分析,Ingenuity Pathway Analysis(IPA)进行通路富集分析。结果解读显示,整体队列中仅3个基因(PKHD1L1、COL4A3、DERL3)在治疗后显著下调;分层分析显示,持久获益患者治疗后PI3K/AKT/mTOR通路相关基因表达呈下调趋势,包括肌醇代谢、PI3K信号传导等通路;同时,持久获益患者治疗后PD-1/PD-L1通路基因表达显著上调,而多个免疫炎症通路(如Th1/Th2细胞互作、NK细胞信号)表达下调。文献未提及具体实验产品,领域常规使用的RNA测序试剂盒包括Roche KAPA stranded RNA HyperPrep Kit,测序平台为Illumina NovaSeq系列。
3.4 反向蛋白质阵列(RPPA)与蛋白质组分析
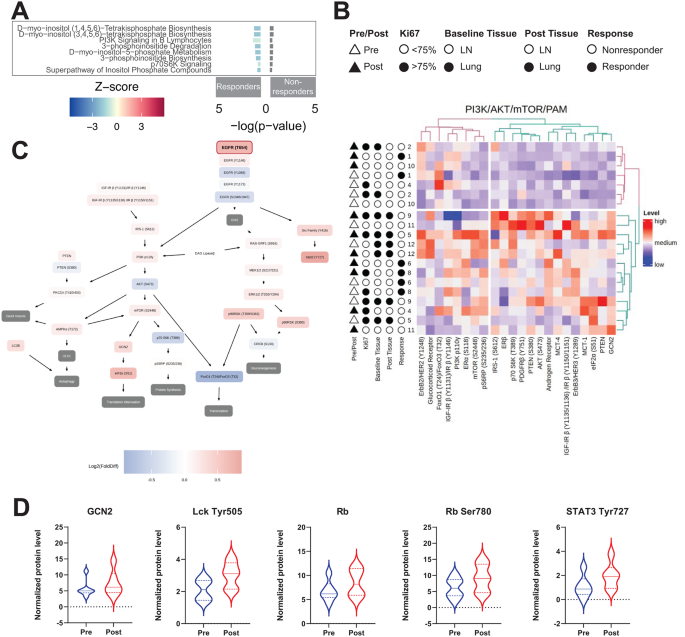
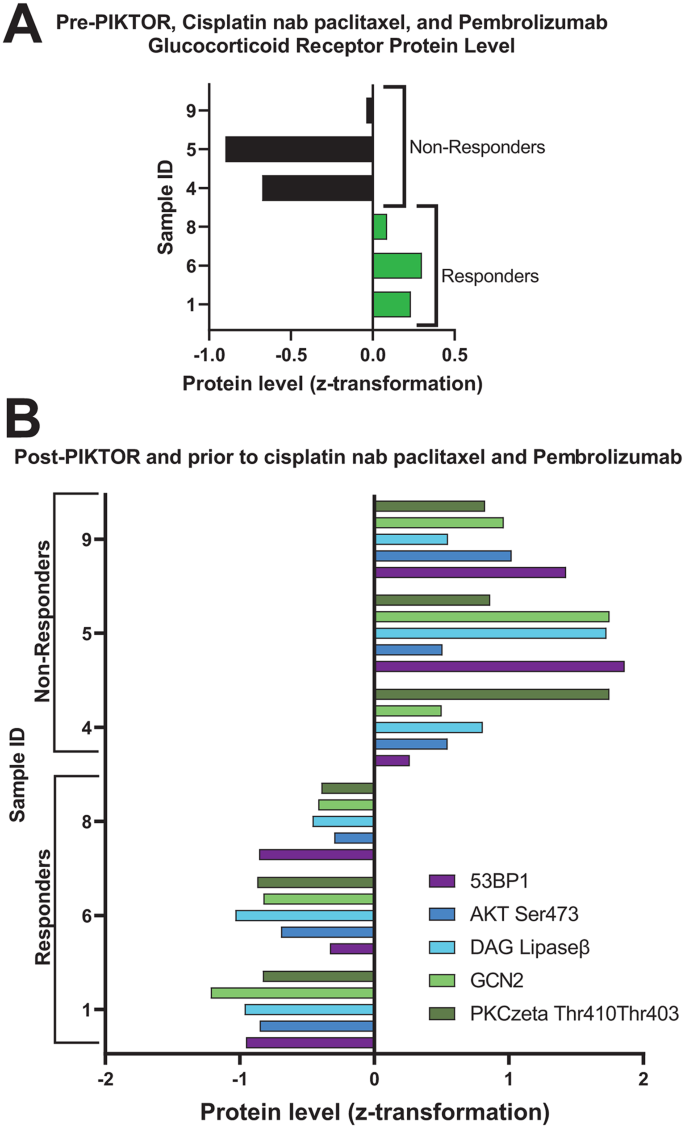
实验目的是解析PIKTOR治疗前后肿瘤细胞信号通路蛋白的动态变化,明确功能层面的调控特征。方法细节为通过激光捕获显微切割(LCM)分离转移灶样本中的肿瘤细胞,提取蛋白质后构建RPPA,使用特异性抗体检测细胞信号通路蛋白的表达及磷酸化水平,采用Mann-Whitney检验进行统计学分析。结果解读显示,PIKTOR治疗后,肿瘤细胞中AR、AMPKα Thr172、EGFR Thr654等蛋白水平显著升高;PI3K/AKT/mTOR通路关键节点(AKT Ser473、p70S6 Thr389)的磷酸化水平下调,显示通路抑制效果;持久获益患者治疗后,53BP1、DAG Lipaseβ、GCN2、AKT Ser473、PKCzeta Thr410/403这5种蛋白水平显著低于非获益患者;同时,持久获益患者治疗前糖皮质激素受体(GR)蛋白水平显著高于非获益患者(p=0.048,n=10)。文献未提及具体实验产品,领域常规使用的LCM仪器包括ArcturusXT,RPPA检测抗体多为商业化单克隆抗体,如Cell Signaling Technology系列。
4. Biomarker研究及发现成果解析
本研究涉及的Biomarker包括基因组特征(TMB、拷贝数改变比例、MMR缺陷特征)、转录组特征(PD-1/PD-L1通路基因表达)及蛋白质组特征(53BP1、DAG Lipaseβ、GCN2、AKT Ser473、PKCzeta Thr410/403、GR),筛选与验证逻辑遵循“临床疗效分层→多组学特征对比→生物标志物与疗效关联分析→潜在预测价值验证”的完整链条,确保结果的可靠性与临床转化潜力。
Biomarker来源为PIKTOR治疗前及疾病进展时的转移灶活检样本,验证方法包括全外显子测序(TMB、拷贝数变异、MMR特征)、RNA测序(通路基因表达)、RPPA(蛋白表达及磷酸化水平);特异性与敏感性数据显示,持久获益患者中,治疗后TMB升高比例为66.7%(2/3),拷贝数改变比例升高比例为100%(3/3);治疗前GR蛋白水平在获益患者中的表达量显著高于非获益患者(p=0.048,n=10);治疗后5种蛋白(53BP1、DAG Lipaseβ、GCN2、AKT Ser473、PKCzeta Thr410/403)在获益患者中的水平显著低于非获益患者(p<0.05,n=10)。
核心成果提炼显示,这些Biomarker的功能关联明确:TMB升高提示肿瘤免疫原性增强,有利于后续免疫治疗的激活;MMR缺陷特征消失可能与肿瘤细胞克隆选择有关,增强了对铂类化疗的敏感性;GR高表达可能反映肿瘤的化疗耐药状态,经PIKTOR预处理后可逆转耐药,恢复肿瘤对治疗的敏感性;5种蛋白的低表达提示DDR缺陷、免疫抑制状态减弱及增殖能力降低,共同促进了肿瘤对后续化疗及免疫治疗的敏感性。本研究的创新性在于,首次在经化疗预处理的转移性TNBC中,系统解析了PIKTOR预处理后多组学层面的Biomarker变化,明确了治疗前GR高表达、治疗后TMB升高及5种蛋白低表达可作为患者从序贯治疗中获益的潜在预测指标,为临床筛选获益患者提供了可量化的分子依据。