1. 领域背景与文献引入
文献英文标题:Circulating Tumor DNA from Ascites as an alternative to tumor sampling for genomic profiling in ovarian cancer patients;发表期刊:Biomarker Research;影响因子:未公开;研究领域:卵巢癌精准诊疗、液体活检与生物标志物研究
卵巢癌是妇科恶性肿瘤中死亡率最高的亚型,基因组检测(尤其是同源重组缺陷(HRD)和BRCA基因突变检测)是指导铂类化疗及PARP抑制剂靶向治疗的核心依据。领域共识:约25%的高级别卵巢癌患者存在胚系或体细胞BRCA1/2突变,50%的高级别卵巢癌患者存在HRD,这类患者对铂类化疗和PARP抑制剂敏感性更高。当前领域的核心问题在于,组织活检作为HRD检测的金标准,存在较高的检测失败率(约20%晚期卵巢癌患者组织HRD检测无结果),且诊断或复发阶段的有创活检可能因患者身体状况、肿瘤位置等因素无法实施;外周血液体活检作为无创检测手段,存在循环肿瘤DNA(ctDNA)含量低、化疗期间检测灵敏度受限等局限性。而卵巢癌患者在诊断和复发阶段常伴有腹水生成,腹水中可能富含肿瘤来源的游离DNA(cfDNA),但此前针对腹水中cfDNA用于HRD和BRCA检测的可行性研究较为匮乏,因此本研究旨在评估腹水中cfDNA检测基因组不稳定性评分(GIS)以判断HRD状态的可行性,为无法获取组织样本的卵巢癌患者提供替代检测途径。
2. 文献综述解析
作者以卵巢癌基因组检测的技术路径(组织活检vs液体活检)为分类维度,系统梳理了现有研究的优势与局限性,明确了腹水中cfDNA作为替代检测样本的研究空白。
现有研究中,组织活检是HRD和BRCA检测的标准方法,能精准反映肿瘤的基因组特征,为临床治疗决策提供直接依据,但该方法存在样本获取困难、有创操作风险高、检测失败率高(约20%晚期患者组织检测无贡献结果)等局限性;外周血液体活检作为无创检测手段,已在肿瘤早筛、疗效监测等场景得到应用,但外周血中ctDNA含量较低,尤其是化疗期间肿瘤负荷降低时,检测灵敏度难以保障,无法满足HRD检测的需求。本文的创新价值在于首次针对卵巢癌患者腹水中的cfDNA开展系统研究,证明腹水中cfDNA含量高、肿瘤特异性强,其体细胞拷贝数改变(SCNA)谱与组织样本高度一致,可作为HRD和BRCA检测的有效替代样本,填补了卵巢癌液体活检领域中腹水样本应用的研究空白。
3. 研究思路总结与详细解析
本研究的核心目标是评估腹水中cfDNA用于HRD和BRCA检测的可行性与实用性,核心科学问题为腹水中cfDNA是否能准确反映肿瘤的基因组特征,替代组织样本完成HRD检测;技术路线遵循“样本采集→肿瘤源性验证→基因组特征分析→临床可行性验证”的闭环逻辑,通过前瞻性入组患者、多组学检测及回顾性分析,系统验证了腹水中cfDNA的临床应用价值。
3.1 患者入组与腹水样本采集
实验目的是获取卵巢癌患者的腹水样本,明确腹水在临床中的获取可行性,为后续基因组分析提供样本基础。方法细节为前瞻性入组NCT03010124研究中的20例疑似或确诊卵巢癌患者,共采集29份腹水样本,每份样本取1-4ml经双离心处理的新鲜腹水;同时回顾性分析100例连续接受诊断或间隔腹腔镜手术的高级别卵巢癌患者的手术记录,统计腹水的发生率及体积范围。结果解读显示,20例患者共采集29份腹水样本,回顾性分析发现97%的患者存在可见腹腔积液,腹水体积中位数为500ml(范围50-11000ml),新辅助化疗后仍有40%的患者存在腹水,体积中位数150ml(范围80-5000ml),说明腹水在卵巢癌患者中获取可行性极高,大部分患者可通过腹水样本完成基因组检测。文献未提及具体实验产品,领域常规使用一次性离心管、移液器、低温冰箱等样本处理与存储设备。
3.2 腹水中cfDNA提取与肿瘤源性验证
实验目的是提取腹水中的cfDNA,并确认其为肿瘤来源,排除正常细胞cfDNA的干扰。方法细节为从双离心后的腹水中提取cfDNA,采用靶向二代测序(NGS)检测TP53基因突变,分析突变的等位基因频率以判断cfDNA的肿瘤源性。结果解读显示,93%(27/29)的样本可检测到cfDNA,中位含量为1120ng(范围24-5732ng),即使化疗期间采集的样本也可检测到cfDNA;27份可检测cfDNA的样本中100%检测到有害突变,中位等位基因频率为60%(范围3.3-87%),其中92%(25/27)的样本检测到TP53突变,充分证明腹水中的cfDNA为肿瘤源性。
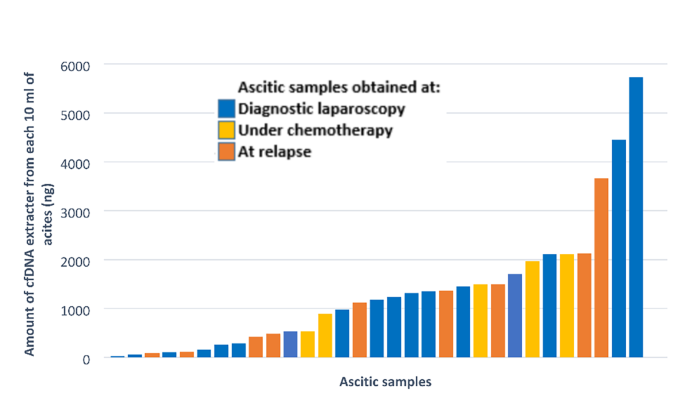
文献未提及具体实验产品,领域常规使用cfDNA提取试剂盒、靶向NGS测序文库构建试剂盒、Illumina系列测序平台等。
3.3 SCNA分析与HRD状态验证
实验目的是通过腹水中cfDNA的SCNA分析计算GIS,判断HRD状态,并与组织样本的基因组特征对比,验证腹水cfDNA的检测准确性。方法细节为采用单核苷酸多态性(SNP)阵列分析腹水中cfDNA的体细胞拷贝数改变(SCNA),计算GIS以评估HRD状态;对同时拥有组织样本的患者,对比腹水cfDNA与组织样本的SCNA谱。结果解读显示,17例患者的SCNA分析结果显示,11例患者GIS高(判定为HRD阳性),6例患者GIS低(判定为HRD阴性);4例已知BRCA突变的患者,其腹水中的GIS均为高;当同一患者同时拥有腹水和组织样本时,两者的SCNA谱高度重叠,说明腹水中cfDNA的基因组特征与组织样本完全一致。
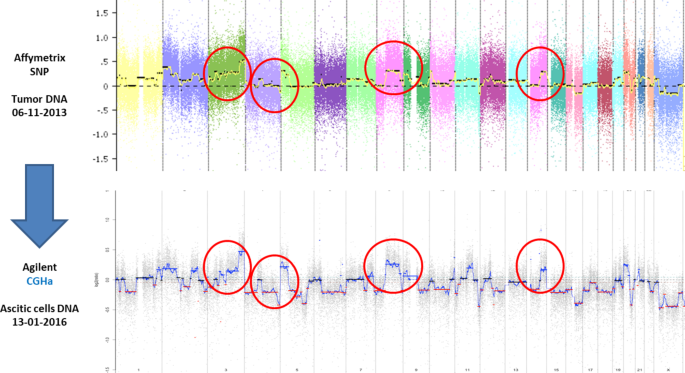
文献未提及具体实验产品,领域常规使用SNP阵列检测试剂盒、基因组分析软件(如CopyNumber、Partek Genomics Suite)等。
4. Biomarker研究及发现成果解析
本文聚焦的Biomarker为卵巢癌患者腹水中的肿瘤源性cfDNA,通过多步骤验证明确其可作为HRD和BRCA检测的替代Biomarker,为卵巢癌精准诊疗提供了新的检测途径。
Biomarker定位:本研究中的Biomarker为卵巢癌患者腹水中的肿瘤源性游离DNA(cfDNA),筛选与验证逻辑为:前瞻性采集卵巢癌患者腹水样本→提取cfDNA→靶向NGS检测TP53突变确认肿瘤源性→SNP阵列分析SCNA计算GIS→对比组织样本验证基因组特征一致性,形成完整的筛选与验证链条。研究过程详述:该Biomarker来源于卵巢癌患者的新鲜腹水样本(经双离心处理以去除细胞成分),验证方法包括靶向NGS检测TP53突变(确认肿瘤源性)、SNP阵列分析SCNA计算GIS(评估HRD状态);特异性方面,27份可检测cfDNA的样本中100%检测到有害突变,中位等位基因频率为60%(n=27,P值未明确提供),TP53突变检出率为92%(n=27),充分证明腹水中cfDNA的肿瘤特异性;敏感性方面,93%的腹水样本可检测到cfDNA,即使化疗期间采集的样本也可成功检出,说明该Biomarker的检测敏感性较高;ROC曲线、特异性与敏感性的具体统计数据未在文献中提及。核心成果提炼:腹水中的肿瘤源性cfDNA可作为HRD和BRCA检测的有效替代Biomarker,其GIS评分与组织样本高度一致,4例已知BRCA突变的患者腹水中GIS均为高(n=4,P值未明确提供);创新性在于首次系统证明腹水中cfDNA用于卵巢癌HRD和BRCA检测的可行性,为无法获取组织样本的卵巢癌患者提供了无创、高效的检测途径;统计学结果显示,研究共纳入20例患者(29份腹水样本),17例完成SCNA分析的患者中,64.7%(11/17)为高GIS(HRD阳性),35.3%(6/17)为低GIS(HRD阴性),样本量及分组比例明确。